Хидеаки Такахата
1 Отделение по неврохирургия, Национална болнична организация, Медицински център Нагасаки, Нагасаки, Япония
Кейсуке Цуцуми
1 Отделение по неврохирургия, Национална болнична организация, Медицински център Нагасаки, Нагасаки, Япония
Хироши Баба
1 Отделение по неврохирургия, Национална болнична организация, Медицински център Нагасаки, Нагасаки, Япония
Изуми Нагата
2 Катедра по неврохирургия, Университет Нагасаки, Висше училище по биомедицински науки, Нагасаки, Япония
Масахиро Йонекура
1 Катедра по неврохирургия, Национална болнична организация, Медицински център Нагасаки, Нагасаки, Япония
Резюме
Заден план
Инсултът е основна причина за дисфагия, но малко се знае кога и как пациентите с дисфагия трябва да бъдат хранени и лекувани след остър инсулт. Целта на това проучване е да установи осъществимостта, рисковете и клиничните резултати от ранните интензивни грижи за устната кухина и нова структурирана политика за орално хранене при логопед/езиков терапевт/медицинска сестра при пациенти с остър вътремозъчен кръвоизлив (ICH).
Методи
Общо 219 пациенти със спонтанен ICH, които са приети в нашата институция от 2004 до 2007 г., са анализирани ретроспективно. Програма за ранна интервенция за орално хранене, която се състоеше от интензивни грижи за устната кухина и ранни поведенчески интервенции, беше въведена от април 2005 г. и напълно работеща до януари 2006 г. Резултатите бяха сравнени между група за ранна интервенция от 129 пациенти, назначени след януари 2006 г., и исторически контрол група от 90 пациенти, наети между януари 2004 г. и март 2005 г. Използвана е техника на логистична регресия, за да се коригират базовите разлики между групите. За да се анализира времето за постигане на перорално хранене, се използва методът на Каплан-Майер и моделът на пропорционален риск на Кокс.
Резултати
маса 1
Функционална скала за орален прием (FOIS) [17]
| Ниво 1: | Нищо през устата. |
| Ниво 2: | Тръба зависима с минимални опити за храна или течност. |
| Ниво 3: | Тръба зависима от постоянен прием на храна или течност през устата. |
| Ниво 4: | Общо орално хранене с една консистенция. |
| Ниво 5: | Пълна орална диета с множество консистенции, но изискваща специална подготовка или компенсации. |
| Ниво 6: | Пълна орална диета с множество консистенции без специална подготовка, но със специфични хранителни ограничения. |
| Ниво 7: | Пълна орална диета без ограничения. |
Статистически анализ
Връзките между изходните характеристики и клиничните променливи в двете групи бяха оценени с χ 2 тест или точен тест на Fisher за категорични променливи и t-тест на Student за количествени данни. Приложен е и логистичен регресионен анализ за идентифициране на клиничните променливи, които са значително свързани с перорален прием без хранителни добавки (FOIS резултат 4-7). Кривите на Каплан-Майер бяха използвани за оценка на кумулативната скорост на преживяемост без хранителни добавки (оценка на FOIS ≥ 4) и бяха сравнени с резултатите от статистиката на log-rank. За оценка на коригираното съотношение на риска е използван многовариатен модел на пропорционален риск на Cox. Статистическата обработка беше извършена с помощта на софтуерните програми GraphPad Prism 4 (GraphPad Software Co. Ltd, CA, USA) и HALBAU7 (CMIC Co. Ltd, Tokyo, Japan).
Резултати
Няма значителни разлики в демографските данни, GCS оценката при приемането, местоположението на хематома или обема на хематома между двете групи. Пациентите с предшестваща анамнеза за инсулт или хронично бъбречно заболяване, които се нуждаят от хемодиализа, са разпределени по равно. Никой пациент не е бил подложен на хранене в сонда преди приемане (Таблица (Таблица2 2).
Таблица 2
| Демография | |||
| Възраст, години (SD) | 68,0 (12,7) | 69,2 (11,7) | 0,646 |
| Жена, n (%) | 40 (44,4) | 51 (39,5) | 0,468 |
| Тежест, n (%) | |||
| GCS 13-15 | 51 (56,7) | 86 (66,7) | |
| GCS 9-12 | 20 (22,2) | 28 (21,7) | |
| GCS 3-8 | 19 (22,2) | 15 (11,6) | 0,141 |
| Местоположение на хематома, n (%) | |||
| Supratentorial | 68 (75,6) | 109 (84,5) | 0,098 |
| Страна на хематома, n (%) | |||
| Нали | 30/68 (44.1) | 48/109 (44,0) | 0,992 |
| Обем на хематома, ml (SD) | |||
| Supratentorial | 33,0 (29,5) | 26,4 (28,8) | 0,147 |
| Инфранториал | 14,5 (14,0) | 13,2 (10,6) | 0,739 |
| Основно съпътстващо заболяване, n (%) | |||
| История на инсулт | 22 (24,4) | 33 (25,6) | 0,849 |
| CKD с HD | 5 (5,6) | 9 (7,0) | 0,672 |
| Деменция | 4 (4.4) | 7 (5.4) | 1.000 |
| История на гръдно заболяване | 1 (1.1) | 6 (4.7) | 0,141 |
| Текущ дим | 17 (18,9) | 34 (26,4) | 0,198 |
| Хирургична процедура, n (%) | |||
| Обща сума | 41 (45,6) | 33 (25,6) | 0,002 |
| Трепанация | 15 (16,7) | 8 (6,2) | 0,013 |
| Краниотомия | 26 (28,9) | 25 (19,4) | 0.101 |
Данните са дадени като n (%) или средно (SD). Болестта на гръдния кош включва пневмония, хронична обструктивна белодробна болест, астма и белодробен тумор.
Съкращения: GCS, скала на кома в Глазгоу; ХБН, хронично бъбречно заболяване; HD, хемодиализа.
Едномерните сравнения показват, че делът на пациентите с FOIS резултат 4-7 е значително по-висок в групата за ранна интервенция в сравнение с контролната група (86,8% (112/129) срещу 67,8% (61/90); коефициент на шансовете 3,13, 95% CI, 1,59-6,15; P (Таблица 3). 3). Честотата на инфекция на гръдния кош е била по-ниска в групата за ранна интервенция (20,9% (27/129) срещу 35,6% (32/90); съотношение на шансовете 0,48, 95% CI, 0,26-0,88; P = 0,016) и употребата на антибактериалните лекарства значително намалява в групата за ранна интервенция, от 16,3 на 6,1 флакона на пациент (P = 0,009).
Таблица 3
| Първичен резултат, n (%) | ||||
| Смърт | 7 (7,8) | 2 (1.6) | 0,034 | 0,19 (0,04-0,92) |
| FOIS 1 | 17 (18,9) | 8 (6,2) | ||
| FOIS 2, 3 | 5 (5,6) | 7 (5.4) | ||
| FOIS 4-6 |
Таблица 4
Коригирано съотношение на шансовете: резултати от логистичен регресионен анализ
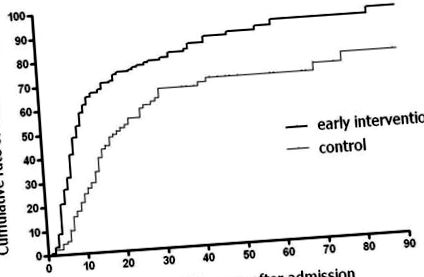
| Възраст (години) | 0,93 (0,89-0,97) | (Фигура 1). 1). Коригираното съотношение на риска при използване на модел на пропорционален риск на Cox за ранна намеса е 2,07 (95% CI, 1,50-2,86; P (Таблица 5 5). |
Въпреки че това е проучване за перорално хранене, диагнозите на дисфагия не са били поставяни преди започване на лечението, тъй като интервенциите (като рехабилитация на устата, релаксация на шията и обучение за седнали позиции) предшестват официалните диагностични тестове за дисфагия в нашия протокол . Вместо да бъдат диагностицирани, пациентите са получили както грижи, така и интервенции скоро след приемането, тъй като са били изложени на риск от усложнения, свързани с дисфагия. При пациенти с остър инсулт започването на грижи и интервенции след поставяне на официална диагноза може да е твърде късно, тъй като обичайните клинични тестове за дисфагия не са приложими за пациенти с тежки увреждания, които са изложени на по-голям риск от усложнения, свързани с дисфагия. Следователно, това проучване включва всички пациенти с ICH и сравнява общите резултати между двете групи.
В това проучване има няколко слабости. Това беше ретроспективно кохортно проучване, проведено в един център с неизбежни пристрастия и ограничения. Потенциално пристрастие възниква и от ретроспективното прилагане на резултатите от неслепи наблюдатели. Редица терапевтични интервенции, използвани в групата за ранна интервенция, затрудняват извеждането на коя част от този режим на лечение може да носи основната отговорност за резултата. Тези слабости обаче могат отчасти да отразят настоящите проблеми при провеждането на рандомизирано контролирано проучване (RCT) относно приема на храна при тежко засегнати пациенти с инсулт без обща мярка за преглъщане.
Трудно е да се проведе пробно интервенционно проучване на ежедневните грижи, когато пациентите с инсулт и членовете на техните семейства предпочитат по-специални грижи. Също така е трудно да се извърши двойно-сляпо проучване на поведенческата интервенция, което отнема седмици, за да се осъществи, защото пациентите, които участват в проучването, в крайна сметка могат да разпознаят, че са били поставени в отделни контролни групи. Това препятствие е споменато от Carnaby et al [19] в техния RCT, в който не са наблюдавани значителни разлики между лечебната и контролната групи, използвайки log-rank теста. FOIS, който е приложим за пациенти в безсъзнание, беше предоставен едва наскоро. Тези причини вероятно са причините, поради които в миналото не е имало проспективни, многоцентрови, двойно-сляпи опити за рехабилитация при дисфагия [18,23]. По-нататъшните проучвания трябва да оценяват проспективно и поотделно ефектите от интензивна орална грижа и ранна интервенция при тежко засегнати пациенти с остър инсулт в бъдеще.
В това проучване ефектите от ранната интервенция са ретроспективно сравнени с предишни резултати. По този начин периодът на проследяване беше кратък и непоследователен. Въпреки това, получените криви на Каплан-Майер за нашите пациенти разкриват значително и бързо подобрение на способността за преглъщане в групата за ранна интервенция и кривите не се пресичат. В допълнение, резултатите, получени от едномерните методи, са в съответствие с тези, получени от многомерните методи както в категориалния анализ, така и в анализа на оцеляването. Тези последици изглежда подкрепят ефикасността на ранната намеса. Въпреки че няма предишни проучвания за преглъщане на дисфункция при тежки пациенти с ICH, нашите данни за функционалната независимост и смъртност, получени през контролния период, са сравними с резултатите, докладвани в литературата [24]. Следователно нашите данни за функцията на преглъщане, получени през 2004 и 2005 г., изглеждат точни.
Заключения
Ранното започване на перорално хранене след достатъчна подготовка може безопасно да подобри клиничните резултати на пациентите с ICH по отношение на преживяемостта, честотата на гръдната инфекция, продължителността на престоя в болницата и функцията на преглъщане. Обща мярка за изход при преглъщане, която може да се приложи при всеки пациент, може да бъде жизненоважна при изследването на хранителните проблеми и при установяването на базирани на факти практики за лечение на дисфагия. Техниките, използвани в това проучване, могат да се използват безопасно и евентуално с достатъчно полза, за да се оправдае RCT. По-нататъшни проучвания и многоцентрово РКИ трябва да се извършват в бъдеще, за да се подобри пероралното хранене при пациенти с инсулт.
Съкращения
ICH: вътремозъчен кръвоизлив; SLT: логопед и логопед; CT: компютърна томография; GCS: скала на кома в Глазгоу; mRS: модифицирана скала на Ранкин; GOS: Мащаб на резултатите от Глазгоу; FOIS: функционална скала за орален прием; RCT: рандомизирано контролирано проучване.
Конкуриращи се интереси
Хидеаки Такахата, доктор по медицина: Няма
Keisuke Tsutsumi, MD: Няма
Хироши Баба, доктор по медицина: Няма
Изуми Нагата, доктор по медицина: Няма
Масахиро Йонекура, доктор по медицина: Няма
Принос на авторите
HT участва в разработването и дизайна на изследването, провежда и контролира оценки и процедури в рамките на проучването, преглежда и интерпретира данни и участва в разработването на ръкописа. KT и HB участваха в разработването и дизайна на проучването, провеждаха и контролираха оценките в рамките на проучването и контролираха и участваха в разработването на проекта. IN и MY контролираха, предоставиха критичен преглед на проекта и участваха в разработването на ръкописа. Всички автори прочетоха и одобриха окончателния ръкопис.
История преди публикацията
Историята на предварителната публикация за тази статия можете да видите тук:
Благодарности
Авторите биха искали да благодарят на г-жа Tokie Ide и г-жа Aya Kondoh за ценната помощ при събирането на данни, както и на г-жа Shiho Fushitani за ръководството и обучението на медицинските сестри и лечението на пациентите. Бихме искали да благодарим и на сестринския персонал на отделението, чиято всеотдайна помощ беше необходима за успешното завършване на това проучване.
Тази работа беше представена отчасти на годишната среща на Японското общество за рехабилитация на дисфагия през 2009 г.
Това проучване беше подкрепено с грант за изследване от нашата болница за публикацията.
- Хранене и хранене в ранна детска възраст - Рано развитие и възпитание на деца (3-7)
- Диетична интервенция при чувствителни към храна пациенти с IgA нефропатия - изглед в пълен текст
- Ранно хранене на кърмачета с формула или твърди храни и риск от наднормено тегло или затлъстяване при деца в
- Ранно хранене след обръщане на илеостомия на веригата Проспективно проучване - ScienceDirect
- Ранното хранене след лигиране на варикозна лента на хранопровода при цироза е безопасно Рандомизирано контролирано