Субекти
Резюме
Промените в начина на живот като висока консумация на преработени храни, богати на мазнини и захар и заседнал начин на живот са свързани с нарастващото разпространение на метаболитен синдром (MetS), който засяга около 35% сред американското население. MetS е основният рисков фактор за захарен диабет, който е свързан със съдови промени в ретината. Ранните последици от MetS в ретината обаче не са добре описани. Следователно ние имаме за цел да характеризираме ранните ефекти на диетата с високо съдържание на фруктоза и високо съдържание на мазнини (HFHF) върху функцията и структурата на ретината на плъховете и да оценим връзките с метаболитните промени. Кафявите норвежки плъхове на възраст 6 седмици са били хранени в продължение на 8 дни, 5 седмици или 13 седмици с HFHF диета или стандартна чау. Само след 4 седмици от тази диета, плъховете демонстрират намаляване на чувствителността на конусния фоторецептор към светлина. Нещо повече, ние забелязахме, че MetS значително влошава индуцираната от лазера хороидална неоваскуларизация съответно със 72% и 67% 2 седмици и 3 седмици след лазерно лечение. Тези аномалии на ретината са свързани с дерегулация на метаболизма на глюкозата, но не и с липидния метаболизъм. Тези данни показват модификации на ретината в HFHF-индуциран MetS при плъхове, в много ранен стадий на заболяването.
Въведение
Трябва да се отбележи, че нито едно проучване, използващо само фруктоза, включително нашите 14, не рекапитулира всички клинични характеристики на MetS, включително дислипидемия и хипергликемия, от една страна, и промени в ретината, от друга страна.
В настоящото проучване предположихме, че диетата с високо съдържание на фруктоза и високо съдържание на мазнини би била достатъчна, за да предизвика промяна в MetS и ретината при плъховете. За тази цел ние характеризирахме последиците от храненето на кафяви норвежки плъхове с 60% фруктоза - 9% наситена мазнина, зависима от времето върху метаболизма на липидите и глюкозата, както и върху функционирането и развитието на съдови промени в ретината.
Резултати
Диетата с HFHF предизвиква увеличаване на телесните мазнини, но не и на телесното тегло
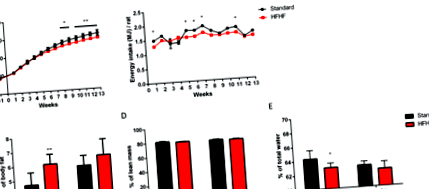
Консумацията на храна и телесното тегло на плъховете се записват ежеседмично по време на целия експеримент. Както е показано на фиг. 1А, стандартно хранените плъхове са имали значително по-високо телесно тегло, отколкото плъховете, хранени с диета с HFHF, от 8 седмици диета до края на експеримента (P Фигура 1
Съставът на тялото се измерва чрез неинвазивен EchoMRI. Плъховете, хранени с HFHF, са имали по-голяма телесна мастна маса от плъховете от стандартната диета на 5 седмици диета (P Фигура 2
Цитокините в плазмата също бяха оценени във всяка времева точка, показана на фиг. 2C, F, I. Нивата на TNFα при 8-дневно хранене са били под границата на откриване на чувствителността към luminex. Няма разлика в нивата на инсулин, лептин, IL1β и TNFα на 8 дни и 5 седмици хранене между двете диети. Инсулинемията е била по-висока при плъхове, хранени с HFHF с диета на 13 седмици диета (P = 0,07). Освен това се наблюдава двукратно увеличение на плазменото ниво на TNFa (P Фигура 3
HFHF диета, индуцирана чернодробна стеатоза
Хепатосоматичният индекс е по-висок при плъхове, хранени с HFHF на 5 седмици (P Фигура 4
Диетата с HFHF индуцира намаляване на чувствителността на конуса
ERG отговор
HFHF диетата насърчава хороидалната неоваскуларизация в ретината
Ретиналните и хориоидалните васкулатури са оценени с помощта на cSLO ангиография след инжектиране на флуоресцеин и индоцианиново зелено (ICG) багрила, съответно. Ангиографията се извършва 1, 2 и 3 седмици след индуцирането на хориоидална неоваскуларизация с лазерни въздействия в мембраната на Bruch. Флуоресцеинът съответства на васкуларизацията на ретината, докато индоцианиновото зелено разкрива хориоидална васкуларизация. Използването на кафяви норвежки пигментирани плъхове позволи да се направи разлика между двете съдови системи. Флуоресцеиновата ангиография не показва разлики между HFHF диетата и стандартната диета (допълнителна фигура 3). Въпреки това, ICG ангиографията разкрива увеличение на хориоидалната неоваскуларизация на 2 седмици (Фиг. 6, + 71%, Р Фигура 6
HFHF диета, индуцирана глиоза на ретината
Активирането на клетките на Müller се оценява чрез полуколичествено определяне на имуномаркирането срещу глиалния фибриларен киселинен протеин (GFAP). Имунореактивността се оценява от „без петна“ до „силна“, използвайки стандартизирана процедура, от ретини на HFHF диети, хранени с плъхове и стандартно хранени плъхове. Резултатите изразяват процента на 4-те етапа на активиране на клетките на Мюлер в ретината. Ослепеното точкуване разкрива по-високо оцветяване на GFAP клетки в HFHF ретини в сравнение със стандартните ретини (Фиг. 7, Р Фигура 7
Дискусия
Диабетната ретинопатия (DR) и свързаната с възрастта макулна дегенерация (AMD) споделят общи патогенни пътища като клетъчен възпалителен отговор и оксидативен стрес. Систематичен преглед и мета-анализ на литературата разкрива, че диабетът ще бъде рисков фактор за неоваскуларната форма на напреднала ВМД (ИЛИ = 1,48 [1,44–1,51, 95% ДИ] от проучвания в напречно сечение; ИЛИ = 1,15 [1,11– 1,21, 95% CI] от проучвания за контрол на случаите) 16. Данните от проучването на очите на Blue Mountains в Австралия показват, че затлъстяването, високата глюкоза и високият триглицерид са свързани с повишената честота на късно AMD по време на 10-годишно проследяване 2. Повечето модели на диабет при гризачи показват късни събития на AMD, докато ранните биомаркери за ретинална дисфункция все още липсват Освен това аномалиите на ретината се развиват много по-рано от началото на клиничното изследване. По този начин е необходим подходящ модел на инсулинова резистентност и непоносимост към глюкоза, свързани с ранна дисфункция на ретината, като потенциално ценен инструмент за изследване на приноса на всеки рисков фактор за развитието на AMD и DR, в комбинация с други модели на плъхове.
Сред параметрите на функцията на ретината, чувствителността само на конусите е значително намалена чрез HFHF диета. Това откритие би било от значение за ефекта на диабета върху човешкото зрение. В действителност, хората с диабет тип 1 за по-малко от 5 години са имали слабо увреждане на зрението, като загуба на синьо чувствително цветно зрение без видими аномалии или промени в ретината по време на внимателен офталмоскопски преглед 26. Друго скорошно проучване съобщава за връзка при увреждане на цветното зрение при диабет без ретинопатия 27. Това намаляване на чувствителността на фоторецепторите изглежда е ранен показател за невродегенеративни симптоми и че невронното увреждане предхожда клиничната ретинопатия.
При хората често се появява дислипидемия, т.е.повишаване на триглицеридите, общия холестерол и LDL-холестерола, докато се наблюдава хиперинсулинемия 28. Друго проучване на Crapo и сътрудници 29 демонстрира, че диетата с високо съдържание на фруктоза предизвиква хипертриглицеридемия при диабетици. Ние предположихме, че липсата на HFHF диетичен ефект върху гладуващата инсулинемия може да обясни защо HFHF диетата не е ефективна при предизвикване на дислипидемия при плъхове от Браун Норвегия.
Дебатът все още е открит, за да се открие произходът на функционалните промени в ретината по време на метаболитен синдром. От нашия модел ние постулираме, че дерегулацията на метаболизма на глюкозата би била ключовото събитие при появата на аномалии на ретината, т.е. намалена чувствителност на конуса. Въпреки че тези промени са слаби, ние постулираме, че дерегулациите в метаболизма на глюкозата са достатъчни, за да създадат благоприятна среда за неоваскуларни и невронални усложнения в ретината.
Материали и методи
Животни
Експериментална процедура, предназначена за намаляване на броя на използваните животни и усъвършенстване на процедурата. GTT: тест за толерантност към глюкоза, ITT: тест за толерантност към инсулин, ERG: електроретинография.
- Диетата, богата на животински протеини, е свързана с по-голям риск от ранна смърт - ScienceDaily
- Сравнение на нискокалорична високо протеинова и нискокалорична стандартна протеинова диета с обиколка на талията
- Диетична диаграма за пациент с високо кръвно налягане, Диетична диаграма с високо кръвно налягане Либрат
- Пиенето на две или повече диетични газирани напитки на ден, свързани с висок риск от инсулт, инфаркти - CNN
- Dukan Diet Диета с високо съдържание на протеини, която да ви помогне да отслабнете и да го запазите за цял живот от Williams,