Пол Холвоет
Отдел за атеросклероза и метаболизъм, Катедра по сърдечно-съдови науки, KU Льовен, Herestraat 49, P.O. Box 705, 3000 Льовен, Белгия
Резюме
1. Въведение
До 2015 г. приблизително 2,3 милиарда възрастни ще бъдат с наднормено тегло и повече от 700 милиона ще бъдат със затлъстяване според прогнозите на Световната здравна организация. Понастоящем Съединените щати (САЩ) са най-големият единичен пазар за лекарства за отслабване, като около 68% от населението е или с наднормено тегло, или със затлъстяване, следвано от Обединеното кралство и други европейски страни. Само в САЩ над 9 милиона деца и тийнейджъри са със затлъстяване. Нещо повече, Китай, Русия, Индия и Бразилия скоро биха могли да започнат да надминават западните страни по своето затлъстело население.
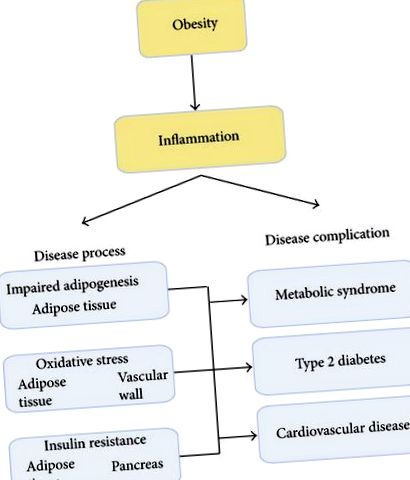
Първата ни цел е да покажем, че затлъстяването е състояние на хронично възпалително заболяване, което е свързано с други болестни процеси като ремоделиране на мастната тъкан (AT), оксидативен стрес и инсулинова резистентност (IR). Тези болестни процеси допринасят за развитието на диабет тип 2 (T2DM) и метаболитния синдром (MetS) [1]. MetS е често срещано и сложно разстройство, съчетаващо затлъстяване, дислипидемия, хипертония и IR [2–5]. Той е основен рисков фактор за T2DM и сърдечно-съдови заболявания (ССЗ) [3, 6–13] (Фигура 1).
Схематично представяне на централната роля на възпалението при разстройства, предизвикани от затлъстяването. Възпалителното състояние, свързано с прекомерен прием на калории по време на затлъстяване, индуцира ремоделиране на мастната тъкан, оксидативен стрес и инсулинова резистентност, свързано с повишен риск от развитие на метаболитен синдром, диабет тип 2 и сърдечно-съдови заболявания.
Втората ни цел е да анализираме ефектите от поведението и личните фактори и факторите на стрес върху развитието на затлъстяването и свързаните с него разстройства. Ние наблягаме на ефектите на стресовите фактори върху загубата на епигенетични регулаторни механизми на болестните процеси, с основен фокус върху възпалението.
Накрая обсъждаме ограниченията на настоящото противовъзпалително и антиоксидантно лечение на затлъстяването и свързаните с него метаболитни и сърдечно-съдови нарушения, като показваме неподходящия им контрол върху болестните процеси.
2. Затлъстяването е хронично възпалително заболяване
Нискостепенното възпаление е характеристика на състоянието на затлъстяване (Фигура 2). Циркулиращите концентрации на много възпалителни маркери при затлъстели лица са по-високи, отколкото при слабите хора и се смята, че те играят роля в причиняването на IR и други метаболитни нарушения. Възпалителните маркери са по-високи и при АТ на затлъстели хора; те се секретират от инфилтриращи макрофаги и от самите адипоцити. Концентрациите на възпалителни маркери в кръвта се понижават след загуба на тегло [14]. Храните с високо съдържание на глюкоза и с високо съдържание на мазнини могат да предизвикат възпаление след хранене. Последното се влошава от крайни продукти за гликиране (AGE) и частично се компенсира от включването на някои антиоксиданти или храни, съдържащи антиоксиданти в храната [15].
Нискостепенно хронично възпаление и оксидативен стрес в мастната тъкан по време на затлъстяване. Прекомерното натрупване на мастна тъкан по време на затлъстяване се характеризира с набиране на имунни клетки. Активираните Т клетки и хемокини индуцират миграция на моноцити в мастните тъкани, където те се диференцират в провоспалителни M1 макрофаги. Взаимодействието между активирани Т клетки, макрофаги и дисфункционални адипоцити води до дисрегулиран адипокин и екзозомоподобно производство на везикули, причиняващо инсулинова резистентност (IR). Хипоксията на мастната тъкан по време на затлъстяване е свързана с производството на ROS и вол-LDL и образуването на пяна. В допълнение, хипоксията и повишеният оксидативен стрес предизвикват апоптоза на адипоцитите, допринасяйки за инсулинова резистентност.
В механично отношение цитокин-интерлевкин- (IL-) 1β се очертава като виден подбудител на провъзпалителния отговор при затлъстяване [16]. Всъщност липсата на Il-1 рецептор-I (Il-1RI) предпазва мишките от индуцирано от диета високо съдържание на мазнини възпаление, съвпадащо с подобрена глюкозна хомеостаза [17]. Друг подбудител на възпаление е NLR пирин, съдържащ домейн-3 (Nlrp3, известен също като Nalp3 или криопирин) инфламазома; индукцията му е свързана с IR. Аблация на Nlrp3 при мишки намалява Il-18 и интерферон-γ (Ifn-y) и подобрява инсулиновата сигнализация [18]. Повишената секреция на ангиопоетин-подобен протеин-2 (Angptl2) от AT също активира възпалителна каскада и индуцира хемотаксис на моноцити/макрофаги. Делецията на Angptl2 подобрява AT възпалението и системния IR при индуцирани от диета затлъстели мишки [19].
В допълнение, възпалението се причинява от промени в нивата на адипокини. Свръхекспресията на миши резистин, получен от адипоцити, води до ускорено възпаление на бяло AT (WAT), свързано с повишена липолиза и безсерумни мастни киселини (FA) и IR [20]. За разлика от това, адипоцитът, получен от адипоцити, предпазва от възпаление, като насърчава поляризацията на макрофагите към противовъзпалителен фенотип [21]. Увеличенията на адипонектин намаляват съдържанието на мазнини и възпалителните цитокини тумор-фактор на некроза- (Tnf-) α и Il-6 при затлъстели плъхове [22].
Като цяло приносът на възпалението при AT за развитието на затлъстяване е много подобен на приноса му за развитието на атеросклероза в артериалните тъкани [37–39]. Приносът на фенотипния превключвател от M2 към M1 макрофагите към възпалението и IR е от решаващо значение за това. Всъщност проучването I LIKE HOMe показа сходна хетерогенност на моноцитите при затлъстяване и субклинична атеросклероза. Индексът на телесна маса (ИТМ) е в значителна корелация с дебелината на каротидната интима-среда (IMT). Високият брой на CD16 (+) моноцити е бил значително свързан както с по-висок ИТМ, така и с повишен IMT на каротидната. Корекцията на броя на моноцитите CD16 (+) отслаби корелацията между ИТМ и каротиден IMT, което предполага, че увеличаването на броя на CD16 (+) моноцити при затлъстяване може отчасти да обясни връзката между затлъстяването и IMT [40].
3. Затлъстяването е свързано с метаболитен синдром
Затлъстяването често се групира с други сърдечно-съдови рискови фактори, като дислипидемия, хипертония и хипергликемия, в MetS. Третият доклад на експертната група на Националната образователна програма за холестерол за откриване, оценка и лечение на висок холестерол в кръвта при възрастни (ATPIII) подчертава значението на лечението на пациенти с MetS за предотвратяване на ССЗ [2]. Той определя компонентите на MetS като (1) обиколка на талията ≥102 cm при мъжете и ≥88 cm при жените; (2) триглицериди на гладно ≥150 mg/dL (1,70 mmol/L); (3) HDL-холестерол 12 години). Повишеният вол-LDL, но не и повишеният LDL-холестерол, е свързан с по-висок риск от бъдещи MetS. Повишената вол-LDL е свързана особено с честотата на коремно затлъстяване, хипергликемия и хипертриглицеридемия [49].
Повишаването на вол-LDL във връзка с MetS и атеросклероза може да се дължи на загуба на антиоксидантна способност, причинена от ниска серумна активност на антиоксидантния ензим супероксиддисмутаза (SOD) [59] или ниска HDL-асоциирана параоксоназна (PON) антиоксидантна активност [58] . Повишаването на вол-LDL може да се дължи и на повишен оксидант капацитет, например чрез увеличена експресия на NADPH оксидаза (NOX). Всъщност производството на реактивни кислородни видове (ROS) се е увеличило селективно в AT на затлъстели мишки, причинено от по-висока експресия на Nox и намалена експресия на антиоксидант SOD. В култивираните адипоцити повишената FA увеличава оксидативния стрес чрез активиране на Nox, а оксидативният стрес намалява производството на адипонектин и увеличава Il-6 и Mcp-1. И накрая, при затлъстели мишки, лечението с инхибитор на Nox намалява ROS в AT, намалява възпалителните адипокини и намалява диабета, хиперлипидемията и чернодробната стеатоза [60].
5. Метаболитният синдром е свързан със сърдечно-съдови заболявания
Грунди и колеги са измерили серия от сърдечно-съдови рискови фактори при 59 820 мъже и 22 192 жени. Профилите на рисковите фактори бяха разделени на пет квинтили кардиореспираторна годност (CRF). С намаляването на CRF се наблюдава повишаване на затлъстяването, триглицеридите, съотношенията триглицериди/HDL липопротеини, кръвното налягане, MetS и диабет и тютюнопушенето [64]. В Тайванското проучване на кохортата на хипертонията, хипергликемията и хиперлипидемията, причиненият от MetS риск за ССЗ е 39% при мъжете и 44% при жените. От всички компоненти на MetS централното затлъстяване е имало най-високия популационен риск (PAR) при жените (57%), докато хипертонията е имала най-висок PAR при мъжете (57%) [65]. В Дзянсу, Китай, MetS е свързан с повече от два пъти по-висок риск от ССЗ след корекция за възраст, пол, пол, ИТМ, консумация на алкохол, фамилна анамнеза за ССЗ и тютюнопушене [66].
Juonala и сътр. извърши мета-анализ на данни от четири проспективни проучвания, за да определи дали този риск е намален при лица с наднормено тегло или затлъстяване като деца, но не и като възрастни. Средната продължителност на проследяването е била двадесет и три години. Субектите с постоянно висок статус на затлъстяване от детството до зряла възраст са имали пет пъти по-висок риск от T2DM и два пъти по-висок риск от хипертония и по-нисък HDL-холестерол, свързани с повишен IMT на каротидната артерия. Интересното е, че рисковете от тези резултати при деца с наднормено тегло или с наднормено тегло, които до зряла възраст са станали неносещи, са подобни на тези при лица, които никога не са били със затлъстяване.
6. Поведение и затлъстяване
Има все повече доказателства, че липсата на физически упражнения, тютюнопушене и богати на мазнини диети допринасят за развитието на затлъстяване и свързаните с това разстройства (Фигура 3).
- Кръглите червеи потушават затлъстяването и свързаните с него метаболитни нарушения - ScienceDaily
- Периваскуларна мастна тъкан като подходящо депа за мазнини за сърдечно-съдов риск при затлъстяване
- Ресвератролът и неговите човешки метаболити - ефекти върху метаболитното здраве и затлъстяването
- Един подход може да предотврати затлъстяването на тийнейджърите, хранителните разстройства, казват новите насоки - ScienceDaily
- Затлъстяване, загуба на тегло и условни сърдечно-съдови рискови фактори - Tzotzas - 2011 - Прегледи на затлъстяването