Сузане Махер
1 Катедра по серология на кръвната група и трансфузионна медицина, Медицински университет в Грац, Грац, Австрия
Камила Дрекслер
1 Катедра по серология на кръвната група и трансфузионна медицина, Медицински университет в Грац, Грац, Австрия
Инес Линденау
1 Катедра по серология на кръвната група и трансфузионна медицина, Медицински университет в Грац, Грац, Австрия
2 Катедра по вътрешни болести, Отдел по ендокринология и диабетология, Медицински университет в Грац, Auenbruggerplatz 15, 8036 Грац, Австрия
Назанин Саребан
1 Катедра по серология на кръвната група и трансфузионна медицина, Медицински университет в Грац, Грац, Австрия
Петер Шленке
1 Катедра по серология на кръвната група и трансфузионна медицина, Медицински университет в Грац, Грац, Австрия
Карин Амрейн
2 Катедра по вътрешни болести, Отдел по ендокринология и диабетология, Медицински университет в Грац, Auenbruggerplatz 15, 8036 Грац, Австрия
Резюме
Заден план
Около 2–3% от населението участва в програми за кръводаряване. Всяко даряване на цяла кръв или десет дарения за афереза причиняват загуба на 200–250 mg желязо. В резултат на това един от най-честите рискове при редовните кръводарители е дефицитът на желязо. Въпреки че това е известно от десетилетия, в повечето страни в момента състоянието на желязо не се оценява или лекува в тази популация. Жените в пременопауза са особено засегнати, тъй като имат по-ниски железни запаси и по-високи дневни нужди. Освен анемия, дефицитът на желязо може да доведе до умора и нарушена когнитивна и физическа работоспособност. Настоящите железни препарати за интравенозно приложение се понасят добре и позволяват прилагане на големи дози до 1 g за едно посещение. Нашата хипотеза е, че при донори на кръв с дефицит на желязо интравенозно приложеното желязо е по-ефективно и толкова безопасно, колкото и пероралното добавяне на желязо. Тъй като анемията е една от най-честите причини за отлагане на постоянни или периодични донори, поддържането на пълна с желязо донорна група може да помогне за предотвратяване на недостиг на кръвоснабдяване и за избягване на свързаните с дефицит на желязо съпътстващи заболявания.
Методи/дизайн
В това рандомизирано клинично проучване ние включваме мъже и жени донори на кръв на възраст ≥18 и ≤65 години със стойност на феритина ≤30 ng/ml. Стратифицирани по пол, участниците се рандомизират с уеб-базиран инструмент за рандомизация в съотношение 1: 1 към 1 g интравенозно приложена феридна карбоксималтоза или 10 g добавки от железен фумарат при една до две дневни дози от 100 mg всяка. Осем до 12 седмици след първото посещение, състоянието на желязото, кръвната картина и симптомите се оценяват и в двете групи. Основната крайна точка е разликата в наситеността на трансферин (%) след интервенцията между двете групи. Вторичните крайни точки включват други параметри на метаболизма на желязото и броя на червените кръвни клетки, броя на пациентите с нежелани събития, свързани с лекарството, и субективни симптоми, включително тези на синдрома на неспокойните крака, качеството на живот и умората.
Дискусия
Добавянето на желязо, прилагано интравенозно при неанемични, но дефицитни на желязо донори на кръв, може да представлява ефективна стратегия за защита на донорите на кръв от съпътстващи заболявания, свързани с дефицит на желязо, и следователно да подобри благосъстоянието на донорите на кръв. Освен това добавките с желязо ще помогнат за поддържането на напълнената с желязо донорна кръв.
Пробна регистрация
Електронен допълнителен материал
Онлайн версията на тази статия (doi: 10.1186/s13063-016-1648-y) съдържа допълнителен материал, който е достъпен за оторизирани потребители.
Заден план
Потенциалните рискове, свързани с терапията с желязо, включват маскиране на други причини за дефицит на желязо, претоварване с желязо при неразпозната хемохроматоза и свързани с лекарства нежелани ефекти. Резултатите от интервенционни проучвания в други условия показват, че тежките лекарствени реакции на орално и интравенозно желязо са редки и че стомашно-чревните странични ефекти се наблюдават по-рядко при интравенозно прилагано желязо, отколкото при перорални добавки с желязо [25, 28]. Анафилактични реакции обаче са описани при интравенозно приложение на желязо [29]. Нов, чест неблагоприятен ефект след интравенозната инфузия на желязо и по-често след инфузия на железна карбоксималтоза е хипофосфатемията, която може да бъде тежка и да доведе до дълбока слабост и дори остеомалация [30–33].
Цели и хипотеза на изследването
Това проучване ще оцени ефикасността, безопасността и осъществимостта на интравенозната инфузия на високи дози желязо при донори на кръв с дефицит на желязо чрез сравняване на интравенозно прилаганата ферокарбоксималтоза с орални добавки на железен фумарат.
Нашата хипотеза е, че 1 g интравенозно инфузирана феридна карбоксималтоза ще подобри състоянието на желязо на донорите на кръв с дефицит на желязо по-ефективно в сравнение със сравнима доза на перорални добавки с желязо (10 g, приемайки 10% степен на резорбция, дадена в продължение на 8-12 седмици).
Методи/дизайн
Контролен списък SPIRIT е достъпен онлайн за този ръкопис (Допълнителен файл 1).
Уча дизайн
Това е проспективно, рандомизирано клинично изпитване. Изследваната популация се състои от здрави възрастни, включително донори на афереза на цяла кръв и тромбоцити с дефицит на желязо (феритин ≤ 30 ng/ml).
Участници
Критерии за включване
Критериите за включване са както следва:
Възраст ≥ 18 години и ≤ 65 години
Дефицит на желязо (феритин ≤30 ng/ml при скрининг - обикновено преди кръводаряване)
Изпълнение на австрийските критерии за кръводаряване
Критерии за изключване
Критериите за изключване са както следва:
Бременност или кърмене
История на анафилаксия до интравенозна инфузия на желязо или други вещества
Признаци или симптоми, предполагащи остро или хронично стомашно-чревно или прекомерно гинекологично кървене
Проучване на лекарства/интервенция
Изследваните лекарства, използвани в интервенцията, са:
Високи дози (1000 mg) интравенозни инфузии на желязо (феридна карбоксималтоза, Ferinject ®, производител Vifor Pharma, Австрия) или
Перорални добавки от желязо (железен фумарат, Ferretab®, производител Gerot Lannach, Австрия) в съответна прогнозна доза> 10.000 mg (приемайки абсорбция от 10%, 100 капсули по 152 mg железен фумарат всяка), взети в продължение на 8-12 седмици. Участниците се съветват да приемат таблетки сутрин с портокалов или лимонов сок.
Резултати
Първична крайна точка
Първичната крайна точка е разликата в наситеността на трансферин (%) при посещение 1 между високите дози интравенозна инфузия и групата на пероралните добавки с желязо
Вторични цели
Вторичните цели са:
Други параметри на метаболизма на желязото, броя на червените кръвни клетки, включително процента на участниците с нормален (специфичен за пола) хемоглобин при посещение 1 (групово сравнение) и допълнителни параметри (напр. Фосфат)
Симптоми, включително тези на синдрома на неспокойните крака, качеството на живот, умората
Сравнение на двете лечения по отношение на честотата и тежестта на нежеланите събития, толерантността и спазването
Методи на процедурата
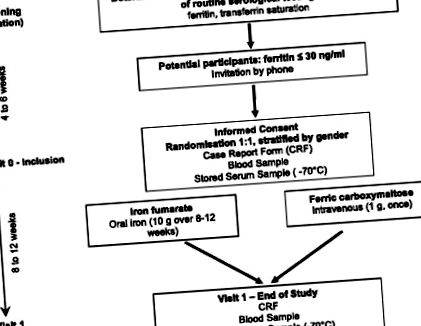
Схема на процедурата за изследване е дадена на фиг. 1. Общата продължителност на изследването за всеки пациент ще бъде 8–12 седмици. Въз основа на предишния опит при набирането на кръводарители за наблюдателни изследвания, ние се стремим да включим двама участници в проучването седмично. По този начин общият период на набиране се очаква да продължи 21–24 месеца, а общата продължителност на активното проучване ще бъде 26 месеца. Набирането започна през юни 2014 г. и завърши през юни 2016 г. По време на ревизията бяха включени всички 176 участници (172 според изчислението на размера на извадката плюс 4 отпадащи).
Проучете диаграмата
Продължителност на обучението за отделния участник
Периодът на активно лечение за всеки участник е 8–12 седмици.
Прожекция
Обикновено след редовно даряване на афереза на цяла кръв или тромбоцити, феритинът се измерва от останалия серум за рутинно изследване на инфекциозни заболявания. Редовното писмено информирано съгласие за кръводаряване обхваща допълнителния анализ на феритина. След това донори със серумен феритин ≤30 ng/ml ще бъдат поканени по телефона да участват в проучването.
Посещение 0, включително процедура за рандомизация (4–6 седмици след даряването на кръв)
Донорите, желаещи да участват, се приканват да посетят отделението за афереза към Отделението по серология на кръвната група и трансфузионна медицина. След даване на писмено информирано съгласие, проверка на критерии за включване/изключване и извършване на тест за бременност в урината при жени в менопауза, донорът попълва формуляр за доклад за случая (CRF).
CRF включва въпроси относно следните аспекти:
История на кръводаряване (общ брой, време)
История на анемия
Симптоми на умора
Субективно физическо и когнитивно представяне, включително самоотчитане на физическа активност и отработени часове на седмица
Симптоми на депресия или летаргия
Трофични промени на ноктите или косата
Умора, предизвикана от кръводаряване
Симптоми на синдрома на неспокойните крака
Процедура за рандомизация
Всеки участник ще бъде рандомизиран в съотношение 1: 1 (стратифициран по пол) към високодозово парентерално вливано желязо или орални добавки с желязо, използвайки уеб-базиран инструмент за рандомизация (http://www.randomizer.at). Съответствието на този софтуер с добра клинична практика (GCP) е потвърдено от Австрийската агенция за здраве и безопасност на храните (AGES).
Кръвни проби
30 ml) се взимат от всички участници, в случай на рандомизиране на парентерално вливано желязо от венозен достъп, поставен за прилагане на интравенозно приложеното желязо. Някои параметри могат да бъдат измерени след края на изследването от проби от замразена кръв, съхранявани при -70 ° C.
Тестове за окултна кръв в изпражненията
За да се оцени окултно стомашно-чревно кървене, всички участници са помолени да направят три теста за окултна кръв в изпражненията у дома в периода между посещение 0 и посещение 1.
Лекарства
Според рандомизацията на участника се раздават или 100 таблетки орални добавки с желязо, или желязото се прилага интравенозно от изследователите в проучването в присъствието на медицинска сестра.
За перорални добавки с желязо всички участници получават точен график за прием на таблетки, заедно с ясни инструкции според листовката: предлагаме да приемате 10 таблетки седмично (3 дни 2 таблетки, 4 дни 1 таблетка) и да приемате таблетките с портокал сок.
Желязото се прилага интравенозно на участниците в легло в отделна стая на отделението за афереза на Университетската клиника по серология и трансфузионна медицина на кръвна група. Желязото се влива интравенозно в продължение на 30 минути или повече по специална периферна линия. Разработена е стандартна оперативна процедура, включваща екипа за реанимация на отделението по анестезиология и основно оборудване за спешни случаи е на разположение по всяко време.
Посещение 1 (8–12 седмици след посещение 0)
Избира се период на лечение от 8–12 седмици, тъй като прилагането на 8–13 дози от 100 mg желязо за една седмица е осъществимо и също така съответства на типичния интервал на даряване. Освен това серумните нива на феритин са фалшиво високи, когато се анализират ≤6 седмици след интравенозна инфузия на желязо.
CRF, включително оценка на съответствието, се попълва от донора и кръвна проба (
30 ml) се изтегля. Всички резултати се обобщават в писмен доклад за участниците в проучването и се изпращат по обикновена поща.
CRF при посещение 1 допълнително ще включва въпроси относно следните аспекти:
Информация за съответните нежелани събития, сериозни нежелани събития и нежелани лекарствени реакции
Съответствие с приема на орално лекарство за изследване (самоотчитане; участниците също са помолени да върнат всички останали лекарства)
Статистически аспекти
Обосновка на размера на извадката
Дискусия
Досега нито едно рандомизирано контролирано проучване не е сравнявало високи дози интравенозно желязо с орално добавяне на желязо при донори на кръв с дефицит на желязо. Интравенозното желязо може да бъде отличен вариант в тази обстановка. Ако нашето проучване може да установи, че интравенозното желязо е възможно при донори на кръв и съществените пречки като разходите и логистиката могат да бъдат преодолени, високи дози интравенозно инфузирано желязо, дадено непосредствено след даряване на пълна кръв или афереза чрез сегашния венозен достъп, може да бъде много ефективен начин за корекция и/или профилактика на ятрогенен дефицит на желязо. Такъв подход би могъл да предпази донорите на кръв от симптоми, свързани с дефицит на желязо, и да помогне за поддържането на напълнения с донори кръв.
Пробен статус по време на първоначалното подаване на ръкописа
Набирането за този процес продължава.
Благодарности
Оценяваме подкрепата на звеното за афереза под ръководството на С. Сипуржински и М. Степанек. Освен това благодарим на Т. Стоякович за научна подкрепа по отношение на лабораторни данни и на М. Шрок, К. Райнпрехт и М. Мориц за оперативна подкрепа. Благодарни сме за статистическата подкрепа на Катедрата по медицинска информатика, статистика и документация на Медицинския университет в Грац за изчисляване на размера на извадката.
Финансиране
Опитът се финансира от Медицинския университет в Грац и Vifor Pharma и е получил лекарството за устно проучване от GL Pharma.
Принос на авторите
KA, CD и NS са проектирали проучването; SM и PS допринесоха за дизайна на изследването и процедурата за скрининг; KA осигури финансиране за проекта; SM, CD и IL формират текущата група за управление на изпитванията със съвети от KA и PS; SM, CD и KA изготвят ръкописа. Всички автори коментираха изменените проекти и одобриха окончателния ръкопис.
Конкуриращи се интереси
Авторите заявяват, че нямат конкуриращи се интереси.
Етично одобрение и съгласие за участие
Проучването се извършва съгласно насоките на GCP и е в съответствие с Декларацията от Хелзинки. Изследването е одобрено от Австрийската агенция за здраве и безопасност на храните (AGES) и от Етичния комитет на Медицинския университет в Грац. Всички участници дават писмено информирано съгласие.
Съкращения
| ВЪЗРАСТИТЕ | Австрийска агенция за здраве и безопасност на храните |
| CRF | Формуляр за доклад на случая |
| GCP | Добра клинична практика |
| ICU | Интензивно отделение |
| IV | Интравенозно |
| PO | Перорално |
| β-HCG | Бета-човешки хорион гонадотропин |
Допълнителен файл
SPIRIT 2013 Контролен списък: Препоръчани елементи, които трябва да се разгледат в протокол за клинично изпитване и свързани документи * (DOCX 63 kb)
- Хранене за намаляване на високото кръвно налягане
- Запълване на вашето упражнение Топливост срещу твърдост - манекени
- Диетите, които подрязват коремните мазнини, подобряват притока на кръв - Бъдеще
- Ектоморф, Мезоморф и Ендоморф Типове на тялото - Диета; Тренировка - Iron Orr Fitness
- Ефект от бързото отслабване с добавка на гладно върху серумни електролити, липиди и кръв