Мусуми BOSE
1 Нюйоркски изследователски център за затлъстяване, Колумбийски колеж на лекари и хирурзи, Ню Йорк, Ню Йорк
Хулио ТЕЙКСЕЙРА
2 Отделение за бариатрична хирургия, Болничен център "Св. Лука"/Рузвелт, Колеж на лекари и хирурзи на Университета Колумбия, Ню Йорк, Ню Йорк
Бланка ОЛИВАН
1 Нюйоркски изследователски център за затлъстяване, Колумбийски колеж на лекари и хирурзи, Ню Йорк, Ню Йорк
Baani BAWA
1 Нюйоркски изследователски център за затлъстяване, Колумбийски колеж на лекари и хирурзи, Ню Йорк, Ню Йорк
Сара АРИАС
1 Нюйоркски изследователски център за затлъстяване, Колумбийски колеж на лекари и хирурзи, Ню Йорк, Ню Йорк
Sriram MACHINENI
1 Нюйоркски изследователски център за затлъстяване, Колумбийски колеж на лекари и хирурзи, Ню Йорк, Ню Йорк
F. Xavier PI-SUNYER
1 Нюйоркски изследователски център за затлъстяване, Колумбийски колеж на лекари и хирурзи, Ню Йорк, Ню Йорк
Филип Е. ШЕРЕР
3 Център за диабет Touchstone, отдели по вътрешни болести и клетъчна биология, Югозападен медицински център на Тексаския университет, Далас, Тексас, САЩ
Blandine LAFERRÈRE
1 Нюйоркски изследователски център за затлъстяване, Колумбийски колеж на лекари и хирурзи, Ню Йорк, Ню Йорк
Резюме
Заден план
Целта на настоящото проучване беше да се определят механизмите, залегнали в ремисия на диабет тип 2 след операция на стомашен байпас (GBP), като се характеризират краткосрочните и дългосрочните промени в хормоналните детерминанти на кръвната глюкоза.
Методи
Единадесет болестно затлъстели жени с диабет са проучени преди и 1, 6 и 12 месеца след GBP; за контрол са използвани осем жени с диабет с болестно затлъстяване. Енкретиновият ефект се измерва като разлика в нивата на инсулин в отговор на перорална глюкоза и на изогликемично интравенозно предизвикателство. Резултатните мерки бяха глюкоза, инсулин, С-пептид, проинсулин, амилин, глюкагон, глюкозозависим инсулинотропен полипептид (GIP), глюкагон-подобен пептид-1 (GLP-1) и инкретиновият ефект върху секрецията на инсулин.
Резултати
Намаляването на глюкозата на гладно (r = 0,724) и инсулина (r = 0,576) е свързано със загуба на тегло до 12 месеца след GBP. За разлика от това, притъпеният инкретинов ефект (изчислен на 22%), който се подобрява на 1 месец, остава непроменен с по-нататъшна загуба на тегло на 6 (52%) и 12 (52%) месеца. Притъпените нива на инкретин (GLP-1 и GIP), ранната фаза на секреция на инсулин и други параметри на функцията на β-клетките (амилин, проинсулин/инсулин) следват същия модел, с бързо подобрение след 1 месец, което остава непроменено на 1 година.
Заключения
Данните предполагат, че загубата на тегло и инкретините могат да допринесат независимо за подобряване на нивата на глюкозата през първата година след операция на GBP.
Въведение
Първата цел на настоящото проучване беше да се характеризира моделът на промени в хормоналните детерминанти на нивата на кръвната захар през първата година след хирургическа загуба на тегло от GBP при пациенти с диабет. Ние предположихме, че ранното (1 месец) повишаване на нивата на инкретин след перорална глюкоза и подобреният инкретинов ефект върху секрецията на инсулин ще останат непроменени до 1 година след GBP. Също така предположихме, че други маркери на метаболизма и функцията на β-клетките, като глюкоза, инсулин, амилин, проинсулин, глюкагон, лептин и адипонектин, ще се подобрят като функция на загуба на тегло.
Методи
Субекти
Единадесет жени със затлъстяване с диабет тип 2 (OBDM), известни за по-малко от 5 години (диапазон 1–52 месеца), HbA1c 6,7 ± 0,8%, индекс на телесна маса (ИТМ) 45,1 ± 7,8 kg/m 2 и на възраст 44,3 ± 11,1 години са изследвани преди и 1, 6 и 12 месеца след GBP. Пет жени са приемали сулфонилурейни продукти и/или метформин и са им държали лекарствата 3 дни преди изходните проучвания и са спирали след GBP. Като контроли бяха използвани затлъстели жени с нормален глюкозен толеранс (OBNGT; n = 8). Всички участници са предоставили информирано съгласие преди записване в проучването. По-рано са публикувани данни за 1 месец от осем пациенти с GBP. 2, 3
Roux-en-Y GBP
Всички OBDM са подложени на лапароскопски GBP. Иеюнумът беше разделен на 30 cm от лигамента на Treitz и анастомозиран до 30 ml проксимална стомашна торбичка. Иеюнумът беше повторно анастомозиран на 150 cm дистално от газовата троеюностомия. Препоръките за диета след GBP включват дневен прием от 600–800 kcal, 70 g протеин и 1,8 L течност през първите няколко седмици, последван от диета ad libitum с акцент върху приема на протеини, течности и витамини през следващата година . Това беше постигнато, индивидуално, с множество малки хранения и леки закуски с различни търговски протеинови добавки. Диетата след GBP се наблюдава от хранителни записи, но не е нито пряко контролирана, нито контролирана в рамките на няколко дни, предхождащи тестването.
Инкретинов ефект върху секрецията на инсулин
За да се изчисли инкретиновият ефект за всеки пациент, всички субекти са били подложени на орален тест за глюкозен толеранс (OGTT), последван от изогликемичен интравенозен (iv) глюкозен тест (IsoG IVGT). OGTT винаги се извършва първо, последвано от, в отделен ден, IsoG IVGT. Всеки тест се провежда сутрин след пост през нощта. По време на OGTT и IsoG IVGT, ръката, използвана за вземане на кръв, се поддържа топла с нагревателна подложка.
За OGTT, след i.v. вмъкване, в 08:00 ч. субектите получават 50 g глюкоза в 200 ml перорално. Кръвни проби бяха събрани в продължение на 3 часа в охладени епруветкови епруветки с апротинин (500 каликреинови инхибиторни единици/мл кръв; Roche Applied Sciences, Индианаполис, IN, САЩ) и инхибитор на дипептидил пептидаза (DPP) IV (50 μmol/L; Millipore, St Charles, MO, USA) и се центрофугира на 1620 ж за 15 минути при 4 ° C за отделяне на плазмата. Плазмените проби се съхраняват при -70 ° C до анализ.
За да се изчисли инкретиновият ефект за всеки пациент, i.v. предизвикателство за глюкоза се дава в отделен ден. Целта на IsoG IVGT беше да изложи панкреаса на нивата на кръвната захар, съответстващи на тези, получени по време на OGTT за същия пациент през същия период на изследване. Влива се глюкоза (стерилна 20% декстроза) i.v. над 3 часа с помощта на помпа (Gemini; CareFusion, Сан Диего, Калифорния, САЩ). Кръвни проби се събират на всеки 5 минути, като се използва контралатерален антекубитален i.v. катетър за незабавно измерване на нивата на глюкоза в леглото. Скоростта на вливане на глюкоза се коригира, за да съответства на концентрациите на глюкоза, получени за същия пациент по време на OGTT във всеки момент от време в продължение на 3 часа.
Разликата в отговорите на β-клетките [обща площ на инсулина под кривата (INS AUC0–180)] към оралния и изогликемичния i.v. глюкозните стимули представляват действието на инкретиновия ефект, изразено като процент от отговора на пероралната глюкоза, който се приема като знаменател (100%). 4 Използваната формула беше:
където INC е инкретиновият ефект, а INS AUC е инсулиновата зона под кривата след перорално или изогликемично i.v. глюкоза, както е посочено.
Анализи
Общият GLP-1 се измерва чрез радиоимуноанализ (RIA; Millipore) след екстракция с етанол в плазмата. Коефициентите на вариация (CV) в рамките на интра- и интераси са съответно 3–6,5% и 4,7–8,8%. Този анализ реагира на 100% с GLP-17–36, GLP-19–36 и GLP-17–37, но не и с глюкагон (0,2%), GLP-2 (ISI = 10000 (глюкоза на гладно × инсулин на гладно × средна глюкоза × среден инсулин по време на OGTT) .
Данните са представени като средната стойност ± SD.
Стойностите са средната стойност ± SD.
Нива и ефекти на инкретина
Нивата на инкретин на гладно не се променят след GBP (данните не са показани). Увеличението на пиковите GLP-1 и GIP отговори на пероралната глюкоза, съответно с фактори 10 и 1,4, показани преди това на 1 месец, 2, не се променят допълнително на 6 и 12 месеца (Таблица 2; Фиг. 2). Нивата на глюкоза бяха съпоставени и не се различаваха значително между OGTT и isoG IVGT през всеки период на изследване (данните не са показани). Ранното увеличение на инкретиновия ефект върху секрецията на инсулин (от 22,1% на 46,9%) до нивото, наблюдавано в контролния OBNGT (43%), продължава и на 6 и 12 месеца (Таблица 2; Фиг. 2).
Относително въздействие на загуба на тегло и инкретини
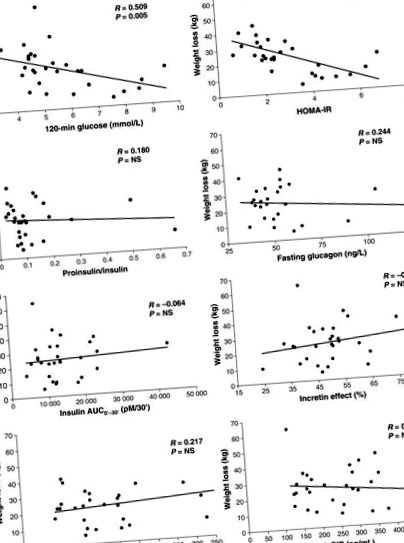
Налице е положителна корелация между телесното тегло и глюкозата на гладно, инсулин, проинсулин, амилин, глюкагон и лептин и отрицателна корелация между телесното тегло и адипонектина. Само промени в глюкозата на гладно (r = 0,724; P Фиг. 3). Глюкозата след хранене (120 минути) е в отрицателна корелация с ранната фаза на секреция на инсулин (r = -0,407; P = 0,023), пик на GLP-1 (r = -0,562; P 2 = 0,235; P = 0,024). Пиковите GLP-1 и инкретиновите ефекти са свързани с ранната фаза, но не и с късната фаза, секреция на инсулин. Само глюкоза на гладно след GBP, а не глюкоза на 120 минути, прогнозира HbA1c на 12 месеца (R 2 = 0,323; P = 0,022).
Корелации между загуба на тегло и глюкоза на гладно, инсулин на гладно, проинсулин на гладно и глюкагон на гладно на 1, 6 и 12 месеца след стомашен байпас (GBP). Няма връзка между загубата на тегло и ранната фаза на секреция на инсулин (INSAUC0–30 ′), инкретиновия ефект, пиковия глюкагоноподобен пептид-1 (GLP-1) и пиковия глюкозозависим инсулинотропен полипептид (GIP) при 1, 6 и 12 месеца след GBP. HOMA-IR, модел на хомеостаза оценка на инсулинова резистентност.
Дискусия
С повишения инкретинов ефект, нашите данни показват промяна в модела на секреция на инсулин (и С-пептид), с повишена ранна фаза и намалена късна фаза, в отговор на пероралната глюкоза. Това е в съгласие с възстановяването на ранната фаза на секреция на инсулин след инфузия на GLP-1 11 или след i.v. глюкоза. 12 Въпреки че настоящото проучване е малко и ограничено до 1 година, по-големи и по-дълги проучвания показват, че ремисията на диабета продължава години след байпас операция. 1, 13 Възможно е да се предположи, че по-високите нива на инкретин след GBP могат да защитят функцията на островните клетки и/или β-клетъчната маса. 14.
Нашите данни предполагат, че повишаването на нивата на инкретин и ефекта след GBP, което е придружено от възстановяване на ранната фаза на секреция на инсулин, може да допринесе за подобряване на PPG. В нашето предишно проучване, краткосрочно съответстващо на диетата отслабване, за разлика от GBP, не възстановява ранната фаза на секреция на инсулин или намалява 120 ′ глюкоза при хора с диабет. 3 В допълнение, диетата не повишава нивата или ефектите на инкретина. 3 Неотдавнашно проучване при плъхове Goto-Kakizaki показа, че повишената секреция на GLP-1 и подобрената толерантност към глюкозата след дуоденален йеюнален байпас се обръща от антагонизма на GLP-1 рецептора, предоставяйки пряко доказателство, че подобряването на толерантността към глюкозата след операция за байпас се медиира от засилено GLP-1 действие. 15 Нашите данни показват благоприятен ефект на GBP чрез промени в инкретините и ранната фаза на секреция на инсулин за контрол на PPG. Това би могло да има значително клинично значение, тъй като повишеният PPG е маркер за сърдечно-съдов риск. 16 Според нашата хипотеза, промяната в нивата и ефекта на инкретина, както и в ранната фаза на секреция на инсулин след GBP са независими от загубата на тегло и вероятно са последица от процедурата за хирургичен байпас, както се предполага от проучвания върху животни. 17
В допълнение към медиирания от инкретина ефект върху подобрената секреция на инсулин и хомеостазата на глюкозата, GBP упражнява своя метаболитен ефект до голяма степен чрез значителната и продължителна загуба на тегло. Нашите данни също така показват, че за разлика от промените в инкретина, нивата на глюкоза на гладно, проинсулин, С-пептид и инсулин се подобряват в зависимост от загубата на тегло през първата година след операцията.
Повишените нива на проинсулин, наблюдавани преди операцията, намаляват значително, отразявайки намаленото търсене на β-клетките и подобрената функция на островчетата, както е показано по-рано при лица без диабет. 18 Нивата на амилин на гладно и отговорът към пероралната глюкоза се подобряват на 1 месец и не се променят с по-нататъшна загуба на тегло. Схемата на нивата на инсулин, про-инсулин и амилин, три β-клетъчни пептиди, в отговор на орално стимулиране на глюкозата се променя по подобен начин след GBP, с повишена ранна фаза и намалена секреция в късна фаза (Фиг. 1). Промените настъпват бързо на 1 месец и след това нивата остават непроменени до 1 година. Амилин, съвместно секретиран с инсулин, не само отразява функцията на β-клетките, но може също да окаже влияние върху секрецията на инсулин и метаболизма на PPG.
Малко са проучванията, съобщаващи за промени в инсулиновата резистентност след байпасна операция. Нашите данни показват, че инсулиновата резистентност, изчислена от HOMA-IR, намалява на 1 година, когато скоростта на загуба на тегло е минимална, подобно на други проучвания с помощта на скоби. 19 В допълнение към загубата на тегло, фактори като промени в транспортерите на глюкоза, 20 инкретина или адипокини, 18, 21 и повишена чревна глюконеогенеза, както е показано в модел на гризачи, 22 могат да обяснят подобрена дългосрочна чувствителност към инсулин. В настоящото проучване повишаването на нивата на адипонектин е значително само между 6 и 12 месеца след операцията. Има няколко случая, при които общите нива на адипонектин не се променят, но разпределението на различните адипонектинови комплекси се променя. Ще бъде интересно да се види дали различните комплекси реагират диференцирано на GBP. Измерването на различните комплекси има тенденция да дава по-точна индикация за общите метаболитни подобрения в отговор на интервенция. 23.
Хиперглюкагонемията на диабета намалява с индуцирана загуба на тегло. 24 Любопитното е, че нашите данни показват, че нивата на глюкагон на гладно не са се променили 1 месец след GBP. Освен това нивата на глюкагон се повишават повече в отговор на пероралната глюкоза 1 месец след GBP. Механизмът на тази парадоксална хиперглюкагонемия 1 месец след GBP е неясен и изглежда независим от GLP-1, GIP и/или загуба на тегло. Това може да бъде свързано с остри невронални промени след GBP. На 6 и 12 месеца, въпреки че нивата на глюкагон на гладно намаляват с по-нататъшна загуба на тегло, нивата на глюкагон все още не се потискат от перорална глюкоза.
В обобщение, нашите данни предполагат относителна роля на промените в инкретина и загубата на тегло върху функцията на островните клетки и контрола на глюкозата. Нашите данни показват, че ефектът на загуба на тегло изглежда преобладаващ при нивата на глюкоза и инсулин на гладно, докато хирургичният ефект е преобладаващ при промени в инкретина. Освен това показахме, че инкретиновият ефект, независимо от загубата на тегло, може да обясни изместването на секрецията на инсулин към ранната фаза и по-ниските нива на глюкоза след 120 минути. Разбирането на механизмите на бърза и продължителна ремисия на диабета след GBP може да доведе до разработването на нови терапевтични подходи и по-нови, по-малко инвазивни хирургични техники за лечение на хора с диабет.
Благодарности
Тази работа е финансирана от безвъзмездни средства от Американската асоциация по диабет (7-05 CR-18), Националните здравни институти (R01-DK67561, 1 UL1 RR024156-03, ORC DK-26687 и DERC DK-63068-05), Програма за проучвания, инициирани от Merck Investigator, и Програма за инициирани от Amylin Investigator. Авторите благодарят на участниците доброволци и Yim DAM и Ping ZHOU (Нюйоркска лаборатория за изследване на затлъстяването, лаборатория за хормонални ядра) за техническата им помощ при хормоналните анализи.
- Ролята на жлъчката след стомашния байпас на Roux-en-Y за насърчаване на отслабването и подобряване на гликемичния
- Хирургия за отслабване - бандажен бандажен ръкав
- Ползи от чай от куркума Рецепта за напитки за отслабване, която може да помогне за предотвратяване на рак, контрол на диабета
- Защо използването на берберин за отслабване може да помогне на пациентите да подобрят цялостното здраве - алтернатива
- Две нови проучвания показват, че операцията за отслабване може да подобри проблемите с пикочните пътища