Резюме
Ниският прием на калий, често срещан в западните диети, повишава кръвното налягане и повишава чувствителността към солта. Повечето хора в „западните” страни също консумират излишна сол. При проучвания с мишки установихме, че диетата с високо съдържание на сол и ниско съдържание на калий активира чувствителния към тиазиди Na-Cl котранспортер в бъбреците. Този ефект води до задържане на натрий и повишено кръвно налягане и зависи от плазмения калий. Ние предположихме, че този ефект е медииран от промени във вътреклетъчния хлорид, причинени от промени в мембранното напрежение. Разработихме модел в култивирани клетки, който ни позволява да потвърдим тази хипотеза. След това потвърдихме, използвайки екзозоми на урината, че промените в диетата при нормалните хора влияят на чувствителния към тиазиди Na-Cl котранспортер по същия начин. Тези данни показват, че недостигът на калий в храната повишава кръвното налягане до голяма степен чрез стимулиране на реабсорбцията на солта по дисталния нефрон. Те предполагат, че глобалните усилия трябва да се съсредоточат върху увеличаването на приема на калий, което ще смекчи ефекта от диетите с високо съдържание на сол.
ВЪВЕДЕНИЕ
По-голямата част от хората в света днес консумират диета с относително високо съдържание на сол (NaCl) и ниско съдържание на калий (K +) (1). Подобна диета е свързана с хипертония, сърдечно-съдови заболявания и смъртност от всички причини. Ние се фокусирахме върху дисталната извита тубула (DCT) и чувствителния към тиазиди NaCl котранспортер, тъй като наскоро беше показано, че този сегмент на нефрона модулира екскрецията на калий. DCT при повечето видове бозайници е хетерогенен сегмент, включващ проксимална част, DCT1, която основно абсорбира NaCl, и дистална част, DCT2, където електронеутралният транспорт на NaCl съществува едновременно с електрогенни Na + и K + транспортни пътища (2–5 ).
Чувствителният към тиазиди NaCl котранспортер (NCC, генен символ SLC12A3) е преобладаващият апикален път за навлизане на Na + в клетки DCT1, клетки, в които не се осъществява електрогенен транспорт. Тъй като DCT клетките също контролират доставката на NaCl в свързващата тубула, където епителният натриев канал (ENaC) медиира електрогенна Na + реабсорбция и където K + се секретира (6), изглежда, че те имат съществена, макар и индиректна роля в K + секреция. Значението на DCT в секрецията на K + стана очевидно, когато молекулярният разтвор на FHHt доведе до откриването на молекулярен превключвател, включващ кинази „без лизин“ (WNK), свързана с Ste20p пролин аланин киназа (SPAK) и окислителна реакция на стрес 1 киназа (OxSR1). Мутациите на болестта, причиняващи FHHt, изглежда заключват този превключвател в положение „включено“, задвижвайки неумолима NCC активност, което води до хиперкалиемия и хипертония. Въпреки че тази патогенеза е ясна, естеството на физиологичния активатор на превключвателя остава неуловим.
NCC се активира физиологично, когато приемът на NaCl с храната е намален. И все пак NCC реагира и на промените в приема на K + с храната. Високият прием на KCl потиска (7-10), а ниският прием на KCl увеличава NCC активността (9,11,12). Тези ефекти допринасят за системната K + хомеостаза, като променят доставката на Na + до K + секреторните сегменти (9,13). Поради това се опитахме да идентифицираме факторите, модулиращи функцията DCT и активността на NCC.
МАТЕРИАЛИ И МЕТОДИ
Животни
Всички проучвания върху животни са одобрени от Комитета по грижа и употреба на животните в Университета по здравеопазване и наука в Орегон (протокол IS918). Всички мишки са били на възраст от 12 до 24 седмици, от 25 до 30 g и са имали C57Bl/6 фон, с изключение на NCC -/- мишки, които са били на фон BALB/c.
Измерване на кръвното налягане
Неинвазивното систолично кръвно налягане се измерва с маншети с помощта на обемно регистриране на налягането (CODA-16; Kent Scientific, Torrington, CT, USA). Мишките бяха аклиматизирани към машината в продължение на 5 последователни дни преди запис. В проучванията за диетични манипулации мишките са поддържани на изходната диета (висок NaCl [6%]/нормален K + [1%]) (Harlan Laboratories, Indianapolis, IN, USA, K + -дефицитна диета [TD.88239] допълнена с NaCl и KCl) за 1 седмица преди да бъдат получени измервания. След регистриране на кръвното налягане в продължение на 4 дни на изходната диета, диетите бяха променени на високо NaCl/ниско К + (0%). Животните бяха оставени да се приспособят към новата диета за поне 4 дни и данните бяха записани след този период.
Анализ на кръвта
Пълна кръв се събира чрез сърдечна пункция, под анестезия. Електролитите бяха измерени чрез iSTAT (Abbott Point of Care, Inc., Princeton, NJ, USA).
Имуноблотинг
Мишките бяха поддържани на посочени диети в продължение на 7 до 10 дни или третирани с амилорид (50 mg/L питейна вода) в продължение на 5 до 7 дни, след което бъбреците бяха събрани и замразени бързо в течен азот. След това бъбреците се хомогенизират върху лед в охладен буфер, съдържащ протеаза и фосфатазни инхибитори. Протеин (20 до 80 μg) се разделя на 4-12% (тегл./Об.) Bis-Tris гел (Invitrogen, Grand Island, NY, USA).
Клетъчна култура
Flp-In NCC клетки са генерирани, както е съобщено по-рано (14). Клетките HEK293T (American Type Culture Collection) бяха отгледани в модифицираната среда на Dulbecco Eagle (Invitrogen), допълнена с 10% фетален говежди серум (Invitrogen) в 5% CO2 и 95% въздух при 37 ° C. Клетките бяха отгледани до 50% до 70% сливане за трансфекция и съответните cDNAs бяха приложени едновременно върху клетките, използвайки TurboFect трансфекционен реагент (Fermentas, Grand Junction, NY, USA). За измерване на потенциала за обръщане на K + е използван усилвател Achon 200A за кръпка, както се съобщава (15).
Човешки изследвания
Всички проучвания върху хора са одобрени от Съвета за вътрешен преглед на Университета за здраве и наука в Орегон (протокол IRB9934). Здравите човешки доброволци бяха помолени да консумират две различни диети, диета с високо съдържание на сол/ниско съдържание на K + и диета с високо съдържание на сол/K +, всяка за период от 4 дни. Доброволците бяха рандомизирани по реда, в който консумираха двете диети. Сутринта на 5-ия ден от всяка диета се събира урина и се върти в ултрацентрифуга съгласно предварително публикуван протокол (16).
РЕЗУЛТАТИ
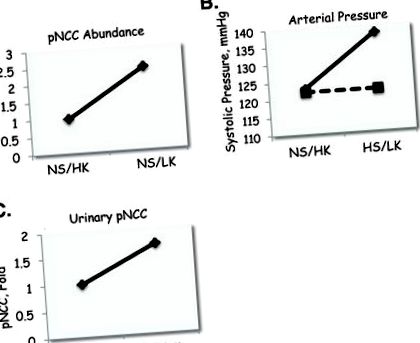
При мишки открихме, че NCC и фосфорилираният NCC (pNCC, като индекс на активиране) са по-разпространени в бъбреците на мишки, консумиращи диета с високо съдържание на сол/ниско съдържание на K + (HS/LK), отколкото диета с високо съдържание на сол/нормално K + (HS/NK) диета (фиг. 1 А). След това показахме, че средното артериално налягане, измерено телеметрично, се увеличава, когато мишките са преминали от HS/NK към HS/LK диета (Фиг. 1 B). Повишаването на артериалното налягане върху LK диетата е предимно през активния период, в съответствие с предишни доклади (11). За да определим дали активирането на NCC по време на LK диета допринася за повишаването на кръвното налягане, сравнихме ефектите от диетата при мишки Slc12a3 -/-, при които NCC беше генетично изтрита, и отпадъци. Имайте предвид, че мишките Slc12a3 -/- имат нормално кръвно налягане на изходно ниво, както беше съобщено по-рано (17). При мишките Slc12a3 -/- кръвното налягане не се повишава по време на LK диета, докато при кошерите (фиг. 1 Б). Влиянието на генотипа върху отговора на LK диета е значително.
Ефекти от диетичния прием на калий върху изобилието на NCC. (А) Ефекти на диетата с високо съдържание на сол/високо калий (HS/HK) спрямо диета с високо съдържание на сол/ниско калий (HS/LK) върху изобилието на фосфорилиран NCC (pNCC), измерено в произволни единици. (Б) Ефекти от същите диети върху артериалното налягане при мишки от див тип (плътна линия) и NCC -/- мишки (пунктирана линия). (° С) Ефект на подобни диети върху pNCC в урина на човешки доброволци.
За да определим дали хората проявяват подобен отговор на приема на K + с храната, ние анализирахме pNCC в екзозомите на урината (18,19) от доброволци, които консумираха HS/LK диета в продължение на 4 дни и след това HS/NK диета в продължение на 4 дни. Изобилието на pNCC е значително по-голямо след диетата HS/LK, отколкото след диетата HS/NK (фиг. 1 С). Диетите имаха сходно съдържание на Na + и калории, докато K + в диетата се различаваше.
Плазменият калий е значително по-нисък при мишки, консумиращи LK, в сравнение с NK диета (2,37 ± 0,13 срещу 3,38 ± 0,04). И все пак някои предполагат, че K + трябва да се приема през устата, за да се промени NCC (8). За да тестваме ролята на плазмата [K +], без да променяме приема на K +, манипулирахме плазмата [K +] фармакологично с K + -съхраняващия диуретик амилорид. Амилорид директно инхибира ENaC, което води до задържане на K +, но не засяга директно NCC (20). Лечението с мишки с амилорид причинява значителна хиперкалиемия и (фиг. 2 А) и, както се предполага от по-висок хематокрит, (фиг. 2 Б), изчерпване на обема на извънклетъчната течност (ECF). Въпреки изчерпването на обема, което се очаква да стимулира NCC, амилоридът намалява както NCC, така и pNCC, което предполага, че K + сигналът заменя ECF сигнала (фиг. 2 С). Тъй като амилоридът може да има ефекти, несвързани с промените в плазмата [K +], ние лекувахме мишки с LK диета заедно с амилорид, за да поддържаме [K +] в нормалните граници. Това предотвратява хиперкалиемия (фиг. 2 А), промени в хематокрита (фиг. 2 Б) и промени в NCC и pNCC (фиг. 2 В). Заедно тези резултати предполагат, че приемът на K + с храната влияе върху NCC чрез ефекти върху плазмата или върху общото тяло K + .
Ефекти на плазмения калий върху изобилието на NCC. (А) Плазмена концентрация на калий при мишки, лекувани с носител (VEH), амилорид (AML) или амилорид плюс нискокалиева диета (AML + LK). (Б) Стойности на хематокрит при същите мишки. (° С) Изобилие на pNCC в бъбреците на същите мишки.
След това тествахме дали NCC се модулира директно от извънклетъчни [K +], като използваме култивирани Flp-In NCC клетки (14). Клетките, култивирани в LK среда, имат по-голямо изобилие на pNCC, отколкото клетките, култивирани в NK (фиг. 3 А). Тъй като се очаква LK среда да хиперполяризира клетките (21), ние определихме ефектите от промяната на мембранния потенциал върху pNCC. Открихме тясна връзка между мембранното напрежение и изобилието на pNCC (Фиг. 3 Б). След това показахме, че ефектите на K + върху pNCC могат да бъдат блокирани от лекарството, блокиращо хлоридните канали 4,4′-диизотиоциано-2,2′-стилбенедисулфонова киселина (DIDS) (фиг. 3 С).
Ефекти на калиевото и мембранното напрежение върху pNCC в култивирани клетки. (А) Ефект на ниска K + среда върху изобилието на pNCC в култивирани човешки ембрионални бъбречни клетки 293. (Б) Регресия на изобилието на pNCC спрямо мембранното напрежение в HEK клетките. (° С) Ефект на блокиране на хлоридните канали с DIDS върху ефектите на ниска K + среда в HEK клетки.
ДИСКУСИЯ
Тези резултати показват доминиращата роля, която плазмата [K +] играе в регулирането на NCC, и показват, че извънклетъчната [K +] влияе непряко на NCC чрез модулиране на вътреклетъчната [Cl -]. Тъй като DCT се намира нагоре от важните K + секреторни нефронови сегменти, NCC активността ще има важни ефекти върху екскрецията на K +. Резултатите показват, че ползите за здравето от хранителните добавки K + са силно зависими от NCC.
Настоящите резултати потвърждават, че приемът на K + с диета модулира изобилието на pNCC и показват, че приемът на K + с храната е по-мощен в това отношение от обема на ECF. Тези ефекти върху NCC водят до промени в кръвното налягане, които изискват модулация на NCC активността. Те са медиирани до голяма степен от промени в плазмата [K +], тъй като ефектите се възпроизвеждат, когато плазмата [K +] се променя с помощта на лекарства или диета, заключение, съвместимо с експерименти с инфузия на K + наскоро (7).
Резултатите показват, че извънклетъчният [K +], независимо от хормоналните ефекти, директно модулира оста WNK-SPAK/OxSR1-NCC. Нашият клетъчен модел предполага, че са включени промени в мембранното напрежение, тъй като маневри, които променят мембранното напрежение, водят до промени в изобилието на pNCC в съответствие с зависимостта от напрежението. Доказателствата също така показват, че ефектите на калия се медиират от промени в концентрацията на вътреклетъчен хлорид.
Широко прието е, че диетата с ниско съдържание на NaCl стимулира дейността на NCC, допринасяйки за физиологично полезно задържане на NaCl, чрез действието на хормони, включително ангиотензин II и алдостерон (22,23). Настоящата работа добавя към все по-голям брой доказателства, показващи, че NCC се активира и от LK диета и че ефектите от LK диета върху активността на NCC се появяват и се засилват от приема на HS. Въпреки че това заключение изглежда неинтуитивно, то потвърждава скорошни резултати от друга група (11). Освен това, това вероятно отчита наблюдението, че диетичният K + има по-голям ефект за понижаване на налягането при хората по време на висок в сравнение с нисък прием на NaCl (24). Тъй като ефектите от диетата HS/LK върху артериалното налягане отсъстват, когато NCC е генетично изтрит (фиг. 2 В), NCC играе съществена и ненужна роля в антихипертензивните ефекти на диетичния K +. Тъй като документирахме, че лишаването от K + при хранене при хората също стимулира NCC, резултатите са от значение за човешкото здраве, където се смята, че диетата HS/LK допринася за глобалната епидемия от хипертония (1,25,26).
Резултатите показват, че DCT действа като бъбречен K + сензор, работещ съвместно с надбъбречната жлеза, за да запази K + хомеостазата. В това отношение DCT клетките и надбъбречните клетки на зона гломерулоза и двете усещат един и същ сигнал, мембранно напрежение, но реагират в противоположни посоки. Увеличаването на плазмата [K +] стимулира производството и освобождаването на алдостерон от надбъбречната жлеза, докато увеличаването на плазмата [K +] инхибира NCC. За да се получи калиуреза, събитията в надбъбречната жлеза и DCT трябва да се случат pari passu. Това се гарантира чрез наличието на един и същ сигнал, извънклетъчен [K +], регулиращ и двата клетъчни типа. Тъй като надбъбречните клетки реагират на ECF обемния сигнал ангиотензин II, DCT клетките вероятно също реагират. В този случай обаче сигналите в двата органа са съгласувани.
ПРИЗНАВАНИЯ
Тази работа беше финансирана отчасти от безвъзмездни средства от NIH (DK51496 за DHE и DK54983 за WHW) и от Министерството на ветераните (1I0BX002228–01A1 за DHE). AST е получил награда за докторска стипендия на Американската асоциация по сърдечни заболявания (3PRE14090030). Тази работа е извършена от AST в частично изпълнение за докторска степен по клетъчна и биологична биология от Орегонския университет за здраве и наука.
Бележки под линия
Потенциален конфликт на интереси: Няма разкрити.
ДИСКУСИЯ
Вълк, Бостън: Какъв е ефектът от ниския и високия магнезий върху вашите клетки, защото магнезият засяга почти всички транспортни канали, които сте демонстрирали?
Елисън, Портланд: Не знам от голяма гледна точка. Ако перфузирате DCT сегменти или дестилирате нефронови сегменти с ниско съдържание на магнезий във ваната, клетките хиперполяризират. Така че може да получите ефекти. И със сигурност хипомагнезиемията може да затрудни коригирането на хипокалиемията и може да допринесе и за това. Така че трябва да помисля за това.
Вълк, Бостън: Има някои епидемиологични доказателства, че диетите с високо съдържание на магнезий са свързани с ниско или високо кръвно налягане и по-нисък сърдечно-съдов риск.
Елисън, Портланд: Това е чудесен въпрос, за който трябва да прекарам известно време в мислене.
Зейдел, Бостън: Само за да изясня, имате клетка в дисталния извит тубул, която има електронеутрален вход на натриев хлорид и оказва влияние върху калия. Мисълта е, че има намалена доставка; ако абсорбира повече сол, по-малко натрий попада в събирателния канал. Поради това намалява отделянето на калий. Измервали ли сте нива на хлорид в дисталните извити тубални клетки? Започнали ли сте да правите такива измервания?
Елисън, Портланд: Не сме го измервали в DCT клетки in vivo; ние се надяваме да направим това. Измерили сме го в нашия клетъчен модел и те са ясно засегнати от начина, по който предвиждаме. И ние също показахме, че тези ниски концентрации на хлорид в клетките са необходими за активиране на NCC. Работим за преместването му в по-физиологичен модел, но както знаете, това не е толкова лесно.
Зейдел, Бостън: Когато намалите нивото на калий отвън и хиперполяризирате клетката, тази хиперполяризация продължава ли в хронично състояние, за разлика от това, което правите в културата, където рязко понижавате калия? Бих си помислил, че клетката ще се адаптира, но може би греша.
Елисън, Портланд: Винаги го мислим като калий, определящ потенциала за покой на клетките, което ме кара да мисля, че е по-хроничен. Със сигурност в зона гломерулоза се смята, че това е основният механизъм за регулиране на калия на секрецията на алдостерон. Мисля, че се предполага, че той остава стабилен, но не знам данни, които да го подкрепят.
Шустер, Ню Йорк: Има ли активиращи мутации в дисталния свит тубулен К-канал, които биха имитирали този ефект?
Елисън, Портланд: Мутациите, които влагаме в клетките, са мутации, които причиняват епилепсия, атаксия, сензорно-неврална глухота и тубулопатичен синдром (наречен EAST или гърчове, сензорна глухота, атаксия, умствена изостаналост и електролитен дисбаланс, наречен SeSAME синдром), който е сензорна невроепилепсия. Но те изглеждат като синдром на Gitelman. Тези мутации имат ефект, който прилича на синдрома на Gitelman. Те деполяризират клетките и следователно изключват pNCC. Те не активират мутации в онези канали, за които съм наясно.
Бланц, Сан Диего: Познаваме много хора, които въпреки високия прием на натрий/нисък калий не стават хипертоници. Имате ли някакви епидемиологични проучвания при гризачи, които ви дават пример за това защо някои не реагират на тази диетична формула?
Елисън, Портланд: Мисля, че това е в съответствие с модела, постулиран от Рик Клифтън, където той показва, че хетерозиготни състояния на носители за NCC или NKCC2 изглежда предотвратяват развитието на или намаляват риска от развитие на хипертония през целия живот. Това потенциално биха били хора, които биха могли да изядат един тон сол и никога да не получат хипертония.
Бланц, Сан Диего: Имате ли ген, който вашите епидемиологични или резултати колеги биха могли да открият, който би ви насочил към избягване на техните диетични неразположение?
Елисън, Портланд: Имаме безвъзмездна помощ, която представихме заедно с Хауърд Прат от Университета в Индиана, за да се опитаме да разгледаме някои от тези неща, но не знам, че все още е направено.
Люк, Синсинати: Има доказателства, че при диета с ниско съдържание на сол калият има много по-малък ефект върху кръвното налягане, отколкото при диета с високо съдържание на сол. Когато използвате диета с ниско съдържание на сол, натоварването с калий не оказва толкова голям ефект върху кръвното налягане, което продължава да подчертава значението на солта по отношение на извънклетъчния обем. Така че това, върху което трябва да се съсредоточим, е диета с високо съдържание на калий/ниско съдържание на сол. Съгласни ли сте с това?
Елисън, Портланд: Да.
Люк, Синсинати: И не знаем колко ниска трябва да е солта. Искам да кажа, че това е съвсем ясно. Американското сърце може да е прекалило с 1,5 грама. Но не мисля, че трябва да забравяме историята и може би трябва да наблегнем малко повече на калия и диетата DASH прави това. Натоварването с натриев хлорид е много различно от натоварването с натриев бикарбонат, което отново мисля, че подкрепя хипотезата.
Елисън, Портланд: Да. Благодаря ви за тези коментари.
- Прегледът на диетите за кръвна група Яжте правилно за вашия тип Townsend Писмо за лекари
- Varanasis Chhappan Bhog тиква намалява кръвното налягане и затлъстяването - Опитах все пак NDTV Храна
- Кръвната група диети Десет енергийно стимулиращи суперхрани, подходящи за вашия тип
- Какво; s правилната диета за високо кръвно налягане DR
- Свалете хипертонията Как да намалите високото кръвно налягане