Алисън Л. Шрайбер
1 Катедра по физиология, 1901 Perdido Street, Център за здравни науки на Луизиана, Ню Орлиънс, Ню Орлиънс, LA САЩ 70112
Кенет П. Арцено, III
3 Pennington Biomedical Research Center, 6400 Perkins Road, Baton Rouge, LA USA 70808
Рафаел А. Малбру
3 Биомедицински изследователски център Pennington, 6400 Perkins Road, Baton Rouge, LA USA 70808
Алън Дж. Мутон
1 Катедра по физиология, 1901 Perdido Street, Център за здравни науки на Луизиана, Ню Орлиънс, Ню Орлиънс, LA САЩ 70112
Кристина С. Чен
2 съвместна програма за диабет, ендокринология и метаболизъм, 6400 Perkins Road, Baton Rouge, LA USA 70808
Елиас М. Пейка
2 съвместна програма за диабет, ендокринология и метаболизъм, 6400 Perkins Road, Baton Rouge, LA USA 70808
Х. Дъглас Бреймер
3 Pennington Biomedical Research Center, 6400 Perkins Road, Baton Rouge, LA USA 70808
Стефани Д. Примо
1 Катедра по физиология, 1901 Perdido Street, Център за здравни науки на Луизиана, Ню Орлиънс, Ню Орлиънс, LA САЩ 70112
2 съвместна програма за диабет, ендокринология и метаболизъм, 6400 Perkins Road, Baton Rouge, LA USA 70808
3 Pennington Biomedical Research Center, 6400 Perkins Road, Baton Rouge, LA USA 70808
Резюме
Въведение
Диетичните мазнини са от решаващо значение за цялостното здраве, развитие и репродуктивна функция. Въпреки това хората с наднормено тегло/затлъстяване могат да получат множество физиологични и психологически съпътстващи заболявания (Friedman and Kim, 1985; Linne, 2004; Nelson and Fleming, 2007; Norman and Clark, 1998; Wade and Jones, 2004). Въпреки че много от тези съпътстващи заболявания са преобладаващи както при мъжете, така и при жените, затлъстяването при жените е свързано с по-висок процент на безплодие, диабет тип II, сърдечно-съдови заболявания, депресия и някои форми на рак (Guh et al., 2009; Hackethal et al ., 2014; Yao et al., 2014). За разлика от мъжете си, процентът на затлъстяване при жените продължава да се увеличава през целия живот, като приблизително 42% от жените след менопаузата се считат за затлъстели (NHANES). Поради драстичното увеличаване на продължителността на живота, жените ще прекарат втората половина от живота си в дефицит на естроген, което ги предразполага към развитие на висцерално затлъстяване, метаболитен синдром, инсулинова резистентност и диабет тип II (Carr, 2003; Ley et al., 1992; Louet et al., 2004; Mauvais-Jarvis, 2012; Mauvais-Jarvis et al., 2013; Panotopoulos et al., 1996; Phillips et al., 2008; Rosety-Rodriguez et al., 2013).
Многобройни изследвания са изследвали ролята на ендогенните естрогени върху енергийната хомеостаза. Данните от модели на гризачи показват, че женските консумират повече калории по време на диеструс, отколкото проеструс или еструс, като плъховете в еструса консумират най-малко калории (Asarian and Geary, 2006, 2013; Wade, 1972). Отбелязаното намаляване на ендогенния естроген и прогестерон чрез овариектомия (OVX) предизвиква хиперфагия и бързо увеличаване на теглото и затлъстяването и увеличаване на размера на храненето, серумната глюкоза, холестерола, триглицеридите и свободните мастни киселини (Eckel, 1999; Eckel и Geary, 1999; Eckel et al., 2000; Eckel and Moore, 2004; Majumdar et al., 2014; McElroy and Wade, 1987; Messina et al., 2006; Santollo and Eckel, 2008a; Schneider et al., 1986; Wade, 1975; Wade и Schneider, 1992). Проучванията, изследващи ефектите от естроевия цикъл, OVX и лечението с естрадиол бензоат (EB) върху хранителните ефекти на различни пептиди и лекарства, илюстрират сложната роля, която естрадиолът (E2) играе върху енергийната хомеостаза (Brown and Clegg, 2010; Eckel, 1999; Eckel et al., 2002; Eckel et al., 2005; Messina et al., 2006; Rivera and Eckel, 2005; Rivera et al., 2009; Santollo and Eckel, 2008a, b). Освен това, проучванията съобщават за ефектите на естроевия цикъл и лечението с Е2 върху експресията на хипоталамусните пептиди, участващи в поведението на хранене (Gao et al., 1997; Khorram et al., 1985; Le et al., 1991; Leibowitz et al., 1998; Olofsson et al., 2009; Petersen et al., 1993; Silva et al., 2010; Vigo et al., 2007a; Vigo et al., 2007b; Zhao et al., 2005).
Целта на настоящата поредица от експерименти беше да се изследват ефектите на E2 върху хипоталамусната препро QRFP, QRFP-r1 (VMH/ARC) и QRFP-r2 (LH) mRNA експресия при женски плъхове, хранени или с HFD, или с LFD. Промените в експресията в естроусния цикъл, след OVX и след заместване на EB бяха оценени в VMH/ARC и LH.
Материали и методи
Животни
В тези експерименти са използвани възрастни женски плъхове Long Evans (Harlan, Inc., Indianapolis, IN) с тегло между 150–175 g при пристигане. Плъховете бяха настанени в стандартни клетки за обувки в одобрено от AAALAC (Асоциация за оценка и акредитация на лабораторни грижи за животни) животно на 12/12h цикъл светлина/тъмнина (светлините са включени в 0700) с храна и вода, налични по желание. Плъховете получиха непрекъснат достъп до гранулирана диета с високо съдържание на мазнини (HFD, 60% kcal от мазнини; D12492; Research Diets, New Brunswick, NJ) или гранулирана диета с ниско съдържание на мазнини (LFD, 10% kcal от мазнини; D12450B; Research Diets) Всички процедури са одобрени от Центъра за биомедицински изследвания в Пенингтън и Центъра за здравни науки на LSU Институционални комитети за грижа и употреба на животните.
Експеримент 1: Влияние на еструсния цикъл върху експресията на хипоталамусния ген
Определянето на естрозния цикъл започна 2 седмици след достъп до диета с HFD или LFD. През това време се измерва телесното тегло и приема на храна. Ежедневни вагинални цитонамазки се вземат чрез промивка от колоездещи женски плъхове между 0900 и 1000 за 2 седмици. Определянето на естрозната фаза се основава на вагинална цитология на клетки, гледани под микроскоп с ниска мощност, както беше описано по-рано (Primeaux, 2011) Накратко, диеструсът е идентифициран от наличието на левкоцити и ядрени епителни клетки. Proestrus е идентифициран от големи клъстери с кръгли ядрени клетки и отсъствието на левкоцити. Еструсът е идентифициран от наличието на рогови клетки. Жените бяха евтаназирани след определяне на естроен цикъл и естросната фаза беше проверена чрез визуална проверка на репродуктивните органи (n = 7-13/фаза/диета). Мозъците бяха извадени, замразени върху сух лед и съхранявани при -80 ° C до по-нататъшна обработка.
Експеримент 2: Ефект на OVX върху експресията на хипоталамусния ген
За OVX женските плъхове са анестезирани с изофлуран (1,5–3% в кислород) непосредствено преди операцията. Гръбните странични области на плъха бяха обръснати, почистени и инжектирани с местна упойка (Лидакаин/Бувикаин; 1 mg/kg, sc) за намаляване на дискомфорта. Яйчниците бяха отстранени чрез малки двустранни разрези на гръбната страна. След като яйчниците бяха отстранени, мускулните разрези бяха зашити със стерилни резорбируеми (Vicryl) конци и кожните разрези бяха затворени с щипки за рани. След операция е даден карпрофен (1,0 mg/kg, sc) за следоперативна аналгезия. Плъховете са били хранени или с HFD, или с LFD, започвайки 2 седмици след OVX операция. Групите, хранени по двойки, бяха включени за контрол на хиперфагия, свързана с OVX (OVX-PF). Ежедневният калориен прием за групите OVX-PF се основава на дневния прием на HFD и LFD от колоездещи плъхове в експеримент 1. Измерват се телесно тегло и храна в продължение на 3 седмици. Отстраняването на яйчниците беше проверено по време на умъртвяването (n = 8–9/група/диета) и мозъците бяха отстранени, замразени върху сух лед и съхранявани при -80 ° C до по-нататъшна обработка.
Експеримент 3: Хипоталамусна генна експресия след лечение с EB
Женските плъхове са претърпели OVX операция, както е описано в експеримент 2. Плъховете са привикнали към HFD или LFD, започвайки 1 седмица преди OVX операцията. Започвайки 1 седмица след операцията, естрадиол бензоат (EB, 4 ug/100 μl, sc, @ 1500h) се прилага на всички плъхове на всеки 4 дни, за да имитира естростния цикъл на плъхове. Приемът на храна и телесното тегло се оценяват ежедневно в продължение на 3 седмици. Плъховете бяха жертвани или в 0900h в деня, в който трябваше да получат EB (група преди EB), или в 0900h в деня след администрацията на EB (EB group). Отстраняването на яйчниците беше проверено по време на умъртвяването (n = 8-10/група/диета) и мозъците бяха събрани, замразени и съхранявани при -80 ° C до по-нататъшна обработка.
Верижна реакция на полимераза в реално време (PCR)
Статистически анализ
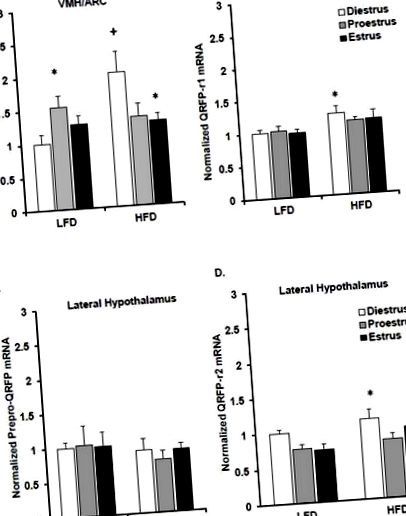
В експеримент 1, експресията на хипоталамусния ген се оценява чрез 2 × 3 ANOVA (диета × естрозна фаза). Средният дневен прием на храна в килокалории (kcal) се оценява по време на всяка фаза на естросния цикъл за всяка диета, като се използва еднопосочна ANOVA. Повишаването на телесното тегло се оценява с помощта на t-тест между участниците. В експеримент 2 се използва 2 × 3 ANOVA за анализ на разликите в експресията на хипоталамусния ген между диеструсите (от експеримент 1) и плъховете OVX и OVX-PF, консумиращи HFD или LFD. 2 × 2 ANOVA беше използван за анализ на разликите в средния дневен прием на храна и наддаването на телесно тегло между OVX и OVX-PF. В експеримент 3 се използва 2 × 2 ANOVA за оценка на ефектите от лечението с ЕВ върху генната експресия, средния дневен прием на храна и наддаването на телесно тегло при плъхове, консумиращи HFD или LFD. Използвани са post-hoc тестове на Bonferroni за сравняване на групи, когато е открит значим основен ефект или взаимодействие. Ниво на значимост на p Фигура 1А). При плъхове, хранени с HFD, нивото на пре-QRFP иРНК е най-високо по време на диеструс, докато при плъхове, хранени с LFD, експресията на мРНК на пре-QRFP е най-висока по време на проеструс. Открит е значителен ефект от диетата върху експресията на иРНК на QRFP-r1 в VMH/ARC (F = 4.3, p Фигура 1В). Експресията на QRFP-r1 е най-висока по време на диеструс при плъхове, хранени с HFD. Не бяха открити разлики в предварителните QRFP иРНК в LH (Фигура 1С), но QRFP-r2 иРНК беше значително повлияна от естроусен цикъл (F = 4.8, p Фигура 1D), като най-високата експресия се наблюдава по време на диеструса. Приемът на храна се различава в рамките на естрозния цикъл при жените, консумиращи HFD (F = 7,1, p Таблица 1). Плъховете в диеструма консумират повече храна, отколкото плъховете в еструса. Като цяло, плъхове, консумиращи HFD, са натрупали повече тегло от плъхове, хранени с LFD (t = 5,6, p Таблица 1).
Експеримент 2: Ефект на OVX върху експресията на хипоталамусния ген
Експресията на мРНК на Prepro-QRFP във VMH/ARC се увеличава от консумацията на HFD (F = 2,8, p Фигура 2А). Парното хранене отслабва индуцираното от OVX увеличаване на препре-QRFP експресията при плъхове, хранени с HFD, но не и при плъхове, хранени с LFD. Нивата на иРНК на QRFP-r1 във VMH/ARC също се повишават от консумацията на HFD (F = 5.6, p Фигура 2B). HFD и OVX не засягат препро-QRFP или QRFP-r2 иРНК в LH (Фигура 2C, 2D). Средният дневен прием на храна е по-висок при плъховете OVX, в сравнение с плъховете OVX-PF (F = 10,8, p Таблица 1). Плъхове, хранени с HFD, са наддавали повече тегло, отколкото плъхове, хранени с LFD (F = 60,3, p Таблица 1).
След OVX всички плъхове получават EB на всеки 4 дни. Въз основа на графика за приложение на EB, плъховете в групата преди EB са имали най-ниските нива на естрадиол, а плъховете в групата на EB са имали най-високи нива на естрадиол. A. Приемът на HFD увеличава препро-QRFP иРНК в VMH/ARC на плъхове в групата преди EB. Лечението с EB намалява нивата на препро-QRFP при всички плъхове. Б. Лечението с EB намалява експресията на QRFP-r1 mRNA във VMH/ARC. ° С. Експресията на mPNA на Prepro-QRFP в LH не се променя при лечение с EB. д. Лечението с EB намалява експресията на QRFP-r2 в LH. Стойностите са показани спрямо нивата на циклофилин и като гъвкава промяна от плъхове, хранени с LFD при диеструс. Данните са показани като средна стойност ± SEM, p Фигура 2, препре-QRFP експресията в VMH/ARC е повишена от OVX при плъхове, хранени с LFD. Двойното хранене не променя този ефект, въпреки че плъховете OVX-PF консумират по-малко храна и наддават по-малко тегло. Въпреки това, при плъхове, хранени с HFD, OVX повишава експресията на мРНК на пре-QRFP, която се отслабва чрез хранене по двойки. Отново приемът на HFD и наддаването на тегло бяха намалени чрез хранене по двойки и плъховете OVX-PF не ядоха повече HFD, отколкото LFD. Експресията на Prepro-QRFP в VMH/ARC на групата, хранена с OVF-PF с HFD, е повишена в сравнение с плъховете, хранени с LFD в диеструс, което предполага, че диетичният състав влияе върху експресията на QRFP, в отсъствието на OVX-индуцирана хиперфагия. Освен това, въпреки двойното хранене, плъховете OVX-PF, хранени с HFD, са натрупали повече тегло, отколкото техните колеги, хранени с LFD. Тези данни предполагат, че както E2, така и HFD влияят върху експресията на QRFP и че намаляването на калориите не е достатъчно, за да се намали експресията на VMH/ARC на препро-QRFP при липса на E2. След OVX, плъхове, консумиращи HFD, изразяват най-високите нива на препро-QRFP и QRFP-r1 иРНК, което предполага потенциално увеличаване на активността на QRFP в този мозъчен регион.
Третият експеримент е предназначен за оценка на пряката роля на Е2 върху експресията на иРНК на хипоталамус QRFP, QRFP-r1 и QRFP-r2. След OVX, всички плъхове се подлагаха на EB лечение на всеки четири дни, за да имитират естросния цикъл на плъхове. Този протокол се използва за предотвратяване на хиперфагия и прекомерно наддаване на телесно тегло след OVX. ИРНК на QRFP, QRFP-r1 и QRFP-r2 бяха измерени преди EB, което беше сутринта преди лечението с EB, и post-EB, което беше сутринта след лечението на EB. Те съвпаднаха с най-ниските и най-високите сутрешни нива на EB. Лечението с EB значително намалява експресията на пре-QRFP иРНК в VMH/ARC на плъхове, хранени с LFD и HFD, подкрепяйки регулирането на експресията на QRFP от E2. Лечението с EB също намалява експресията на QRFP-r1 и QRFP-2, особено при HFD плъховете, което предполага, че EB е в състояние да намали активността на QRFP. Подобно на констатациите в експеримент 2, консумацията на HFD увеличава експресията на QRFP в VMH/ARC преди лечението с EB. Интересното е, че това се е случило без наблюдавано увеличаване на общия среден дневен прием на храна или наддаване на тегло при плъхове, хранени с HFD, което отново предполага ефект от хранителните мазнини, който може да не зависи от хиперфагия и мощен ефект на E2 върху експресията на QRFP.
Акценти
Предварителната QRFP експресия на иРНК във VMH/ARC се влияе от естрозната фаза и HFD.
Овариектомията и приемът на HFD увеличават нивата на предварителни QRFP иРНК в VMH/ARC.
Приложението на естрадиол бензоат намалява нивата на мРНК на препро-QRFP в VMH/ARC.
Естрадиолът регулира експресията на QRFP в VMH/ARC на женски плъхове.
Благодарности
Това изследване беше подкрепено от LSUHSC-NO към SDP. Тази работа бе подкрепена отчасти от P20-RR021945 от Националния център за изследователски ресурси и NIH Center Grant 1P30> DK072476 на Pennington Biomedical Research Center.
Бележки под линия
Отказ от отговорност на издателя: Това е PDF файл на нередактиран ръкопис, който е приет за публикуване. Като услуга за нашите клиенти ние предоставяме тази ранна версия на ръкописа. Ръкописът ще бъде подложен на редактиране, набиране и преглед на полученото доказателство, преди да бъде публикуван в окончателния си вид. Моля, обърнете внимание, че по време на производствения процес могат да бъдат открити грешки, които биха могли да повлияят на съдържанието, и всички правни откази от отговорност, които се отнасят до списанието, се отнасят до.
- Диетата с високо съдържание на мазнини (eBook, ePUB) на Хелън Фостър; Zana Morris - Portofrei bei
- Какво е CBD неговите ползи за здравето и страничните ефекти JP диета
- Диетата с високо съдържание на въглехидрати Всичко, което трябва да знаете И рецепти По-близо
- Приемът на диета с високо съдържание на мазнини с различни нива на трансмастни киселини индуцира диференциално окислително действие
- Глагол на диета - английско спрежение - женски род - въпросителна форма