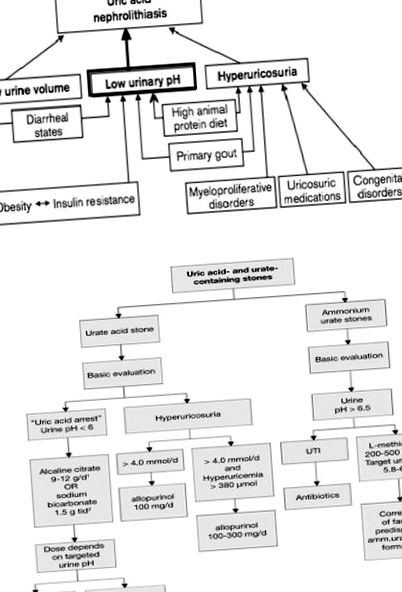
Графично резюме
Цитирано от Urolithiasis - EAU Guidelines 2016 с адаптация.
Резюме
По-задълбоченото разбиране на епидемиологията, както и патофизиологията на уролитиазата на пикочната киселина е важно за идентифицирането, лечението и профилактиката на камъни при тези пациенти. Постоянно ниското рН на урината, хиперурикозурията и ниският обем на урината са най-важните фактори в патогенезата на уролитиазата на пикочната киселина. Други различни причини за образуване на зъбен камък включват хронична диария, бъбречна хиперурикозурия, инсулинова резистентност, първична подагра, допълнителен пурин в диетата, неопластични синдроми и вродена хиперурикемия. Компютърната томография без контраст е радиологичният начин на избор за ранна оценка на пациенти с бъбречна колика. Като се изключат ситуации, при които има остра обструкция, нарастваща химия на кръвта, тежка инфекция или неразрешена болка, първоначалното лечение трябва да бъде медицинско разтваряне чрез орална хемолиза, тъй като този метод се оказа ефективен в повечето случаи.
Заден план
Метаболизъм на пурин и пикочна киселина
Пикочната киселина (2,6,8-триоксипурин) е крайният продукт на пуриновия метаболизъм и няма известна физиологична функция при хората. Ензимът уриказа липсва при хората и се среща при повечето бозайници, превръщайки пикочната киселина в алантоин (10–100 пъти по-разтворим). Концентрацията на пикочна киселина в урината зависи от рН на урината, обема на урината и отделянето на пикочна киселина. PH на урината е най-важният фактор за разтворимостта на пикочната киселина. Загубата на единичен протон от пикочна киселина и следователно дисоциацията на пикочната киселина се контролира от две дисоциационни константи (pKa). Първите рКа с рН 5,5 управляват превръщането на пикочната киселина в по-разтворимия анионен урат. Вторият рКа с рН 10,3 не е клинично значим синус, средното рН на човешката урина е 5,9 и обикновено варира от 4,8 до 7,4. При рН на урината 6.5 по-голямата част от пикочната киселина във формата на анионен урат [4].
Ендогенни източници
При нормални условия почти 300–400 mg/dL се произвеждат от de novo синтеза и тъканния катаболизъм. Ненормално висок синтез на пикочна киселина се появява при подагра, миелопролиферативни нарушения, някои вродени метаболитни дефекти и пациенти, получаващи химиотерапия поради бърз клетъчен оборот.
Екзогенни източници
Диета с високо съдържание на пурини напр. месо, животински органи, риба, сладкиши и мая.
В чревния тракт пурин → свободни нуклеинови киселини → инозинова киселина → хипоксантин → ксантин (чрез ксантиноксидаза) → пикочна киселина [5].
Бъбречна манипулация и елиминиране
Бъбрекът отделя две трети от пикочната киселина. Кожата, ноктите, косата, слюнката и стомашно-чревния тракт (GIT) елиминират останалата трета. В GIT бактериите превръщат част от пикочната киселина в амоняк и въглероден диоксид, който се изхвърля като газ. Амонякът или се абсорбира и отделя с урината, или се използва от бактериите като енергиен източник [6].
По-голямата част от серумната пикочна киселина (95%) е под формата на мононатриев урат и се филтрира свободно в гломерулите, докато останалата част е свързана с протеини. Деветдесет и девет процента от филтрирания урат се реабсорбират в проксималния извит канал (PCT) чрез сложна последователна реабсорбция, секреция и отново реабсорбция и 50% след това се секретират обратно в PCT. След секреторна абсорбция на 80% от този урат се случва в дисталния РСТ. Следователно около 10% от филтрирания урат се екскретира с урината. Фракционната екскреция на урат варира от 60% при недоносено новородено до 12% при 3 деца и 7% при възрастни [7], [8].
Лекарства и фактори, влияещи върху бъбречното боравене с пикочна киселина
Най-важните фактори, които оказват влияние върху бъбречната манипулация на пикочната киселина, включват състоянието на хидратация на пациента и отделянето на урина, серумна концентрация на урат, лекарства и разширение на извънклетъчния обем, което е обратно пропорционално на серумната концентрация на урат. Салицилатите, сулфинпиразонът и пробенецидът са урикозурични чрез блокиране на абсорбцията на урат в РСТ. Хиперурикозурията, причинена от тиазиди, се дължи на изчерпване на извънклетъчния обем и следователно увеличава секрецията на урат в РСТ. Хиперурикозурията по време на бременност се дължи на производството на урат на плода и увеличения вътресъдов обем [9], [10].
Епидемиология
Честотата на изчисленията на пикочна киселина варира в географски план, а честотата в световен мащаб варира от 5 до 40%. Честотата на нефролитиазата в САЩ се изчислява на около 0,5% годишно, честота на разпространение, която може да се обясни като нарастване [10]. В действителност, когато се обобщават данните от Националното проучване на здравето и храненето на САЩ II и III, се съобщава, че честотата на появяващите се заболявания е нараснала от 3,8% през 1976 г. до 5,2% през 1980 до 1994 г. в най-развитите страни [11]. По същия начин годишните икономически разходи, свързани със състоянието, също са се увеличили от отчетени 1,3 млрд. Долара през 1994 г. до 2 млрд. Долара през 2000 г., независимо от факта, че различни мерки като минимално инвазивни процеси, намаляват периодите на хоспитализация, и са приети промени в предлаганите грижи в амбулаторните клиники [12].
Установено е, че нефролитиазата на пикочната киселина представлява около 7–10% от всички калкули. Калкули, изолирани от пациенти, които са били в административната система на ветераните, са установили, че около 9,7% са съставени само от пикочна киселина. В друга голяма поредица беше съобщено, че калкулите на пикочната киселина са открити в 7% от изследваните камъни. Повечето автори смятат, че тази честота е грешно изчисление на истинската честота; това обаче показва важността на това състояние [13], [14].
Появата на камъни с пикочна киселина се различава с; възраст, пол, демографски данни и дори местните екологични аспекти. Например при ретроспективно изследване, при което има шест хиляди пациенти, мъжете са повече от шестдесет и пет години, за да развият камъни с пикочна киселина, два пъти по-разпространени при мъже, приблизително три пъти повече от мъжете [15], [16].
Дисперсията в съотношението на калкула на пикочна киселина може също да варира между различните етнически групи. Половината от пациентите с хмонг, които са имали бъбречни камъни, са имали камъни с пикочна киселина, докато са били при пациенти, които не са хмонг; само 10% са имали състоянието. Честотата или изчисленията на пикочна киселина са 6% сред белите и 30% сред не-белите. Съотношението на честотата в други държави е по-малко от 1% в Индия, 440% в Израел и по-малко от 4% в Япония [17], [18].
Установено е, че околната среда определено влияе върху образуването на камък на пикочната киселина. Честотата на образуване на смятане е била 9% за работниците, работещи в гореща среда, докато честотата на тези, които работят в стандартна работна среда, е 0,9%. Недостатък на това проучване е, че съдържанието на смятане не се отчита в изследването [18], [19].
Патофизиология
Образуването на зъбен камък е сложна процедура, която включва биохимични нарушения на урината, стимулиращи зародиш на кристали, агрегация и вероятно адхезия. Доказано е, че бъбречните плаки на Randall играят роля в образуването на калциев оксалат, но не и пикочна киселина, в различни изследвания, които изследват бъбречната тъкан, събрана по време на перкутанна нефролитотомия [20], [21]. Всъщност, нарушенията на уринирането, които влияят върху развитието на калкула на пикочната киселина, обхващат постоянно ниско рН на урината (основният фактор), хиповолемия и ниски нива на урината и хиперурикозурия (обяснено като дневна пикочна киселина над пикочните пътища при жени и 800 mg/d при мъжете) [22], [23].
Постоянно ниско рН на урината
Уролитиазата на пикочната киселина обикновено се свързва с постоянно ниско рН на урината. Почти всички пациенти с камъни в пикочната киселина демонстрират постоянно ниско рН на урината, докато по-голямата част отделя нормални количества урати. [24], [25] От друга страна, се предполага, че пациенти без вродени или постигнати условия, които предразполагат към образуване на камъни в пикочната киселина, се предполага да има или идиопатична нефролитиаза на пикочна киселина, или „подагрозен диатез [25], [26]. И двете представляват синдром на първична подагра и се илюстрират с висока серумна пикочна киселина, намалена фракционна екскреция на пикочна киселина и постоянно ниско рН на урината. Смята се, че ниското рН на урината индуцира калкули в пикочната киселина чрез основна киселинно-алкална химия и разтворимост на пикочната киселина [9], [27].
Пациентите с ниско рН на урината, но с редовна секреция на пикочна киселина, могат да развият камъни в пикочната киселина, докато други със стандартно или повишено рН на урината, но допълнителна секреция на урат не го правят [28]. Този факт може да бъде демонстриран с дисоциацията на пикочната киселина във вода. Азотът в позиция N-9 на урата, когато се разтвори във вода, може да получи свободен протон за развитие на пикочна киселина.
Първата константа на дисоциация на киселина (рКа) от тази реакция е 5,5 pH; втората рКа няма физиологично значение. Константата на разтворимост (Ksp) на пикочната киселина е приблизително 100 mg/L във водни разтвори при 37 ° C, докато уратът е 20 пъти по-разтворим. Уратът и пикочната киселина съществуват в равни пропорции при рН, равно на рКа (уравнение на Хендерсън-Хаселбах) [10], [29]. Следователно, ако 200 mg урат се добавят към 1-L воден разтвор с рН 5,5 при 37 ° C, 100 mg ще се превърнат в пикочна киселина, а останалата част ще продължи да бъде урат. Напротив, ако 1200 mg урат се добавят към еднакъв обем при рН 6.5, 1100 mg ще останат във разтворима форма на урат. Тези взаимодействия се релефират на върха на кривата на дисоциация на пикочната киселина при това pH, което плато при pH от почти 7.2 [11], [30].
Въпреки това, прецизният механизъм на постоянно подкиселена урина, докладван с камъни в пикочната киселина, все още не е ясен. Въпреки това се предлагат редица различни хипотези. Участниците, които имат идиопатична нефролитиаза на пикочната киселина, и обикновените субекти, и двамата на контролирана диета, бяха сравнени [31]. Сравнението показа, че образувателите на камъни в пикочната киселина имат постоянна кисела урина, както и по-малко отделяне на киселинното им натоварване под формата на амоний. Вместо това те зависят от по-голямо количество титруема киселинна секреция. Освен това, тези пациенти също имат по-малко ефективна реакция към натоварване с амониев хлорид през устата, което се потвърждава чрез секреция на амоний в урината в 7 пъти по-малки количества от тези при обикновените участници.
Тези открития предполагат, че тези пациенти имат нарушение на амониевата секреция, което води до загуба на значителен пикочен буфер. Без този буфер, леко повишаване на концентрацията на Н може значително да намали pH. Изследователите предполагат, че дефектите в ензимите глутаминаза и/или глутамат дехидрогеназа, които метаболизират глутамин в амоняк и кетоглутарат, могат да доведат до нарушена амониева секреция. Нещо повече, те също така теоретизират, че ниската консумация на глутамин по пътя може да го промени до други пътища, които използват глутамин, което води до хиперурикемия [8], [32], [33].
Тези две предпоставки са подпомогнати от констатациите за повишени плазмени нива на глутамат при участници, които имат нефролитиаза на пикочната киселина и, когато получават 15 N-белязан глицин, интегрират повече 15 N в пикочната киселина, отколкото амонията, за разлика от контролите. Независимо от това, трябва да се отбележи, че други изследователи не са открили ясни вариации между активността на бъбречната глутаминаза при участници с подагра и тези, които нямат подагра.
Точната функция на катаболизма на бъбречния глутамин като причина за неадекватно отделяне на амоний в урината все още не е ясна. За да се образуват конкременти на пикочната киселина, рН трябва да остане постоянно ниско и не само ниско. При образуващите се без калкул урина понякога може да развие киселинност, достатъчна да утаи кристали, въпреки нормалните концентрации на пикочна киселина; въпреки че се смята, че преходното алкализиране на урината, което се случва по време на хранене, спира прогресията до добросъвестни калкули. Периодичните алкални приливи в урината разтварят всички кристали на пикочната киселина, които са създадени в резултат на преходно кисела урина, която поддържа този модел. Условия, които теоретично могат да доведат до отсъствие на алкални приливи и отливи, са: повишена бъбречна тубулна реабсорбция на бикарбонат, намалена скорост на гломерулна филтрация, водеща до намалено филтрирано натоварване на бикарбонат и дефектна секреция на стомашна киселина. Наличната информация предполага, че се подозира, че неразпознат бъбречен дефект води до неспособност да произведе физиологичния алкален прилив в урината, а не до нарушена секреция на стомашна киселина [9], [34], [35].
Хиперурикозурия
Хиперурикозурията с редовно рН на урината може също да доведе до образуване на смесени камъни, съставени от урат и калциев оксалат. Въпреки че уратът в повечето пъти е по-разтворим от пикочната киселина, може да се отбележи, че това не е значително по-голямо. Мононатриевият урат при високи нива се утаява от разтвора и се предполага, че води до кристализация на калциев оксалат чрез всеки от тях; затихването на макромолекулните инхибитори на литогенезата, хетерогенното зародиш и появата на осоляване. Хиперурикозурията в повечето случаи произтича от хранителна недискретност, въпреки че мутациите в канала URAT1 могат да доведат до вродена бъбречна хипоурикемична хиперурикозурия [7], [36], [37].
Нисък обем на урината
Намаленото отделяне на урина води до повишени концентрации на литогенни разтворени вещества в урината. Високите концентрации на урат могат да доведат до утаяване на пикочна киселина и мононатриев урат в резултат на ограничена разтворимост на пикочна киселина. Следователно, камъните с пикочна киселина са преобладаващи в тропиците и горещите среди [38], [39].
Макромолекулни инхибитори на кристализацията
Урината съдържа фактори, които инхибират образуването на кристали, които модулират кристализацията на пикочната киселина и образуването на зъбен камък. Повърхностно активните вещества в урината, гликопротеините и гликозаминогликаните (GAGs) имат инхибиторен ефект върху кристализацията на пикочна киселина [40]. Проучванията показват значително по-ниски нива на GAG в урината на генетично и географски изолирани образуващи пикочна киселина. Все още не е ясно как дефицитът на такива инхибитори може да причини образуване на камъни в пикочната киселина [40], [41], [42].
Фамилни, генетични и екологични фактори предразполагат към образуването на уринарни камъни. Съобщава се, че генът ZNF365, разположен в хромозома 10q21-q22, е свързан с уролитиаза на пикочната киселина. Въпреки че тази ДНК кодира четири различни протеина чрез заместващо сплайсинг, само един подсказва напредъка на калкула на пикочната киселина [43]. Точната роля на тези гени все още е неясна.
От друга страна, нов ген на хомолог за ДНК, който не е очевиден при мишките, докато обикновено присъства като неизразен ген както в старите, така и в новите световни маймуни, изглежда се появява в ерата на миоцена, въртящ се във времето, когато маймуните са загубили целта си на уриказа. Продуктът от този ген може да предпази от вредното въздействие на хиперурикемията поради заглушаването на гена на уриказата, като същевременно не губи положителните си въздействия [43], [44].
Необходими са бъдещи проучвания, за да се установи действителната роля на този генен продукт в организма и образуването на камъни в пикочната киселина. Въпреки това, понастоящем всяко усилие за обяснение на ролята на това ще бъде чисто хипотетично (фиг. 1 А, Б).
- Епидемиология, патофизиология и управление на уролитиаза на пикочна киселина Преглед на разказа -
- Консумацията на подсладени със захар напитки и серумни концентрации на пикочна киселина систематичен преглед и
- Кучешко и котешко затлъстяване преглед на патофизиологията, епидемиологията, VMRR
- Препоръки за хранене и начин на живот за профилактика на уролитиазата Систематичен преглед на литературата -
- Диетично управление на уролитиаза (Сборник) DVM 360