Свързани термини:
- Новообразувание
- Витамин D
- Мутация
- Профилактика на рака
- Риск от рак
- Кибрид
- Андроген
- микроРНК
- Рак на простатата
Изтеглете като PDF
За тази страница
Пушенето и здравето на мъжете
Рак на простатата
Етиологията на рака на простатата остава неуловима концепция. Смята се, че няколко фактора допринасят за неговото развитие: генетично предразположение, диета, инфекции, хормонален дисбаланс и излагане на токсини (като тези, открити в CS) [120]. През 2015 г. Картър и сътр. публикува данни от надлъжно кохортно проучване, обхващащо почти 1 милион пациенти (както мъже, така и жени) в Съединените щати. Това разкрива значението на тютюнопушенето при рак на простатата. Пушенето не само увеличава честотата на рак на простатата, но също така повишава риска от заболяване в напреднал стадий и смъртността е била с 43% по-висока при пушачите [121]. Не се знае много за възможната етиопатология. Едно северноиндийско проучване през 2011 г. оценява 578 мъже с рак на простатата. Те откриха повишени нива на възпалителния цитокин IL-18 при мъжете, които пушат. Нещо повече, той също е свързан с по-висок стадий на заболяването. Предполага се, че хроничното възпаление допринася значително за развитието на рак на простатата [122] .
Риск от рак и вегетариански диети
13 Рак на простатата
Малко се знае за етиологията на рака на простатата и единствените добре установени рискови фактори са увеличаване на възрастта, фамилна анамнеза, черен етнически произход и генетични фактори. Екологичните проучвания показват, че рискът може да бъде положително свързан с диета в западен стил и диетите с високо съдържание на червено месо, млечни продукти и животински мазнини са замесени в развитието на рак на простатата, но данните не са последователни и като цяло не са убедителни. За вегетарианците британските кохорти отчитат относителен риск от рак на простатата при лактовегетарианците в сравнение с месоядните от 0,86 (0,61–1,11), AHS съобщава за относителен риск от 0,65 (0,44–0,95), а AHS-2 отчита относителния риск от 0,96 (0,66–1,24) (Таблица 19.2).
Рискът от рак на простатата е положително свързан с циркулиращите нива на IGF-1 и веганите имат относително ниски циркулиращи концентрации на този хормон. Кохортите в Обединеното кралство отчитат относителен риск от рак на простатата при вегани в сравнение с месоядните от 0,61 (0,31–1,20), а AHS-2 отчита относителен риск от 0,66 (0,50–0,87) (Таблица 19.3); тези открития са в съответствие с хипотезата, че веганите могат да имат намален риск от рак на простатата, но те се основават само на 68 случая при вегани и са необходими повече изследвания по тази тема.
Хормонална канцерогенеза
III Рак на простатата
Изобилието от данни свързва андрогенните хормони с етиологията на рака на простатата. Орхиектомията води до инволюция на простатата и е призната за ефективна терапевтична схема за лечение на рак на простатата. Проспективните проучвания не са показали силни взаимовръзки между риска от рак на простатата и циркулиращите нива на тестостерон, дихидротестостерон, андростендион и няколко други андрогенни хормони. Няколко проучвания обаче демонстрират, че вариантните алели на гена, кодиращ андрогенния рецептор (AR), могат да модифицират риска от рак на простатата. AR генът съдържа в екзон 1 полиморфно повторение на CAG, което кодира глутаминов тракт с променлива дължина, който изглежда оказва влияние върху способността на AR да активира генната транскрипция. Изглежда, че рискът от рак на простатата е обратно корелиран с броя повторения на CAG в AR. Полиморфно повторение на GGC в екзон 1 на AR, кодиращо глицинов тракт с променлива дължина, може също да промени риска от рак на простатата.
Епидемиологичните проучвания свързват дефицита на витамин D с рака на простатата и многобройни лабораторни изследвания показват ролята на хормонално активната форма на витамин D, 1,25-дихидроксивитамин D3, в регулирането на пролиферацията и оцеляването на клетъчните линии на рака на простатата. 1,25-дихидроксивитамин D3 функционира чрез рецептор, който е член на суперсемейството на ядрените рецептори. Идентифицирани са няколко алелни варианта на рецептора за витамин D и проучванията показват, че тези варианти могат да бъдат свързани с променен риск от рак на простатата. Въпреки че не всички от тези проучвания съвпадат по отношение на връзките между специфични полиморфизми и риск, те заедно предполагат, че генът, кодиращ рецептора на витамин D, може да действа като модификатор с ниска пенетрантност на развитието на рак на простатата.
Нобъл е първият, който съобщава, че непрекъснатото лечение или с тестостерон, или с тестостерон в комбинация с естроген индуцира развитието на рак на простатата при плъховете NBL. Поредица от изследвания на S.-M. Хо и колеги посочват, че лечението на интактни плъхове с NBL с тестостерон и Е2 в продължение на 16 седмици предизвиква висока честота на епителна дисплазия в дорзолатералния лоб на простатата. В сравнение с околния епител, диспластичните лезии показват няколко промени в генната експресия, които могат да допринесат или да бъдат резултат от тяхното развитие, включително повишена експресия на мРНК на Ha-ras и прогестеронови рецептори. Индукцията на диспластичните лезии се инхибира чрез лечение с бромокриптин, което предполага, че пролактинът допринася за тяхното развитие. Интересното е, че местоположението на хормонално-индуцираните лезии в простатата изглежда зависи от количеството и/или вида на прилагания естроген. Например, тестостеронът в комбинация с повишен Е2 предизвиква атипична хиперплазия във вентралния лоб на простатата. По същия начин, лечението на плъхове с NBL с тестостерон плюс DES предизвиква дисплазия в вентралната простата.
Изследвания на Bosland и колеги показват, че продължителното лечение на плъхове с NBL с тестостерон и Е2 предизвиква 100% честота на аденокарцином в дорзолатералната, но не и в вентралната простата на плъховете с NBL. ДНК адукт с неизвестна структура е открит в дорсолатералната, но не и в вентралната простата на плъховете с NBL, лекувани с тестостерон и Е2 в продължение на 16 седмици или повече. Съвсем наскоро Y. C. Wong и колеги публикуваха поредица от изследвания върху индуцирането на карцином в вентралната простата на плъх NBL чрез непрекъснато лечение с тестостерон и високи дози Е2.
Възпаление и инфекция в етиологията на рака на простатата
Д-р Siobhan Sutcliffe, д-р Michel A. Pontari, в рак на простатата (второ издание), 2016 г.
Резюме
Ролята на инфекцията и възпалението в етиологията на рака на простатата (PCa) не е напълно ясна. Някои доказателства сочат, че има възпалителни лезии, свързани с PCa, които също корелират с прогнозата. Самото възпаление при биопсия не винаги корелира с PCa. Има механизми, които да обяснят защо възпалението може да допринесе за PCa и някои възпалителни гени, които може да са важни. Доказателствата за специфични възпалителни биомаркери са ограничени. Ролята на диетата и инфекцията не са сигурни. Връзката на възпалението и може би инфекцията вероятно включва подбуждане на събития при генетично податливи хора, повлияни от тяхната среда, за да допринесат за развитието на PCa.
Рак на простатата
Етиология
Актуализация на регулирането на апоптозата при рак на простатата
Р. Уилям,. Джон М. Фицпатрик, в Рак на простатата, 2003
Каспази: значението им при апоптозата на простатните клетки
Ролята, която каспазите играят в нормалния процес на самообновяване на простатната жлеза и в етиологията на рака на простатата, се превръща в основна област на изследванията на рака на простатата. Разбирането за това как дерегулацията на каспазите допринася за развитието на рак, вероятно ще помогне в терапевтичните стратегии, насочени към предотвратяване на прогресията към андроген-нечувствителното състояние.
Имунохистохимията на простатата демонстрира експресията на каспаза-3 и каспаза-1, и двете от които корелират с клетъчния тип и физиологията. 85 Оцветяването за каспаза-3 показва ниска експресия на базалните клетки в сравнение с секреторните клетки на жлезата. Високата експресия на каспаза-3 в луминалните секреторни клетки корелира с висок клетъчен оборот, обяснявайки как се поддържа равновесен процес в равновесно състояние на самообновяване на жлезата. Последните проучвания също демонстрират намалена протеинова експресия на каспаза 3 86, 87 и каспаза 1 87 с повишена степен по Gleason.
Доказано е също, че каспазите са замесени по време на регресия на простатата след кастрация. Профилите на простатната тъкан, получени от кастрирани мишки и плъхове, оцветяват специално за обработени каспази. 88 По същия начин инхибирането на каспазите чрез свръхекспресията на CrmA, вирусен инхибитор на активността на каспазата, предотвратява индуцираната от андроген абстиненция апоптоза in vitro. 89 Продължаващият растеж на андроген-нечувствителни тумори след отнемане на андрогена може следователно да е резултат от променена апоптотична сигнализация, медиирана от инхибиране на каспаза. По същия начин, възможността ракът на простатата да метастазира може да включва механизми за инхибиране на каспаза. Използвайки неметастатичен вариант на клетъчната линия на рак на простатата LNCaP (LNCaP-Pro5), беше установено, че тези клетки са по-чувствителни към апоптотична индукция, отколкото техните метастатични аналози. 90 Такива изследвания предполагат, поне in vitro, че апоптотичната резистентност (инхибиране на каспаза) се увеличава с метастатичния потенциал на клетъчните линии на рак на простатата при човека.
Тези проучвания биха включили роля за терапевтичната манипулация на каспазите при рак на простатата, или чрез тяхното повишено активиране, или чрез намаляване на тяхното инхибиране чрез експресията на IAP или активирането на AKT пътя.
Витамин D хормон
Eiji Munetsuna,. Тошиюки Сакаки, във Витамини и хормони, 2016
3.1 Витамин D и рак на простатата
Диетични интервенции
LAUTA KHAODHIAR, GEORGE L. BLACKBURN, в Хранителна онкология (Второ издание), 2006
Диетични мазнини
Въпреки значителния напредък в ранното откриване и лечение на рак на простатата, малко се знае за екологичните и генетични фактори, които причиняват заболяването. Основният проблем при канцерогенезата на рака на простатата не е инициирането на заболяването, а неговото насърчаване и прогресиране (Fleshner et al., 2004). Констатациите от аутопсии показват, че 80% от мъжете са имали микроскопични огнища на рак на простатата до 80-годишна възраст (Sakr et al., 1996). Въпреки че честотата на тези огнища на латентен рак е сходна в целия свят, тя може да варира в различните държави с 20 пъти (Wynder et al., 1971). Тези огнища също изглеждат по-обширни, мултифокални и с по-висок клас при мъжете от западните страни (Breslow et al., 1977).
Доказателства - че мъжете, които мигрират, са склонни да получават честотата на инцидентите в приемащата държава (Haenszel и Kurihara, 1968) и че честотата на рака на простатата варира драстично при едни и същи популации, живеещи в различни географски местоположения (Kolonel et al., 1999) - силно предполага, че факторите на околната среда могат да повлияят на прогресията на латентния рак в по-агресивно състояние (Haenszel and Kurihara, 1968; Kolonel et al., 1999). Екологичните проучвания показват пряка връзка между международната смъртност от рак на простатата и очакваната консумация на диетични мазнини на глава от населението (Rose et al., 1986). При животинския модел на рак на простатата диетата с ниско съдържание на мазнини намалява темповете на туморен растеж (Wang et al., 1995).
В преглед на 33 публикувани проучвания за контрол на случая и кохорти за връзката между рака на простатата и хранителните мазнини или специфични видове мазни храни, 8 проучвания установяват значителна връзка. Освен това много изследвания предполагат асоциации за специфични видове мазни храни (Fleshner et al., 2004). Сред проучванията за контрол на случая, около половината установяват повишен риск с висок прием на хранителни мазнини, животински мазнини и наситени и мононенаситени мазнини (Zhou and Blackburn, 1997; Fleshner et al., 2004). Сред седем кохортни проучвания само HPFS установява връзка между общата консумация на мазнини и риска от напреднал рак на простатата (RR = 1,79, най-висок спрямо най-ниския квинтил на прием) (Giovannucci et al., 1993).
В това проучване асоциацията почива предимно с животински мазнини, особено мазнини от червено месо (но не и растителни). Мазнините от млечни продукти (с изключение на масло) или риба не са свързани с риск. Две други кохортни проучвания съобщават за положителни връзки или с наситени мазнини, или с храна, съдържаща мазнини (като мляко, сирене, масло, месо и яйца). В кохорта мъже от японски произход, живеещи на Хаваите, млякото, яйцата и сиренето са свързани с риска от рак на простатата, въпреки че общите мазнини, наситените и ненаситените мазнини не са (Severson et al., 1989). По същия начин кохорта възрастни адвентисти от седмия ден показа положителни връзки между фаталния рак на простатата и консумацията на мляко, сирене и яйца (Snowdon et al., 1984; Snowdon, 1988).
Механизмите, отговорни за възможната връзка между хранителните мазнини и рака на простатата, не са известни. Предложени са няколко хипотези, включително следното:
Диетичните мазнини могат да повишат нивата на андроген в серума. Androgen вероятно ще играе роля в етиологията на рака на простатата (Kolonel et al., 1999). Андрогените контролират клетъчния растеж в простатата (Ford et al., 1994), а намаляването на производството на андроген е основата при лечението на рак на простатата. Освен това мъжете, кастрирани в млада възраст, не развиват карцином на простатата (Sakr et al., 1996). Наблюдателни проучвания установяват, че промените в приема на хранителни мазнини влияят върху нивата на андрогените в серума и урината при мъжете (Hill et al., 1979; Howie and Shultz, 1985). В изследване на близнаци, близнакът, консумирал повече мазнини, е имал по-високи нива на тестостерон (Bishop et al., 1988). В рандомизирано кръстосано проучване на диетична интервенция с ниско съдържание на мазнини, с високо съдържание на фибри и с високо съдържание на мазнини и с ниско съдържание на фибри, мъжете на диета с високо съдържание на мазнини и ниско съдържание на фибри са имали 13–15% по-високи плазмени концентрации на общия и половия хормон свързващ глобулин (SHBG) - свързан тестостерон и тестостерон в урината, отколкото мъжете на диета с ниско съдържание на мазнини и високо съдържание на фибри (Dorgan et al., 1996).
Специфични видове мастни киселини или техните метаболити могат да инициират или насърчават рак на простатата. Въпреки че данните са ограничени, проучванията in vitro показват, че линолевата киселина, омега-6 полиненаситена мастна киселина, може да стимулира растежа на рака на простатата при човека, докато докозахексаенова киселина (DHA) и ейкозапентаенова киселина (EPA), две омега-3 мастни киселини присъстват в рибените масла го инхибирайте (Rose and Connolly, 1991; Connolly et al., 1997). Друго проучване in vitro съобщава, че ниските концентрации на линоленова киселина (също омега-3 мастна киселина) и EPA насърчават растежа на простатните клетки (Pandalai et al., 1996). Проучване за контрол на случаите при хора в Уругвай съобщава за положителна връзка между а-линоленова киселина и рак на простатата (De Stefani et al., 2000). По същия начин данните от HPFS установяват, че а-линоленова киселина, но не и линолова киселина, е свързана с напреднал риск от рак на простатата (Giovannucci et al., 1993). Основните източници на линоленова киселина в тези проучвания включват червено месо, млечни храни, майонеза, маргарин и масло.
Диетичните мазнини са прооксидант и могат да увеличат маркерите на оксидативен стрес (Fleshner and Klotz, 1998). Полиненаситените мастни киселини предлагат податлива цел за много от тези окислителни видове, образувайки липидни радикали и хидропероксиди, които могат да генерират допълнителни кислородни радикали и/или увреждане на ДНК (Kolonel et al., 1999).
Животински модели на човешка болест
Прогресията на рака на простатата е бавен и многоетапен процес; клинично откриваем рак на простатата обикновено се проявява при възрастни мъже, въпреки че лезиите може да са възникнали много по-рано в живота. Животински модели, които имитират инициирането, прогресирането и метастазирането на рак на простатата при човека, са необходими, за да се разбере етиологията на рака на простатата и да се разработят нови лечения. Неотдавнашният напредък в технологията за генно инженерство на мишки доведе до генерирането на поредица модели мишки за изследване на рак на простатата, които са широко използвани за тестване на въздействието на единичен или комбинации от няколко генни промени върху началото, прогресията и метастазирането на тумори на простатата, както и за оценка на ефектите от екологични, клинични и предклинични лекарства за профилактика и лечение на рак на простатата. Въпреки че е възможно нито един „перфектен“ модел да не може да рекапитулира всички аспекти на това силно хетерогенно заболяване, очаква се моделите, имитиращи някои аспекти на рака на простатата, да продължат да предоставят предклинично ръководство за лечение на това разпространено заболяване.
Витамин D, слънчева светлина и естествената история на рака на простатата
GARY G. SCHWARTZ, TAI C. CHEN, във Витамин D (Второ издание), 2005 г.
Б. Описателната епидемиология на рака на простатата: Ефекти от възрастта, расата и мястото
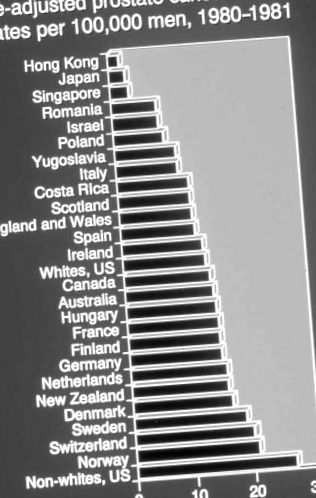
Ракът на простатата е най-честият инцидентен рак (без кожа) сред американските мъже и след рак на белите дробове най-фатален, отчитащ приблизително 221 000 нови случая и 29 000 смъртни случая през 2003 г. [11]. Клиничният рак на простатата е силно зависим от възрастта: смъртността нараства логаритмично с възрастта и е приблизително 50% по-висока сред афро-американците, отколкото сред кавказците. Освен възрастта и расата, най-забележителната характеристика на смъртността от рак на простатата е поразителна вариация по места: степента на смъртност варира над двадесет пъти в целия свят и е най-висока сред афро-американците и северните европейци [12] (вж. Фиг. 1) . Сходството в нивата на смъртност между афро-американците и северноевропейците е важна улика, тъй като предполага, че тези популации могат да споделят някакъв общ фактор, който лежи в основата на подобния им опит със смъртността. Всъщност, каквато и теория за етиологията да има ракът на простатата, която някой предлага, тя трябва да отговори на въпроса: Как са афроамериканците и северноевропейците?
ФИГУРА 1 . Световни коефициенти на смъртност при рак на простатата, извлечени от данни в Kurihara et al. Коефициентите на смъртност показват двадесеткратни вариации и са най-високи сред афроамериканските мъже и сред населението на Северна Европа.
Уникална характеристика на епидемиологията на рака на простатата е високото разпространение на „инцидентен” (известен също като „субклиничен“ или „аутопсия“) рак. Аутопсиите при мъже, починали от причини, различни от рак на простатата, разкриват, че приблизително 27% от мъжете на 40 и 34% от мъжете на 50 са с хистологичен рак на простатата [13]. Преобладаването на тези субклинични видове рак достига 60% при мъжете на възраст над 80 години и продължава да нараства с възрастта [14]. Хистологично тези лезии не се различават от рака на простатата, който е потенциално животозастрашаващ и се счита, че представлява рак на по-ранен етап от естествената им история. За разлика от смъртността, разпространението на инцидентни тумори на простатата е сходно сред възрастните мъже по света, независимо от техния расов или географски произход [15, 16]. Несъответствието между появата на клиничен и субклиничен рак на простатата предполага, че клиничният рак е резултат от фактори, които управляват растежа на субклиничния рак. По този начин, всяка етиологична хипотеза за рак на простатата трябва също да обясни защо субклиничният рак на простатата е повсеместен, докато клиничният рак на простатата не е.
- Дъвка - общ преглед на ScienceDirect теми
- Функционална напитка - общ преглед на ScienceDirect теми
- Кожен васкулит - общ преглед на ScienceDirect теми
- Диетичен прием - преглед на ScienceDirect теми
- Функционално стомашно-чревно разстройство - общ преглед на ScienceDirect теми