Андрей В. Марахонов
1 Изследователски център за медицинска генетика, Москва, Русия
2 Московски физико-технологичен институт, Долгопруден, Русия
7 Лаборатория по генетична епидемиология, Изследователски център по медицинска генетика, ул. Москворечие, 1, Москва, Руска федерация 115478
Федор А. Коновалов
3 Геномед ООД, Москва, Русия
Амин Кх. Макаов
4 Централна районна болница Khabez, Khabez, Русия
Татяна А. Василиева
1 Изследователски център за медицинска генетика, Москва, Русия
Виталий В. Кадишев
1 Изследователски център за медицинска генетика, Москва, Русия
Варвара А. Галкина
1 Изследователски център за медицинска генетика, Москва, Русия
Елена Л. Дадали
1 Изследователски център за медицинска генетика, Москва, Русия
Сергей И. Куцев
1 Изследователски център за медицинска генетика, Москва, Русия
5 Руски национален изследователски медицински университет „Пирогов“, Москва, Русия
6 Московски държавен университет по медицина и стоматология, Москва, Русия
Рена А. Зинченко
1 Изследователски център за медицинска генетика, Москва, Русия
5 Руски национален изследователски медицински университет „Пирогов“, Москва, Русия
6 Московски държавен университет по медицина и стоматология, Москва, Русия
Конференция
Свързани данни
Наборите от данни, използвани и/или анализирани по време на настоящото проучване, са достъпни от съответния автор при разумна заявка.
Резюме
Заден план
Първичната микроцефалия представлява пример за клинично и генетично хетерогенно състояние. Тук описваме случай на първична микроцефалия от република Карачаево-Черкес, който първоначално е диагностициран със синдром на Seckel.
Представяне на дело
Клиничното секвениране на екзома на пробанда разкрива нова хомозиготна делеция на единичен нуклеотид в ASPM гена, c.1386delC, което води до преждевременен терминиращ кодон. Проучването на популацията разкрива, че честотата на алелите е по-малка от 0,005. Мутациите в този ген преди не са били свързани със синдрома на Seckel.
Заключения
Нашият случай представлява допълнителна подкрепа за клиничния континуум между синдрома на Seckel и първичната микроцефалия.
Заден план
В популациите от кръвни родове преобладаването на първичната микроцефалия се оценява на 1 на 10 000—6,8 на 10 000 [7]. Хомозиготните и съставни хетерозиготни мутации в гена на ASPM (MCPH5; OMIM # 605481) представляват до 40% от първичните случаи на MCPH както в семейства на близки, така и на неконсулти [8]. ASPM (Abnormal Spindle Microtubule Assembly) протеин е част от комплекс от майки центриоли; той регулира биогенезата на центриола по време на неврогенезата, апикалния комплекс и клетъчната съдба [9].
Тук представяме случай на първична микроцефалия със семейни рецидиви. Този случай е открит в район Khabezsky на Карачаево-Черкеската република, Русия, обитаван от приблизително 30 000 жители с преобладаващо черкезки произход (95,2%).
Представяне на дело
Родословие на семейството
Резултати от последователността на Sanger
Важно е, че хомозиготни и съединени хетерозиготни мутации на загуба на функция в гена ASPM са описани преди това при пациенти с автозомно-рецесивен първичен MCPH тип 5 (OMIM # 608716). ASPM: мутация p.Tyr462 * не е била открита по-рано в публично достъпните контролни кохорти (база данни за агрегиране на генома), както и в 202 контролни хромозоми, съвпадащи с популацията (скринирани от PCR-RFLP). Ето защо заключаваме, че според критериите на ACMG, по отношение на силата на кумулативните доказателства, тази мутация трябва да се разглежда като патогенна [15]. Тъй като мутацията причинява образуването на преждевременния стоп кодон - p.Tyr462 * - иРНК трябва да бъде цел за медиирано от глупости разпадане на иРНК (NMD), водещо до нулевия алел [16].
Тъй като тази мутация се е появила в хомозиготно състояние в пробанда, около мутацията се извършват оценки на дължината на региона на хомозиготност (ROH) според състоянията на алтернативни алели на чести SNP, обхванати от данни за секвениране на клинични екзоми. Установихме, че в това черкезко семейство регионът ROH се разпространява най-малко от rs79351096 до rs4950927, с минимална дължина 6,2 Mb. Всъщност дължината на ROH региона може да бъде дори по-голяма, тъй като клиничните данни за екзома, използвани за неговата оценка, обхващат само кодиращи последователности на гени, свързани с наследствени заболявания.
Дискусия
Заключения
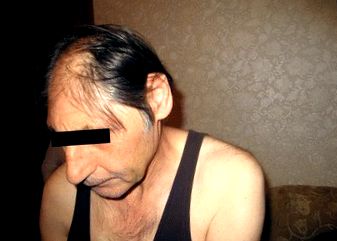
Представеният тук пробанд първоначално е диагностициран със синдром на Seckel поради първична микроцефалия, тежко умствено забавяне и характерни черти на лицето. Този фенотип не е често срещан в описаните случаи на първична микроцефалия, тъй като интелектуалното увреждане обикновено е по-тежко при синдром на Seckel, както и характерни черти на лицето, което може да съответства на относителното щадене на средно-лицевите структури в сравнение с останалата част на главата. Високопроизводителното секвениране на клинично значими гени в пробандата не идентифицира кандидат-нуклеотидни варианти в нито един ген, свързан със синдрома на Seckel. Единствената мутация, идентифицирана в това семейство, е изместваща рамка делеция на единичен нуклеотид, засягаща ASPM гена. Доколкото ни е известно, досега не са мутирани ASPM мутации с подобни на Seckel фенотипове. Следователно, нашето наблюдение разширява фенотипната хетерогенност на MCPH и подкрепя възгледа за MCPH и синдрома на Seckel като клиничен континуум.
Финансиране
Публикуването на тази статия е финансирано от Руската научна фондация [грант номер 17-15-01051].
Наличност на данни и материали
Наборите от данни, използвани и/или анализирани по време на настоящото проучване, са достъпни от съответния автор при разумна заявка.
Относно тази добавка
Тази статия е публикувана като част от BMC Medical Genomics Volume 11 Supplement 1, 2018: Избрани статии от Беляевска конференция 2017: медицинска геномика. Пълното съдържание на добавката е достъпно онлайн на https://bmcmedgenomics.biomedcentral.com/articles/supplements/volume-11-supplement-1.
Принос на авторите
AVM извършва молекулярно-генетични експерименти, анализира и интерпретира данните за пациентите, пише ръкописът. FAK анализира и интерпретира HTS данните на пациента. AKM събра проби. TAV допринесе за анализа на данните за пациентите, подготви ръкописа. VVK, VAG, ELD извършиха клиничен преглед на пациента. SIK и RAZ разработиха проучването и помогнаха за надзора на проекта. Всички автори прочетоха и одобриха окончателния ръкопис.
Бележки
Етично одобрение и съгласие за участие
Клиничното и молекулярно генетично проучване е проведено в съответствие с Декларацията от Хелзинки и одобрено от Институционалния съвет за преглед на Федералната държавна бюджетна институция „Изследователски център за медицинска генетика“, Москва, Русия, с писмено информирано съгласие, получено от всеки участник и/или техния законен представител, според случая.
Съгласие за публикуване
Съгласието за публикуване е получено от законния настойник на пациента.
Конкуриращи се интереси
Авторите заявяват, че нямат конкуриращи се интереси.
Бележка на издателя
Springer Nature остава неутрален по отношение на юрисдикционните претенции в публикувани карти и институционални принадлежности.
- Първична прогресивна афазия Франция PDF PPT Отчети за случаи Симптоми Лечение
- Дъвка без захар представлява опасност за здравето New Scientist
- Роберто Васкес Наказателно дело Wiki Fandom
- Протеинова прахообразна напитка ванилия - висококачествена подкрепа за мускулна маса
- Шест билки, които трябва да имате, за да поддържат вашата детоксикация; Храна за произход