Валтер Д. Лонго
1 Институт за дълголетие и Училище по геронтология на Дейвис, Университет на Южна Калифорния, Лос Анджелис, Калифорния 90089, САЩ
2 IFOM, FIRC Институт по молекулярна онкология, Via Adamello, 16, 20139 Милано, Италия
Сачидананда Панда
3 Регулаторна лаборатория по биология, Salk институт за биологични изследвания, La Jolla, CA 92037
Обобщение
Храненето при повечето животни е ограничено до определен период, оставяйки кратки периоди на гладуване, които съвпадат със съня. Постенето позволява на организмите да навлязат в алтернативни метаболитни фази, които разчитат по-малко на глюкоза и повече на кетонни подобни на тялото източници на въглерод. И периодичното, и периодичното гладуване водят до ползи, вариращи от профилактика до засилено лечение на заболявания. По същия начин, ограниченото във времето хранене (TRF), при което времето за хранене е ограничено до определени часове от деня, позволява ежедневният период на гладуване да продължи> 12 часа, като по този начин дава плейотропни ползи на множество организми. Разбирането на механистичната връзка между хранителните вещества и ползите от гладуването води до идентифициране на диети, имитиращи гладуване (ЯЩ), които постигат промени, подобни на тези, причинени от гладуването. Предвид плейотропните и трайни ползи от TRF и ящура, както фундаменталната наука, така и транслационните изследвания са оправдани да развият интервенции, свързани с гладуването, в ефикасни и евтини лечения с потенциал за подобряване на здравословния живот.
Въведение
Формите на живот на нашата планета са се развили под силното влияние на ежедневния цикъл светлина/тъмнина. Слънчевата светлина като основен източник на енергия за фотосинтеза, ежедневното производство на фотосинтетична биомаса има предвидим дневен ритъм. Ежедневното циклично производство на фотосинтезирана химическа енергия е в основата на хранителната верига. Ежедневните промени в светлината и тъмнината водят до дневни ритми в други параметри на околната среда, като температура и влажност. Такъв предсказуем и силен ежедневен ритъм в наличността на храна и факторите на околната среда доведе до развитието на a
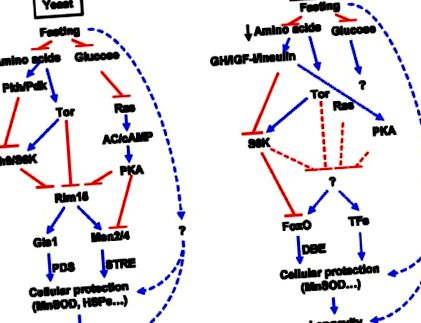
Запазени пътища за чувствителност на хранителни вещества при дрожди и мишки.
В бъдещи проучвания ще бъде важно да се разбере как условията на глад влияят върху способността на дрождите да възстановяват и заместват повредените органели и макромолекули. Простотата на едноклетъчните еукариоти вероятно ще продължи да дава фундаментални нови идеи и ще предоставя по-задълбочени механистични прозрения, които ускоряват изследванията при висшите еукариоти. Изследванията върху червеи и мухи също ще бъдат важни, за да се постигне разбиране на молекулярната биология на гладуването при дрожди и бозайници.
Пости и имитиращи диети при болести на гризачи и дълголетие
Има две основни форми на гладуване, изучавани при модели на гризачи: интермитентно гладуване (IF), което обикновено се отнася само до вода или много нискокалоричен период, продължаващ по-малко от 24 часа и последван от нормален период на хранене от един до два дни, или периодичен гладуване (PF), което продължава 2 или повече дни и се отделя от следващия цикъл с поне една седмица (Longo and Mattson, 2014).
Ролята на IF при стареенето и болестите при гризачите все още е противоречива. При плъхове множество проучвания показват, че всеки ден гладуването последователно удължава продължителността на живота и че този ефект е по-изразен от този, причинен от гладуването за 1 ден на 3-4 дни (Carlson and Hoelzel, 1946; Kendrick, 1973). Въпреки това проучвания с мишки, използващи различни генетични среди, показват, че IF не може да има ефект върху средната продължителност на живота и дори може да намали продължителността на живота, когато се започне на 10-месечна възраст (Goodrick et al., 1990). Дори когато IF беше започнат на 1,5 месеца, ефектите върху дълголетието бяха незначителни и несъвместими (Goodrick et al., 1990).
Въпреки това, при гризачите IF подобрява когнитивните показатели (Fontán-Lozano et al., 2007; Singh et al., 2012), което може да бъде причинено отчасти от неговия стимулиращ ефект върху синаптичната пластичност (Lee et al., 2006) и също така подобрява инсулинова чувствителност и намалява кръвното налягане и сърдечната честота (Mager et al., 2006; Wan et al., 2003).
Седем месеца цикли на ящур също доведоха до подобрения в батерията от поведенчески тестове, вариращи от двигателна координация, до дългосрочна и краткосрочна памет в сравнение с мишки на стандартната контролна диета (Фигура 2) (Brandhorst et al., 2015). Ефектът на ящура върху неврогенезата, вероятно чрез регулиране надолу на IGF-1 и PKA сигнализиране, показва, че генерирането на нови и функционални неврони може да допринесе за повишената когнитивна ефективност при мишки, третирани с ящур, в съгласие с ефектите PF, IGF-1 и PKA върху хемопоетичната регенерация (Cheng et al., 2014).
Не е изненадващо, че циклите на ящур, започнати на 16-месечна възраст, са причинили 18% увеличение на 75% точката на оцеляване и 11% увеличение на средната продължителност на живота. Забележително е, че след 24-месечна възраст мишките се оказаха отрицателно засегнати от 4-дневната ящур, но не и от идентична ящур, намалена до 3 дни, в съгласие с резултатите за ограничаване на протеините, което показва, че младите, но не и възрастните мишки могат да поддържат нормално тегло когато приемът на протеин допринася за по-малко от 7% от общия прием на калории (Фигура 2) (Levine et al., 2014).
IF и PF в превенцията и лечението на хронични заболявания при хората
АКО и болести
IF може да има широк спектър от ефекти върху метаболитни маркери и рискови фактори или заболявания, включително телесни мазнини, кръвно налягане. При субекти с наднормено тегло, които консумират приблизително 500 kcalorie, но относително високо протеинова диета в продължение на 2 дни в седмицата в продължение на 6 месеца, коремните мазнини намаляват кръвното налягане намалява и чувствителността към инсулин се увеличава (Harvie et al., 2011). Подобни резултати бяха получени след 2-3 седмици на всеки ден на гладно (Halberg et al., 2005; Heilbronn et al., 2005). Преглед на констатациите за всички релевантни клинични проучвания, оценяващи както хронично ограничаване на калориите в диапазона 20-50% (CR), така и периодично гладуване, заключава, че CR е по-добър в причиняването на загуба на телесно тегло в сравнение с IF, но и двете интервенции имат сходни ефекти върху намаляването на висцералните мазнини, инсулин и инсулинова резистентност (Barnosky et al., 2014). Освен това беше направено заключението, че нито CR, нито IF имат клинично значими ефекти върху нивата на глюкозата, което увеличава вероятността и двете интервенции да имат ограничено приложение в превенцията и лечението на метаболитен синдром и диабет, особено като се имат предвид трудностите при постигане на съответствие с някоя от двете тежки и хронични CR или тежки ограничения, ограничаващи консумацията на калории до 500–600 kcal на ден между 9 и 15 пъти на месец, средно.
АКО гладуването може също да има някои ефекти върху възпалителните заболявания, тъй като 2-месечно гладуване с алтернативен ден доведе до значително намаляване на възпалителните маркери при пациенти, страдащи от астма (Johnson et al., 2007).
ПФ и болести
Едно от добре утвърдените клинични приложения на PF е при лечението на ревматоиден артрит (RA). Четири различни контролирани проучвания показват, че периодите на гладно с продължителност от една до три седмици намаляват симптомите на RA, въпреки че тези ефекти се обръщат чрез връщане към нормалната диета, освен ако PF не е последвана от вегетарианска диета (Müller et al., 2001).
PF може също да бъде от полза при лечението на хипертония. В проучване, 13 дни вода само на гладно намалява систолното кръвно налягане под 120 при 82% от пациентите с лека хипертония (Goldhamer et al., 2002). PB остава значително по-нисък, след като субектите са се върнали към нормалната си диета в продължение на 6 дни. В друго проучване, 10–11 дни на гладно намаляват систоличното кръвно налягане на пациентите с хипертония с 37–60 mm, но това проучване не проследява пациентите, след като те се върнат към нормалната си диета (Goldhamer et al., 2001). В обобщение, както IF, така и PF имат потенциални приложения за възпалителни и сърдечно-съдови заболявания, но са необходими допълнителни, по-големи и рандомизирани проучвания, преди тези стратегии да могат да бъдат интегрирани в стандарта на грижа от лекарите.
Оптимална методология и обществено здраве
Периодичните диети, имитиращи гладуване (ящури)
Няколко основни пречки могат да бъдат отговорни за много ограничения принос на PF към стандартната медицинска практика: 1) липсата или предклиничните и клинични данни, подкрепящи специфични и постоянни ефекти на гладуването върху профилактиката и лечението на заболявания, и включените механизми, 2 ) опасенията за безопасност, свързани с приемането само на консумация на вода или често приеманите диети с много ниско съдържание на калории (около 200 kcal) извън клиниката, 3) трудностите, свързани със спазването на тези екстремни диети. Въпреки че има вероятност стотици хиляди хора да се подлагат на някаква форма на PF всяка година, здравните специалисти настоятелно препоръчват само водни или подобни интервенции на гладно да бъдат ограничени до специализирани клиники, работещи с медицински персонал.
Ящурите са разработени първо за мишки и в крайна сметка за хора, за да се справят с тези опасения и да помогнат да се идентифицират както положителните, така и потенциално отрицателните ефекти на гладуването, като същевременно се сведат до минимум опасенията за безопасност и съответствие. Ящурът, който първоначално е разработен да замести водата само на гладно при мишки, сега е тестван при хора. Човешката ящур се състои от 5-дневен режим, осигуряващ между 725 и 1090 ккалории, със съдържание на макроелементи, избрано да имитира вода само на гладно, но съдържание на микроелементи, насочено към максимално подхранване. 19 субекта бяха рандомизирани, за да преминат 3 цикъла месечно ящур, докато допълнителни 19 субекти бяха рандомизирани на контролна диета. След 3 цикъла на ящура средният докладван страничен ефект, причинен от диетата, е много нисък и под „лек“ (Фигура. 3). Компонентите на циркадния часовник се свързват с транскрипционни регулаторни региони на хиляди гени и задвижват тяхната ритмична транскрипция до голяма степен специфичен за тъканите начин (Koike et al., 2012; Vollmers et al., 2012). Пътищата mTOR и AMPK също модулират дейностите на протеините надолу по веригата, включително регулаторите на транскрипция CREB, PPAR, FOXO, Hsf1, HNF и PGC1 (Inoki et al., 2011). Регулаторните региони на повечето гени обаче са насочени от множество транскрипционни фактори (Hager et al., 2009). Съответно много транскрипти, регулирани по циркаден начин, които са мишени надолу по веригата на компонентите на часовника, също са насочени от транскрипционни регулатори, чиято дейност се модулира чрез хранене и гладуване (Bugge et al., 2012; Feng et al., 2011; Koike et al., 2012; Vollmers et al., 2009). Подобна конвергентна регулация от циркаден часовник и сензори за хранене/гладуване предлагат адаптивни предимства за организма.
При липса на прием на храна, самоподдържащият се циркаден осцилатор задвижва елементарно трептене на шепа преписи в черния дроб (Фигура 3), като по този начин предлага изпреварващо шофиране за хранене или гладуване. Ежедневните ритми на хранене/гладуване задвижват сигнални пътища, които взаимодействат с циркадния осцилатор, за да увеличат устойчивостта или разликите между пиковете и нивата на тези транскрипционни трептения. След това тези преписи посредничат анаболни и катаболни процеси, които са подходящи за специфични фази на цикъла на хранене/гладно. При липса на функционален циркаден часовник, пътищата, задвижвани от хранене и гладуване, могат да предизвикат някои трептения в транскрипцията (Vollmers et al., 2009), метаболитите надолу по веригата (Adamovich et al., 2014) и дори чревната микробиота (Thaiss et ал., 2014), но тези сигнали не могат напълно да компенсират загубата на циркадния часовник. Следователно синергичните взаимодействия между циркадния осцилатор и сигналите за хранене/гладуване гарантират, че анаболните и катаболните типове метаболизъм са координирано регулирани в хармония с активността/цикъла на почивка на животното.
Епидемиология на циркадни смущения
И накрая, възрастта също е риск за овлажняване на ендогенния циркаден часовник. Фибробластите от по-възрастни индивиди имат овлажнен циркаден часовник и част от това овлажняване се медиира от серумни фактори (Pagani et al., 2011). С увеличеното човешко дълголетие, свързаното с възрастта овлажняване на циркадния часовник се превръща в риск за хронично циркадно нарушаване.
Причинният ефект на работната смяна върху метаболитните заболявания все повече се тества както при животни, така и при хора при контролирани лабораторни условия. Симулираната работа през нощна смяна намалява ежедневните енергийни разходи при доброволци (от
12–16%) и в отговор на хранене (McHill et al., 2014). Това е свързано с намалени нива на хормоните на ситост лептин и пептид YY. Хората, подложени на денонощно изравняване в продължение на 10 дни, развиват повишена глюкоза след прандиал, повишен инсулин (инсулинова резистентност) и повишено средно артериално налягане (Scheer et al., 2009).
Клинични приложения
Предимства на TRF при гризачи и дрозофила. TRF от 8–12 часа през нощта при гризачи или 12 часа през деня за дрозофила придава плейотропни ползи, които включват множество органи. Ползите и посоката на промяна, придавани от TRF по отношение на храненето ad lib на подобна обезогенна диета или диета с високо съдържание на захар.
Възможността хората да приемат протокол TRF показа някои обещания. Същото проучване (Gill and Panda, 2015) тества дали промяната на продължителността на ежедневното хранене, като позволява на участниците да ядат дневния си калориен прием в рамките на самостоятелно избран период от 10-11 часа, би донесла ползи за здравето на хората с наднормено тегло. Осем участници с наднормено тегло изядоха целия си дневен прием на калории в рамките на самостоятелно избран прозорец от 10-11 часа. За половината от тях прозорецът за хранене приключи след 20:00, за да могат да вечерят със семейството си. Въпреки това, за разлика от гризачите, които консумират същия брой калории, когато се налага TRF от 8–15 часа, намаляването на продължителността на хранене при хората също намалява дневния им калориен прием с до 20% (част от това намаление идва от намаляване на алкохола и закуските късно през нощта. ). Те загубиха до 4% телесно тегло за 16 седмици и запазиха тази загуба на тегло до 1 година. Те също съобщават за подобрен сън през нощта и повишена бдителност през деня.
Допълнителни проучвания също предполагат, че TRF носи потенциални ползи за човешкото здраве. В ретроспективно проучване, изследващо самоотчетената продължителност на гладно през нощта и честота на рак на гърдата, продължителен период на гладно през нощта от ≥13 часа корелира с намален риск от рак на гърдата (Marinac et al., 2015a; Marinac et al., 2015b). Въпреки че тези доклади показват осъществимост на TRF като намеса или доброволно приемане на TRF като начин на живот, по-фокусирани проучвания за въздействието на TRF както за профилактика, така и за прогноза на хронични заболявания са оправдани. Почти 50% от възрастните в САЩ имат съществуващо хронично заболяване, за което може да приемат лекарства или добавки. Проучванията на циркадните транскриптоми и протеоми са идентифицирали няколко протеина, които са целта или че абсорбцията на въздействието и клирънсът на лекарствата също са под циркадна модулация (Neufeld-Cohen et al., 2016; Robles et al., 2014; Zhang et al., 2014) . Тъй като начинът на хранене определя фазите на циркадните ритми в периферните органи, времето на приемане на лекарствата спрямо времето на приема на храна вероятно ще повлияе на прогнозата.
Хранене, специфично за възрастта
Заключения
- Различен отговор на промяната на телесното тегло според кетонурията след гладуване при здравословно затлъстяване
- Зелен чай Най-доброто време за пиене на здравословна напитка за бързи резултати при отслабване
- Пийте вода в точното време, за да останете здрави
- Хранене на тийнейджъра със здравословно хранене за тийнейджъри
- Можете ли да предозирате екстракт от зелен чай, здравословно хранене SF Gate