Тази статия е в знак на почит към д-р Дъглас Колман, гигант в областта на изследванията на затлъстяването, който почина на 16 април 2014 г. През 70-те години Колман проведе елегантни изследвания в лабораторията Джаксън в Бар Харбър, Мейн, което го доведе до предлагат съществуването на циркулиращ фактор, свързан с патогенезата на затлъстяването (1, 2). Неговите експерименти с кръвно кръвообращение (парабиоза) при генетично затлъстели мишки са в основата на сегашния възглед за мастната тъкан като ендокринен орган, свързан с регулирането на храненето и телесното тегло.
Глобална криза на затлъстяването
В световен мащаб над 1,4 милиарда възрастни на възраст над 20 години и 40 милиона деца на възраст под 5 години са с наднормено тегло (3). Наднорменото тегло и затлъстяването се характеризират с прекомерно натрупване на мазнини. Индексът на телесна маса (ИТМ), определен като тегло на човек в килограми, разделен на квадрата на височината в метри, често се използва като мярка за затлъстяване. Световната здравна организация определя наднорменото тегло при възрастни като ИТМ ≥25, а затлъстяването като ИТМ ≥30. Разпространението на затлъстяването се е увеличило повече от два пъти в повечето части на света от 1980 г. насам (4). През 2008 г. 35% от възрастните в цял свят са с наднормено тегло и 11% са с наднормено тегло (3). Сред тях> 200 милиона мъже и близо 300 милиона жени са били със затлъстяване. Повече от една трета от възрастните в САЩ (34,9%) са със затлъстяване (5). Чернокожите, които не са испанци, имат най-високи нива на затлъстяване, коригирани за възрастта (47,8%), следвани от испанците (42,5%), неиспанските бели (32,6%) и неиспанските азиатци (10,8%) (5). Затлъстяването също е по-високо сред възрастните на средна възраст, на възраст от 40 до 59 години (39,5%), отколкото сред по-младите хора на възраст от 20 до 39 години (30,3%) или възрастни на 60 години или повече (35,4%) (5).
Понастоящем много развиващи се страни са изправени пред двойна тежест на инфекциозните заболявания и недохранването и нарастването на затлъстяването и други рискови фактори за неинфекциозни заболявания. Децата в развиващите се страни са уязвими към недохранване и също са изложени на недохранване от храни с високо съдържание на мазнини и захар и храни с ниско съдържание на микроелементи, които обикновено са по-евтини, но имат много лошо хранително качество. Тенденцията на „хранителен преход“ доведе до значително увеличаване на детското затлъстяване в развиващите се страни и представлява големи здравни и социално-икономически заплахи в световен мащаб. Всъщност 65% от населението на света живее в страни, където наднорменото тегло и затлъстяването причиняват повече смъртни случаи, отколкото поднормено тегло (3).
Тези мрачни статистически данни подтикнаха правителствата и организациите да разработят превантивни стратегии, фокусирани върху образованието на индивидите и общностите, за да направят по-здравословен избор на храни, популяризиране на достъпни и достъпни здравословни храни за всички, особено на най-бедните, и промени във физическата инфраструктура и работното място, за да ограничат заседнал начин на живот. Важно е, че епидемията от затлъстяване също стимулира изследователските усилия за разбиране на биологичните механизми и за подобряване и разработване на нови медицински и хирургични терапии.
Патогенеза на затлъстяването: от хипоталамусни лезии до лептин
Тази година се навършват 20 години от откриването на лептин, хормон, който играе критична роля в регулирането на апетита и телесното тегло (6). Доказателствата за съществуването на физиологични механизми за регулиране на телесното тегло датират от класическите изследвания преди няколко десетилетия (7). Въз основа на експерименти с лезии на хипоталамус на плъхове се предполага, че в медиалния хипоталамус съществува „център за ситост“, докато в страничния хипоталамус съществува „център за хранене“. Унищожаването на вентромедиалното хипоталамусно ядро (VMH) доведе до ненаситно хранене и масивно наддаване на тегло, докато разрушаването на страничния хипоталамус доведе до глад и загуба на тегло. Когато затлъстелите плъхове, лезирани от VMH, са били хирургично присъединени (парабиоза) с нормални плъхове през техните подкожни тъкани, което позволява бавен обмен на кръвоносните фактори, нормалните плъхове ядат по-малко храна и отслабват. Следователно беше постулирано, че затлъстелите плъхове, лезирани с VMH, не реагират на периферен фактор, който инхибира храненето, и че те свръхпродуцират фактор, който преминава в циркулацията на нормалните плъхове, за да потисне храненето и да намали телесното тегло.
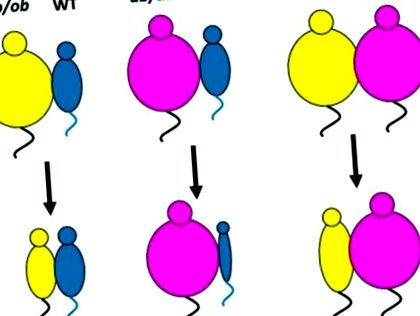
Експерименти с парабиоза при мишки. Семенните изследвания на Coleman показват, че парабиозата (кръстосана циркулация) на ob/ob и нормални WT мишки води до загуба на тегло при ob/ob мишки. За разлика от това, парабиозата на db/db и WT води до загуба на тегло при WT. Парабиозата на db/db и ob/ob мишки води до загуба на тегло при ob/ob мишки. Следователно се постулира, че ob locus произвежда циркулиращ фактор, който инхибира приема на храна, а db локусът кодира рецептора за циркулиращия фактор на ситост.
Откритието на лептин предостави мощни молекулярни инструменти за изучаване на невронни вериги, които контролират енергийния баланс (16, 17). Лептинът се транспортира в мозъка и действа в хипоталамуса, за да регулира храненето, разхода на енергия, невроендокринната ос и метаболизма (Фигура 2). Нетният ефект на лептина е да инхибира приема на храна и да намали телесното тегло. Лептинът също така контролира хедоничните аспекти на приема на храна и взаимодейства със сигнали от червата, мозъчния ствол и други мозъчни области (16, 17). Откритието на лептин стимулира изследователските усилия за разбиране на ролята на други хормони, получени от мастна тъкан (адипокини), невропептиди, участващи в регулирането на храненето и метаболизма, взаимодействието на генетични и екологични фактори при затлъстяването и терапевтичните цели на затлъстяването и свързаните с него заболявания.
Хипоталамусни невронални мишени на лептин. Лептинът инхибира храненето и увеличава енергийните разходи чрез директно потискане на невропептида Y (NPY) и увеличаване на проопиомеланокортина (POMC). Невроните в дъгообразното ядро, експресиращи тези пептиди, се проектират към паравентрикуларното ядро и страничната хипоталамусна област, което води до увеличаване на CRH и TRH и намаляване на меланин-концентриращия хормон (MCH) и орексините. Нетният ефект на лептина е да потисне апетита, да намали теглото и да засили окисляването на мастните киселини и чувствителността към инсулин в периферните органи. AGRP, свързан с Agouti пептид; LRb, дълъг лептинов рецептор; MC4R, рецептор за меланокортин 4; MSH, меланин-стимулиращ хормон; TG, триглицериди.
Както при мишките, вроденият лептинов дефицит или дефектните лептинови рецептори причиняват преяждане и бързо настъпване на затлъстяване при хората (18, 19). Лечението с рекомбинантен лептин причинява драстична загуба на тегло при пациенти с редки мутации със загуба на функция в гена LEP (23, 24). Въпреки това, често срещаните форми на затлъстяване поради преяждане и липса на физически упражнения водят до повишени нива на лептин и лош отговор на лечение с лептин, което предполага лептинова резистентност (20, 25). Медиаторите на лептинова резистентност, напр. Супресор на цитокиновата сигнализация 3 (SOC3) и тирозин фосфатазата PTP1b, са свързани с индуцирано от диетата затлъстяване при мишки (16, 17), но дали тези молекули не са регулирани при често срещани форми на човешко затлъстяване е неизвестно.
Поуки?
Въпреки че лептинът е кръстен заради ефекта си на затлъстяване при мишки, доказателствата показват, че основната физиологична роля на лептина е да сигнализира за мозъчен дефицит и да предизвика хормонални, метаболитни и поведенчески реакции за възстановяване на енергийните запаси (21, 22). Нивата на лептин бързо падат по време на гладуване и медиират потискането на репродукцията, хормона на щитовидната жлеза и имунната функция (21). Тези дефекти се наблюдават и при ob/ob мишки с тотален дефицит на лептин. Частичният дефицит на лептин води до хипогонадизъм при гладуване, хипоталамусна аменорея и липодистрофия при хората (26). По този начин, лептинът има широк диапазон на реакция на дозата при медииране на отговора на глада при спадане на нивата на лептин, както и ограничаване на прехранването с повишаване на нивата (20, 22). Възможно е резистентността към лептин да дава еволюционно предимство, като насърчава съхранението на енергия срещу заплахата от глад.
Лептинът има безброй ефекти върху глюкозния и липидния метаболизъм, развитието на мозъка, хемопоезата, възпалението, костната биология, клетъчния растеж и диференциация и други биологични системи, освен енергийната хомеостаза (7, 16). Това често се случва в ендокринологията, когато хормонът е наименуван първоначално за предполагаема функция и се установи по-късно, че оказва множество ефекти. Като пример, инсулинът има основна роля в регулирането на нивата на глюкозата, но това не е единствената функция на инсулина при нормални или патологични условия. Инсулинът има различни ефекти върху липидния и белтъчния метаболизъм, клетъчния растеж и диференциация и други системи.
Затлъстяването е силно сложно нарушение на енергийния метаболизъм, което завършва с прекомерно натрупване на мазнини в мастните, черния дроб, скелетните мускули и други органи. Затлъстяването се влияе от генетични и екологични фактори, особено от диетата и физическите упражнения. Следователно проучванията върху патогенезата на затлъстяването и откриването на лекарства при животни и клетки трябва да вземат предвид взаимодействията на сложни процеси вместо прости линейни пътища. Ролята на генетиката в човешкото затлъстяване беше призната в изследвания на близнаци преди много десетилетия (27). Откриването на мутации, свързани с човешкото затлъстяване, освети нашите знания (28). Генетичните локуси, идентифицирани в проучвания за асоцииране в целия геном, са свързани със затлъстяването; обаче, общата вариация на признаците, обяснена от тези асоциирани локуси, е много малка, което предполага, че по-голямата част от фамилната агрегация на затлъстяването може да бъде повлияна от модулацията на епигенетичните процеси в околната среда. Въздействието на вътрематочните и постнаталните фактори на околната среда върху програмирането на метаболизма е вълнуваща област за изследване.
Друга област, която се нуждае от подобрение, е оценката на телесния състав. Нашата настояща дефиниция за затлъстяване въз основа на прагова стойност на ИТМ игнорира моделите на разпределение на теглото и мазнините в популацията. ИТМ не е точна мярка за мазнини, не отчита чистата маса и местоположението на мазнините и не отчита расовите/етническите и половите разлики в съдържанието и разпределението на мазнините. Висцералните мазнини и мускулната маса са по-добри предиктори за инсулинова резистентност, диабет и други метаболитни нарушения. Следователно има спешна нужда от точни и достъпни методи за оценка на телесния състав в клинични и популационни проучвания (29).
Нашите познания за механизмите, свързващи затлъстяването с развитието на диабет, сърдечно-съдови заболявания, рак и други заболявания, свързани със затлъстяването, са елементарни. Добре известно е, че затлъстяването е свързано с инсулинова резистентност и активиране на вродения имунитет, но дали те са причинно свързани с редица заболявания, свързани със затлъстяването, като диабет, рак, безплодие и остеоартрит (30)? Можем ли да използваме информация за адипокини, цитокини и други биомаркери за диагностични цели при затлъстяване или за разработването на специфични лекарства за заболявания, свързани със затлъстяването?
Въпреки огромния напредък в разбирането на молекулярните механизми, свързани със загубата на тегло, настоящите диетични и медицински интервенции често не успяват да поддържат дългосрочна загуба на тегло (31). Стомашната байпас хирургия, която е най-ефективното лечение на болестното затлъстяване, бързо обръща диабета при липса на значителна загуба на тегло (32). Тези открития изискват преосмисляне на лечението на затлъстяването и свързаните с него заболявания. Нуждаем се от нови стратегии за превенция и лечение, базирани на по-добро разбиране на биохимията на макронутриентите и микроелементите, енергийния метаболизъм, въздействието на начина на живот и факторите на околната среда върху хомеостатичните механизми, потенциалните роли на ендокринните разрушители и чревната микробиота върху метаболизма и множество пътища, свързващи генетиката и околната среда.
Независимо от тези досадни проблеми, може да се каже, че сме постигнали огромни крачки в разбирането на метаболизма и затлъстяването. Има широк спектър от вълнуващи възможности за изследвания, обхващащи клетъчни модели, генетично модифицирани животински модели, пациенти с различни генетични дефекти и популационни проучвания. Молекулярните инструменти и техники са от съществено значение за разгадаването на тайните на енергийния метаболизъм, затлъстяването и патогенезата на заболяванията. Молекулярната ендокринология ще продължи да играе решаваща роля, като предоставя на основните и транслационни изследователски общности широки възможности за разпространение на тяхната работа.
Благодарности
Тази работа беше подкрепена от Националния здравен институт (грант P01-DK049210; P30-DK19525).
Резюме на разкриването: Авторът няма какво да разкрива.
- Детското затлъстяване, свързано с лоши признаци на здравето на сърцето на 11-12 години Изследвания на Мърдок за деца
- Икономически анализ на училищна програма за превенция на затлъстяването - Wang - 2003 - Изследване на затлъстяването -
- Влошаване Стигматизацията на затлъстелите деца - Latner - 2003 - Изследване на затлъстяването - Wiley
- Членове на редакционния съвет - вестник за терапия за затлъстяване и отслабване
- Детски затлъстяване Демонстрационен проект Демонстрационен проект Методи за оценка между сайтове Детско затлъстяване