Всеки от многото фактори, чрез които начинът на живот и околната среда влияят върху енергийния баланс, взаимодейства със специфични набори от гени за податливост, чиито вариации определят физиологичното въздействие на конкретния фактор. Инициирането и поддържането на поведението при поглъщане се определя едновременно от метаболитни и неметаболитни фактори. Сред последните, екологичните сигнали, както и наградите, когнитивните и емоционалните фактори играят важна роля, особено в приема на храна от човека в съвременния свят.
ОПРЕДЕЛЕНИЕ НА ЕНЕРГЕТИЧНИЯ БАЛАНС
Енергийният баланс е разликата между енергията, въведена с храната, и консумираната енергия. Нуждата от енергия е разделена на:
- Базален метаболизъм;
- Физическа дейност;
- Термогенеза (насочена към поддържане на телесната температура и намалена от глобалното затопляне)):
- Динамична специфична активност на храните;
- Термогенезата не е свързана с физически упражнения
- Потребността от енергия може да бъде променена поради:
- Промени в работата на дихателната верига;
- Промени в изпълнението на физическата работа.
ПРИЕМАНЕ НА ХРАНА
Необходимостта от прием на храна се регулира на хипоталамусно ниво, за да се отговори на сигналите за глад за чувство на глад и ситост, които са резултат от интеграция на ниво различен кортикален сигнал от различни източници и които имат за задача да регулират приема на храна, с мрежа от различни химически медиатори и нервни. Беше отбелязано, че при повечето видове бозайници (както и при хората, ако живеете в дивата природа), има тенденция да има пряка връзка между количеството консумирана храна и количеството работа, необходимо за получаване. В цивилизования този прост доклад е загубен, но все още е верен за ловеца и фермера на човека.
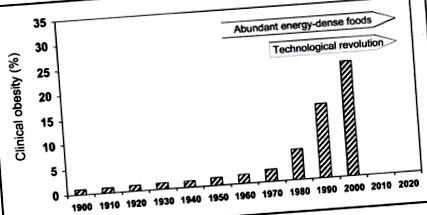
Коя е ролята на глобалното затопляне за затлъстяването?
Мониторинг на приема на храна.
ХОМЕОСТАТИЧНО РЕГУЛИРАНЕ НА ЕНЕРГИЙНИЯ БАЛАНС.
Бъдещи насоки в контрола на теглото
Отговорността за контролиране на енергийната хомеостаза се споделя между няколко мозъчни области, както се доказва при човека от въздействието върху приема на храна на фактори като зрението и миризмата на храна, броя и удобството на придружаващите ястия, както и размера и крайното място за почивка на сметката за ресторанта (Hill & Peters, 1998).
Стомашно-чревният тракт и черният дроб участват в краткосрочната регулация на храненето. Различни сигнали се движат във вагусните нервни влакна от рецептори за разтягане, а хеморецепторите, активирани от наличието на хранителни вещества в стомаха и проксималните тънки черва, участват в прекратяването на храненето. Хранителните вещества, пристигащи през порталната вена, също могат да задействат вагусни аферентни сигнали от черния дроб. Глюкозата може да модулира приема на храна, като въздейства на глюкозо-реагиращите неврони в ЦНС. Кетоните изглежда намаляват апетита. В отговор на хранителна стимулация проксималното черво освобождава холецистокинин (CCK), който достига до черния дроб през порталната вена и ЦНС чрез системната циркулация; CCK може да действа върху CCK -A рецепторите и на двете места, за да инхибира приема на храна. Ендокринните L клетки в крайния тънко черво (илеум) освобождават глюкагоноподобен пептид-1 (GLP-1), който инхибира храненето, най-вероятно на чернодробно място или чрез инхибиране на изпразването на стомаха. Краткосрочните сигнали сами по себе си не водят до трайни промени в приема на енергия и телесното затлъстяване.
ГЛЮКОЗА: Хипогликемия или инхибиране на метаболизма на глюкозата с глюкозния аналог 2 дезокси-D-глюкоза увеличава приема на храна при животните и увеличава усещанията за глад и приема на храна при хората ("Oomura и колеги").
МАЗНИНИ (ТРИГЛИЦЕРИДИ, МАСТНИ КИСЕЛИНИ И АПОЛИПОПРОТЕИНИ):
Интравенозната инфузия на липидни субстрати като Intralipid, заедно с хепарин за освобождаване на липопротеинова липаза и хидролизиране на триглицеридите до мастни киселини и глицерол, намалява приема на храна при павианите. Тези данни предполагат, че увеличаването на циркулиращите липиди, при липса на абсорбция на GI, регулира храненето.
Подобно на инхибирането на метаболизма на глюкозата, инхибирането на метаболизма на липидите увеличава експресията на орексигеновия невропептид меланин, концентриращ хормон в страничния хипоталамус. Въпреки това, за разлика от глюкопривацията, той не увеличава експресията на невропептид Y или свързан с агюти пептид в дъгообразното ядро, и двете от които са орексигени. Друг свързан с липидите продукт, потенциално участващ в регулирането на приема на храна, е аполипопротеинът, ApoAIV. Производството на Apo AIV в червата се стимулира от абсорбцията на мазнини, а приложението на Apo AIV инхибира приема на храна. Този аполипопротеин също се произвежда в хипоталамуса и Apo AIV от централен произход може също да има роля в регулирането на приема на храна.
МЕТАБОЛИТИ: Лактатът, пируватът и кетоните инхибират храненето при животните. Концентрациите на циркулиращ лактат след хранене се увеличават пропорционално на съдържанието на въглехидрати в храната и следователно биха могли да допринесат за краткосрочното инхибиране на приема на храна по време на консумация на въглехидрати.
Дългосрочни сигнали, регулиращи приема на храна и енергийна хомеостаза.
Инсулинът и лептинът са двата най-важни дългосрочни регулатора на приема на храна и енергийния баланс. И инсулинът, и лептинът действат в ЦНС, за да инхибират приема на храна и да увеличат енергийните разходи, най-вероятно чрез активиране на симпатиковата нервна система.
Дългосрочните сигнали взаимодействат с краткосрочните сигнали в регулирането на енергийната хомеостаза и изглежда създават чувствителност към ефектите на ситост, произвеждащи краткосрочен сигнал като CCK.
Лептин, лептинови рецептори и неговите сигнални пътища надолу по веригата.
Лептинът увеличава консумацията на мастни киселини чрез окисляване в скелетните мускули. Освен това показват, че лептинът активира ензим - протеин киназа на 5 'монофосфат или AMPK - в скелетните мускули. В клетките крехкият баланс контролира дали мастните киселини се транспортират в митохондриите и се метаболизират или съхраняват в цитоплазмата като триглицериди. Този баланс се регулира главно от малонил CoA, мастна киселина, която се генерира dall'acetil-CoA карбоксилаза (ACC). Малонил CoA инхибира транспорта на мастни киселини в митохондриите, като по този начин предотвратява метаболизма. AMPK фосфорилираният ACC, inattivandolo. Чрез активиране на dell'AMPK в мускулите, лептинът инхибира синтеза на малонил CoA и премества баланса към окисляването на мастните киселини и не позволява съхранението на мазнини. Тези ефекти са подобни на тези визи при мишки, при които гените, кодиращи АСС, са били извадени от употреба.
Обестатин.
Обестатинът, получен от същия полипептиден прекурсор като грелин, но който по-скоро потиска приема на храна, също подобрява обучението и паметта и в допълнение предизвиква анксиолитичен ефект, както се посочва от увеличения процент на влизане с отворени ръце в повишения плюс лабиринт. Съществува и значителна литература, показваща, че лептинът може да модулира възбудимостта на хипокампалните неврони. Неговите дозозависими диференциални ефекти върху дългосрочното потенциране и депресия предполагат, че лептинът може или да улесни, или да потисне функциите на паметта .
Грелин.
- Приемът на макаронени изделия е свързан с по-добри диетични резултати 2020-01-27 Новини за хранителния бизнес
- Възстановяване на приема на храна след гастректомия за рак на стомаха въз основа на широкомащабен рак на стомаха
- Естрадиолът и генистеинът намаляват приема на храна при мъжки и женски котки с наднормено тегло след гонадектомия -
- Пурини; Факти за регулиране на храните
- Предпочитание на солена храна и прием и риск от рак на стомаха Изследването JACC