Резюме
Пиковата костна маса при възрастни е свързана с теглото при раждане, което предполага, че тя може да бъде повлияна от модела на растеж на плода. Малките за гестационна възраст (SGA) новородени имат по-ниско съдържание на костни минерали (BMC), но какво ще кажете за новородените, адаптирани за гестационна възраст (AGA) с ограничение на растежа на плода? Целта на проучването е да се определи съответната роля на теглото при раждане и модела на растеж на плода върху BMC. Включени са доносени новородени от SGA високорискови бременности (н = 185). Изчислените процентили на теглото на плода се измерват ежемесечно от средата на бременността до раждането и ограниченият растеж на плода (FGR) се определя като загуба с повече от 20 процентила. BMC се измерва при раждането, като се използва двойна рентгенова абсорбциометрия. Новородените са SGA (н = 56) или AGA (н = 129). Новородени с FGR (н = 111) са AGA (н = 71) или SGA (н = 41). BMC е значително по-нисък в SGA от AGA (1,48 ± 0,02 срещу. 1,87 ± 0,04 g/cm) и по-ниска, когато FGR, независимо от теглото при раждане (1,66 g/cm ± 0,03 срещу. 1,89 g ± 0,05). При многовариантния анализ FGR и SGA са значими и независими предиктори за нисък BMC. В заключение, моделът на растеж на плода засяга BMC не само при SGA бебета, но и когато теглото при раждане се поддържа в нормални граници.
МЕТОДИ
Субекти.
Проучваната популация се състои от 185 новородени, включени между май 2004 г. и май 2007 г. в кохортата CASyMIR, френска перспективна кохорта, изследваща метаболитните последици от раждането на SGA в ранна детска възраст. Децата са родени от бели жени, вербувани през първия или втория триместър на бременността в майчинството на болница „Робърт Дебре“ в Париж и считани за висок риск от SGA бременност. Критериите за включване са били съществуваща хипертония, пушене на повече от пет цигари на ден, анамнеза за SGA при предишна бременност или при двамата родители, история на индуцирано от бременността хипертонично разстройство, майчин ръст по-малък от 152 cm, съответстващ на 2 SD за френски жени, маточни малформации, необичайни маточни или пъпни маточни артерии Доплер и малък размер на плода при ултразвуково изследване през втория триместър. Датата на зачеването се определя от ултразвуковото изследване, проведено в 12 седмици на бременността. 1
Теглото при раждане на новородените се записва в рамките на 10 g от акушерките, като се използва електронна везна. Дължината на раждането се измерва на стандартна дъска за измерване на бебета в рамките на милиметър. Двойно рентгеново абсорбциометрично сканиране е направено при всички новородени на третия ден от живота. Протоколът за изследване е одобрен от етичния комитет на Париж - Медицинското училище в Сейнт Луис (Университет Париж 7) и всички родители са дали писмено информирано съгласие.
Оценка на растежа на плода.
Измерване на телесния състав.
Статистически анализ.
Всички анализи бяха извършени с помощта на софтуера JMP версия 5.1 (SAS Inc. Meylan, Франция). Данните са дадени като средно ± SD. За сравнение на пропорциите между групите е използван тест с хи-квадрат. Непрекъснатите променливи бяха сравнени, като се използва дисперсионен анализ в едномерни модели. За по-нататъшна оценка на ефекта от теглото при раждане и ограничаването на растежа на плода върху BMC, е изграден многовариатен линеен модел, включващ гестационна възраст, пол, пушене на майката и сезонност при раждане като ковариати.
РЕЗУЛТАТИ
Минерално съдържание, свързано с теглото при раждане и растежа на плода.
Характеристиките на субектите са показани в таблица 1. Сто осемдесет и пет доносени новородени са включени в това проучване (92 момчета и 93 момичета). В тази популация 56 бебета са класифицирани като SGA и 129 като AGA. Използвайки нашите критерии, 73 новородени са имали нормален или субнормален растеж. За разлика от това, 112 новородени са имали FGR. Гестационната възраст и пол не се различават между трите групи, докато цезаровото сечение е по-често в групата на FGR, отколкото в групите с IG и NG (28,6% срещу. 18,7% и 10,2%, съответно стр = 0,0028). FGR присъства при повечето новородени от SGA (77%) и при 55% от пациентите с AGA. И при SGA, и при AGA основните рискови фактори за ограничаване на растежа на плода са тютюнопушенето при майката, необичайни доплерови измервания и анамнеза за SGA при предишни бременности.
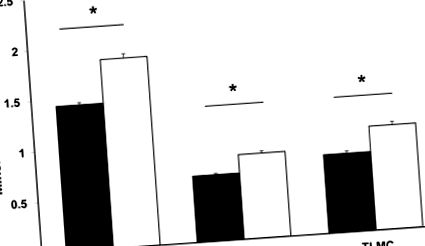
Фигура 1 показва BMC според теглото при раждане. Както се очаква, общата BMC е по-ниска при SGA новородени, отколкото при AGA новородени (1,48 ± 0,02 g/cm срещу. 1,87 ± 0,04 g/cm). CMC и TLMC са изследвани отделно, за да се анализира допълнително кое телесно отделение е било засегнато от ограничаването на растежа на плода. CMC и TLMC са и по-ниски при SGA деца (CMC: 0.66 g/cm ± 0.01 при SGA срещу. 0,84 g/cm ± 0,02 в AGA; TLMC: 0,78 g/cm ± 0,02 в SGA и 1,03 g/cm ± 0,03 в AGA).
Фигура 2A показва общия BMC, CMC и TLMC на бебетата по отношение на растежа на плода, независимо от теглото при раждане. BMC не се различава значително между групите на NG и IG. Въпреки това, той е намален в случай на FGR, независимо от теглото при раждане. Общият BMC е по-нисък в групата с FGR (1,66 g/cm ± 0,03) в сравнение с групата на IG и NG ((1,86 g ± 0,04 и 1,89 g ± 0,05, съответно). По-ниският общ BMC при новородени с ограничен растеж е свързан с намаляване на BMC на багажника и крайниците. TLMC е по-нисък в групата на FGR (TLMC: 0.89 g/cm ± 0.02 в FGR, 1.04 g/cm ± 0.03 в IG и 1.06 g/cm ± 0.03 в NG), докато CMC не се различава значително между групите. Подобни резултати бяха намерени при сравняване на BMC, CMC и TMLC при AGA новородени сред различни модели на фетален растеж (Фиг. 2Б.). BMC и TLMC са по-ниски в групите с FGR (BMC: 1,8 g ± 0,03 в FGR, 2,0 g ± 0,08 в IG и 1,95 ± 0,05 в NG; TLMC: 0,98 g/cm ± 0,02 в FGR, 1,13 g/cm ± 0,05 в IG и 1,10 g/cm ± 0,03 в NG). При SGA новородените BMC и TLMC също са по-ниски при FGR (фиг. 2° С), но тази разлика не достига статистическа значимост поради малкия брой SGA бебета в IG и NG групи (BMC: 1,42 g/cm ± 0,04 в FGR, 1,59 g/cm ± 0,03 в IG и 1,62 g/cm ± 0,09 в NG; TLMC: 0,74 g/cm ± 0,03 в FGR, 0,86 g/cm ± 0,08 в IG и 0,9 g/cm ± 0,07 в NG).
Детерминанти на минералното съдържание.
Детерминантите на минералното съдържание при раждане бяха оценени с помощта на многовариатен анализ (β коефициенти и коригирани стр стойностите са показани в таблица 2, където BMC е коригиран за новородени и майчини фактори). Петдесет и седем процента от вариацията на BMC при раждането се обясняват със значимите детерминанти, включени в модела: гестационна възраст, SGA, FGR и пушене при майката (r 2 = 0,57, стр Таблица 2 Детерминанти на BMC при раждане чрез многовариатен анализ
ДИСКУСИЯ
По-рано се съобщава, че децата, родени с SGA, имат по-нисък BMC и намален маркер за образуване на кост (остеокалцин) в сравнение с тези, родени с AGA, дори след разрешаване на сезонни вариации (5). Генът на остеокалцин се експресира в късната фаза на формиране на костите (период на диференциация и минерализация). Шнуровият серум 1,25- (OH) 2 витамин D, активният метаболит на витамин D, който подобрява маточно-плацентарния трансфер на калций, е по-нисък при SGA, отколкото при бебета с AGA (19). Може да се мисли, че по-ниските нива на IGF-1, отчетени в SGA, могат да повлияят на синтеза на колаген и скоростта на утаяване на костната матрица. Всъщност IGF-1 стимулира репликацията на преостеобластни клетки и подобрява синтеза на остеобластичен колаген тип 1 чрез увеличаване на нивата на транскрипт на колаген от тип 1 в остеобластите (20,21). Но серумните биохимични показатели на синтеза и разграждането на колагена са подобни при децата с SGA и AGA (22). Взети заедно, тези данни подчертават, че намалената BMC при SGA бебета е свързана предимно с ниско количество минерали, а не с дефектен синтез на матрица. Можем да предположим, че в настоящото проучване BMC е по-ниска в групата на FGR по същата причина.
По време на бременността минералите се транспортират активно през плацентата до феталната циркулация срещу градиент на концентрация и плодът е напълно зависим от майчините ресурси, за да придобие Ca 2+, P и Mg. Скоростта на трансфер на Ca 2+ от матернофетала се увеличава драстично през последния триместър на бременността (от 24 седмици до срочна бременност), с пикови нива на нарастване между 36 и 38 седмици бременност (19). Приблизително две трети от цялото тяло Ca 2+, натрупано в здравословен човешки плод, се транспортира през последния триместър на бременността (23). Условия, засягащи трансфера на хранителни вещества в плацентата по това време, също вероятно ще повлияят на минерализацията на костите на плода. Според нашите резултати, в групата на FGR, основните рискови фактори са утероплацентарните съдови аномалии и пушенето при майката. Тютюнопушенето при майките, за което се съобщава, че влияе върху растежа на скелета, действа чрез различни механизми. Най-често цитираните са нарушена плацентарна функция, намален утероплацентарен кръвен поток или ефекти върху феталната способност за пренос на кислород (24,25). Друг докладван механизъм е потенциален токсичен ефект на тежкия метал кадмий върху растежа на скелета на плода. Кадмият присъства във висока концентрация като замърсител в тютюна и има специфични ефекти върху транспорта на калций на трофобласта (26).
В заключение, ограничаването на растежа на плода е важен фактор, определящ BMC при раждането и може да се разглежда като независим предиктор за минерализация на костите на плода, дори когато теглото при раждане се поддържа в нормалните граници. Този ефект е независим от ниското тегло при раждане, което прави SGA бебетата с ограничение на растежа на плода по-изложени на риск от нисък BMC.
- Тенденции в статистиката за теглото при раждане при новороденото
- Съдържание на кости в сурови месни кости, сурово хранене, сурови диетични съставки
- Айшвария Рай е критикувана, че не е отслабнала след раждането на бебето - Агенция за преса Khaama
- Противозачатъчни хапчета, еднакво ефективни за жени, независимо от теглото им - ScienceDaily
- Бонска супа за съставки за отслабване, рецепта, калорично съдържание, резултати и отзиви