А Джоу
1 отдел по хематология, Медицински факултет на Вашингтонския университет, Сейнт Луис, Мисури, САЩ
E M Knoche
1 отдел по хематология, Медицински факултет на Вашингтонския университет, Сейнт Луис, Мисури, САЩ
E K Engle
1 отделение по хематология, Медицинско училище във Вашингтонския университет, Сейнт Луис, Мисури, САЩ
D A C Фишър
1 отдел по хематология, Медицински факултет на Вашингтонския университет, Сейнт Луис, Мисури, САЩ
S T О
1 отделение по хематология, Медицинско училище във Вашингтонския университет, Сейнт Луис, Мисури, САЩ
55-годишна жена е диагностицирана за първи път с PV през 2001 г., когато е получила хемоглобин (Hgb) от 20,0 g/dl. През следващите 10 години пациентът е лекуван с аспирин и интермитентна хидроксиурея и анагрелид, с лошо съответствие. През май 2011 г. (10 години след първоначалната PV диагноза), тя се представи с влошаваща се умора, загуба на тегло и спленомегалия. Лабораторни проучвания разкриват повишен брой на белите кръвни клетки (WBC) от 45 × 10 9/l и Hgb от 9,5 g/dl. Изследването на периферната цитонамазка показа левкоеритробластични промени с малко циркулиращи взривове. Биопсия на костен мозък показа хиперцелуларност с гранулоцитна и мегакариоцитна хиперплазия, без излишни бласти и умерена фиброза при оцветяване с ретикулин. Първоначално се подозираше диагноза миелофиброза след PV; цитогенетиката обаче показва t (9; 22) в 20 от 20 метафазни клетки и флуоресценцията in situ хибридизация за BCR-ABL е положителна (92,5%). Количествената PCR за JAK2 V617F разкрива алелна тежест от 6%. Следователно, изглежда, че пациентът е развил ХМЛ с относително клонално доминиране над PV.
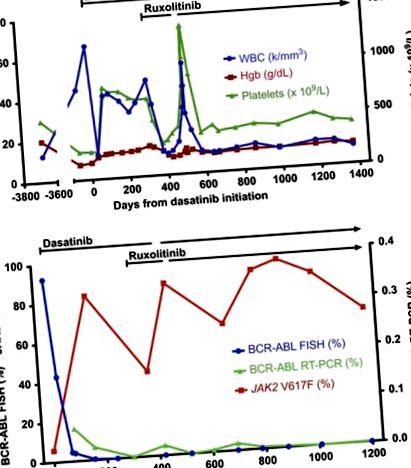
Лечението с дазатиниб 100 mg дневно започва през юли 2011 г., което води до драстично подобрение на левкоцитозата и анемията на пациента в рамките на 1 месец (Фигура 1а). Скоро след това обаче броят на левкоцитите и тромбоцитите започна да се увеличава. Три месеца след започване на лечение с дазатиниб, пълната кръвна картина (CBC) на пациента показва WBC от 42 × 10 9/l, Hgb 12,3 g/dl и брой тромбоцити 799 × 10 9/l. BCR-ABL чрез флуоресценция in situ хибридизация е намаляла до 4.0%, но тежестта на алела JAK2 V617F се е увеличила до 83% (Фигура 1b). Следователно, повторната поява на левкоцитоза и тромбоцитоза при този пациент изглежда се дължи на повторната поява на JAK2-мутантния клон в условията на потискане на BCR-ABL-положителния CML клон от дазатиниб.
Хематологични, цитогенетични и молекулярни данни. (а) Параметрите на CBC във времето са показани във връзка с лечението с дазатиниб и руксолитиниб. (б) Показани са цитогенетични и молекулярни анализи на BCR-ABL и JAK2 V617F във времето във връзка с лечението с дазатиниб и руксолитиниб.
Пациентът е бил лекуван с хидроксиурея без значително подобрение на левкоцитозата или тромбоцитозата и също така не е имало отговор, когато хидроксиуреята е била променена на анагрелид. Повторна биопсия на костния мозък, извършена през май 2012 г. (300 дни след започване на лечението с дазатиниб), разкрива свръхклетъчен мозък, липса на повишени бласти и тежка фиброза при оцветяване с ретикулин. Цитогенетичният анализ демонстрира пълен цитогенетичен отговор с BCR-ABL чрез qRT-PCR, открит при 0,001% (нормализиран до β-2 микроглобулин). Въпреки минималната остатъчна клонална тежест от ХМЛ, пациентът продължава да съобщава за умора и лош апетит, прогресивна загуба на тегло от 15 паунда и постоянна спленомегалия.
Благодарение на прогресивното нарастване на броя, продължаващите конституционални симптоми и лошата поносимост на хидроксиурея, лечението с руксолитиниб 10 mg два пъти дневно започна (в допълнение към продължаването на дазатиниб) през юни 2012 г. В рамките на 6 седмици се наблюдава значително подобрение в кръвта на пациента броя (WBC 11,9 × 10 9/l, Hgb 11,9 g/dl, тромбоцити 297 × 10 9/l), както и подобряване на конституционалните симптоми и спленомегалия. Пациентът понася добре лечението с комбинацията от руксолитиниб и дазатиниб, но се забелязва влошаваща се анемия през септември 2012 г., приблизително 4 месеца след започване на лечението с двете терапии. Тя бе посъветвана да държи руксолитиниб, но случайно задържа дазатиниб в продължение на 1 месец. Впоследствие дазатиниб беше възобновено и руксолитиниб беше задържан през октомври 2012 г. в продължение на месец, след което Hgb на пациента се подобри и тя бе възобновена отново с руксолитиниб при намалена доза от 5 mg два пъти дневно. Два месеца по-късно дозата на руксолитиниб е увеличена до 10 mg, редуващи се с 5 mg два пъти дневно.
Три години след започване на лечението с дазатиниб и руксолитиниб, симптомите на пациента и CBC остават стабилни и тя продължава комбинираната терапия с дазатиниб и руксолитиниб. Пациентът поддържа пълен цитогенетичен отговор с ниско ниво BCR-ABL, откриваемо чрез qRT-PCR, докато тежестта на алела JAK2 V617F варира между 43 и 96%.
Серийните количествени измервания на BCR-ABL и JAK2 V617F след лечение с дазатиниб показват значително намаляване на нивата на BCR-ABL със съпътстващо увеличаване на тежестта на алела JAK2 V617F, което предполага, че двете нарушения са възникнали от независими клонинги. За по-нататъшно разглеждане на този проблем бяха изолирани единични клетъчни колонии-предшественици и генотипирани за BCR-ABL и JAK2 V617F (Фигура 2). По-голямата част от колониите демонстрираха само присъствието на JAK2 V617F или BCR-ABL, но не и двете, потвърждавайки, че двете нарушения са възникнали в отделни клонинги.
Генотипизиране на отделни родословни колонии. Получено е информирано съгласие от пациента и пробите са събрани съгласно протокол, одобрен от Комитета по човешки изследвания на Вашингтонския университет (# 01-1014). Колониите бяха изолирани от периферната кръв по време на диагностика на ХМЛ и бяха генотипирани за BCR-ABL и JAK2 V617F. Показан е броят на колониите с всеки генотип.
Няколко други съобщения за случаи наблюдават подобно нарастване на тежестта на алела JAK2 V617F след успешно лечение с ABL инхибитор на тирозин киназа (TKI), 5, 6, 7, 8, включително наскоро публикуван доклад за двама пациенти с PV/CML, които са лекувани с комбинацията от иматиниб и руксолитиниб. 9 Подобно на нашия случай, лечението с иматиниб не е довело до подобряване на конституционалните симптоми или спленомегалия при нито един от пациентите, въпреки че и двамата са постигнали пълен цитогенетичен и основен молекулярен отговор на ХМЛ. Добавянето на руксолитиниб към иматиниб и в двата случая води до подобряване на конституционалните симптоми и спленомегалия; обаче и двамата пациенти се нуждаят от намаляване на дозата на руксолитиниб и иматиниб поради хематологична токсичност.
Доколкото ни е известно, това е първият доклад за пациент с едновременно PV и CML, лекуван с JAK инхибитор, и второ поколение ABL TKI, което окончателно показва, че двете новообразувания са възникнали от отделни клонинги. Нито един от предишните доклади за случаи не включва корелационен клонален анализ на пациенти, лекувани с тази комбинация от терапия. Генотипирането на отделни родословни колонии предполага, че двете нарушения са възникнали от независими клонинги, което е в съответствие с констатациите от серийни количествени измервания на BCR-ABL и JAK2 V617F по време на лечението; все пак е възможно тези два клонинга да са произлезли от споделен родов клонинг.
Комбинацията от руксолитиниб и дазатиниб е безопасна и ефективна при лечението на съпътстващи PV и ХМЛ при този пациент. Оптималният график на лечение (например едновременни, последователни или синхронизирани TKI схеми) за лечение на пациенти със съпътстващи PV/CML все още е неясен, но потенциално може да се ръководи от молекулярно наблюдение и биологични корелационни анализи. В крайна сметка най-добрият подход за лечение ще бъде определен от кинетичната динамика на всеки клонинг и поносимостта на комбинирането на TKI.
Благодарности
Тази работа беше подкрепена от грантове на NIH K08HL106576 (Oh), K12HL087107 (Oh) и T32HL007088 (Engle, Fisher). Техническа поддръжка беше осигурена от Центъра за ракови заболявания на Alvin J. Siteman и ядрата на поточната цитометрия, които се поддържат от NCI Cancer Center Support Grant P30CA91842. Благодарим на D. Moore за съдействието за банкиране на тъкани и L. He, G. Rippberger и M. Fulbright за съдействието при експерименти с генотипиране JAK2 и BCR-ABL.
Бележки
Авторите не декларират конфликт на интереси.
- Диетични протеини и хронична бъбречна болест - Протеинови и фосфорни храни - DaVita
- Диетични модификации за хронична уртикария Световна алергична организация
- Хранене, диета; Хранене при хронична диария при деца NIDDK
- Ефективност на различни техники за церебрална защита, използвани по време на хирургично лечение на хронична
- Ефекти от хроничната инфузия на лептин върху последващо телесно тегло и състав при мишки Can body