Дял
Свидетелство на д-р Сидни Улф, Бен Улпау и д-р Елизабет Барбеен.
Група за здравни изследвания на публичен гражданин
Заседание на консултативния комитет по ендокринни метаболитни лекарства на FDA относно римонабант
Въведение: Канабиноидните рецептори и вероятната римонабантна токсичност в тялото
Неуловимата идея за вълшебно лекарство от куршум, което има предимство, медиирано чрез действието му върху един рецепторен сайт, но въпреки това е лишено от рискове при безброй други сайтове в тялото, е отново (както при Vioxx, Rezulin, Redux и много други лекарства, отстранени поради тяхната токсичност), илюстрирани от римонабант. Да, има доказателства за загуба на тегло поради инхибиране на локализираните в мозъка диети. Но къде другаде в мозъка или други части на тялото се намират тези CB1 канабиноидни рецептори (които римонабантът инхибира)?
CB1 рецепторите се изразяват в:
- Мозък: обонятелни и кортикални области (неокортекс и пиеформна кора), хипокампус и амигдала, базални ганглии, ядра на таламуса и хипоталамуса, мозъчна кора и мозъчни стволови ядра. Един от най-разпространените рецептори, свързани с G-протеин в мозъка. [1]
- Периферия: вегетативна нервна система, черен дроб, мускули, стомашно-чревен тракт и мастна тъкан, [2] хипофизна жлеза, имунни клетки и репродуктивни тъкани. [3]
- На всички CB1 рецептори, с по-висок афинитет към цити на ЦНС
Широк обхват на канабиноидната система:
- „CB система, участваща в различни физиологични функции, които включват роли в възстановяването на стреса и поддържането на хомеостатичния баланс. Такива роли включват например неврозащита, модулация на ноцицепция, регулиране на двигателната активност, контрол на определени фази на паметта, модулация на имунната и възпалителна реакция, влияние върху сърдечно-съдовата и дихателната системи и антипролиферация на туморни клетки. ”[4 ]
Психиатрични неблагоприятни ефекти
Като се имат предвид многобройните места в мозъка с CB1 рецептори, извънредно широките видове психиатрична дисфункция, причинени от лекарството (в допълнение към „статистически значимо повишена самоубийство“ и други депресивни симптоми) не са изненадващи.
Както се вижда в следващата таблица, има значително увеличение на тревожността, безсънието, пристъпите на паника и почти значително увеличаване на агресията (също се наблюдава при проучвания при животни) и възбуда при пациенти, получаващи 20 mg римонабант спрямо пациенти, получаващи плацебо. В допълнение, значително повече пациенти, получаващи римонабант, се нуждаят от успокоително или транквилизатор или антидепресант за нежелани събития, причинени от лекарството.
Психиатрични симптоми, докладвани като нежелани събития - обединени проучвания на РИО
(Данни от стр. 23 и 25, Бритателен документ на FDA: изчислени стойности на p)
Плацебо
N = 1602
# (%)
20 mg римонабант
N = 2176
# (%)
p Стойност
Общ брой пациенти, съобщаващи за симптоми
25 пъти човек на базата на BSA)
Репродуктивна токсичност (заек) *: намален размер на постелята, увеличена загуба след имплантацията, намалено телесно тегло на плода и увеличени малформации (аненцефалия, микроофталмия, разширени мозъчни вентрикули и омфалоцеле) при (5 пъти човешко на база BSA)
Случаят на канабиноидна регулация на имплантацията и развитието на плода също трябва да се вземе като пример за това колко ограничено разбиране имат учените за ролята на тази широко разпръсната невротрансмитерна система. Rimonabant е първото лекарство от своя клас, което се използва при хора и има много важни въпроси, които остават без отговор.
Въпроси относно дългосрочната безопасност
Основен проблем, в допълнение към обсъдените по-горе, е липсата на надеждна информация относно дългосрочните ефекти от употребата на римонабант. От проведените до момента проучвания две са с продължителност две години, докато останалите три са една година. Тъй като римонабантът е първото лекарство от своя клас, няма данни за оценка на дългосрочния ефект на антагонизиране на широко разпространената канабиноидна система. Загубеното тегло при използване на римонабант се възстановява след прекратяване на употребата [24] [25], което означава, че ако лекарството изобщо е ефективно, ще трябва да се предписва дългосрочно. Като се има предвид този факт, пълната липса на данни за употребата на римонабант при хора за продължителен период от време е причина за значително безпокойство.
Литературата за изследвания върху животни, проведени с римонабант, съдържа зловещи индикации за проблеми, които могат да възникнат, тъй като хората продължават да използват лекарството за по-дълги периоди от време. Zimmer et al. съобщават, че нокаутиращите мишки CB1 имат значително повишена смъртност поради "спонтанни" смъртни случаи с неизвестна причина (Фигура по-долу). [26] Цимер, експерт по изследване на канабиноидна система, също отбелязва, че същата тази верига мишки с дефицит на СВ1 показва повишена загуба на неврони при стареене. [27] Въпреки че това не се обобщава директно за употребата на римонабант при хора, все още е причина за безпокойство при липсата на проучвания за оценка на ефектите от дългосрочния антагонизъм на CB1.
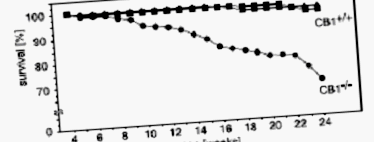
От Zimmer et al., 1999: Степен на смъртност при нокаутиращи мишки CB1 (-/-), див тип (+/+) и хетерозиготни.
Други проучвания показват ясни ефекти на рецептора CB1 върху сърдечно-съдовата система при предизвикване на хипотония и брадикардия. [28] [29] Не е ясно дали римонабантът чрез блокиране на регулаторните ефекти на ендогенните агонисти или чрез механизъм на обратен агонист [30] може да промени функционирането на сърдечно-съдовата система по начин, който може да се окаже вреден в дългосрочен план.
Заключение
Неотдавнашен задълбочен преглед на римонабант от базата данни на Cochrane за систематични прегледи стигна до заключението, че 1) че средната загуба на тегло е „умерена“ и 2) са необходими по-строги проучвания на ефикасността и безопасността, за „да се направи пълна оценка на съотношението полза и риск от това ново лекарство. ”[31] Ние силно се съгласяваме с това твърдение, което ясно изисква отхвърлянето на одобрението на римонабант поради липса на способност„ да се оцени изцяло съотношението полза и риск от това ново лекарство “.
[1] Di Marzo V, Bifulco M, De Petrocellis L. Ендоканабиноидната система и нейната терапевтична експлоатация. Отзиви за природата. Откриване на наркотици 2004;3: 771–84.
[3] Pertwee, RG. „Фармакологията на канабиноидните рецептори и техните лиганди.“ Международен вестник за затлъстяването 30 (2006): s13-s18. www.nature.com/ijo
[5] Faith, Myles S., Patty E. Matz и Marie A. Jorge. „Затлъстяването - асоциации на депресията сред населението.“ Journal of Psychosomatic Research 53 (2002): 935-942.
[6] Голей, Ален, Ан Лоран-Джакар, Франк Хабихт, Жан-Пиер Гачу, Мирей Шабло, Ан Камер и Ив Шуц. "Ефект на орлистат при пациенти със затлъстяване с нарушено хранене." Фармакология и терапия 13 (2005): 1701-1708.
[7] Гаде, Кишор М. „Ефект на римонабант върху теглото и кардиометаболитните рискови фактори.“ Кн. 296. Университет Джон Хопкинс, 2006.
[8] Херман, Кристоф. „Международен опит със скалата за тревожност и депресия в болницата - преглед на данните за валидиране и клиничните резултати.“ Journal of Psychosomatic Research 42 (1996): 17-41.
[9] Crawford, J R., J D. Henry, C Crombie и E P. Taylor. „Нормативни данни за HADS от голяма неклинична проба.“ Британски вестник по клинична психология 40 (2001): 429-434.
[10] Саймън, Грегъри Е., Майкъл фон Корф, Катлийн Сондърс и др. „Асоциация между затлъстяването и психиатричните разстройства в възрастното население на САЩ.“ Arch Gen Psychiatry (2006): 824-830.
[11] Страница 14, документ за преглед на FDA
[12] Xie, S., M. A. Furjaniec, J. J. Ferrara, E. L. Ardino, et al. „Ендоканабиноидната система и римонабант: ново лекарство с нов механизъм на действие, включващо канабиноиден CB1 рецептор Antagoinst - или обратен агонизъм - като лечение на потенциално затлъстяване и друга терапевтична употреба.“ Journal of Clinical Pharmacy and Therapeutics 32 (2007): 209-231.
[13] Ван Гаал, Люк Ф., Айла М. Рисанен, Андре Дж. Шийн и др. „Ефекти на блокера на рецепторите на канабиноид-1 върху намаляването на теглото и сърдечно-съдовите рискови фактори при пациенти с наднормено тегло: 1-годишен опит от проучването RIO-Europe.“ Lancet 365 (2005): 1389-1397.
[14] Pi-Sunyer, F, Louis J. Aronne и Hassan M. Heshmati. „Ефект на римонабант, блокиращ рецептор за канабиноид-1, върху теглото и кардиометаболитните рискови фактори при пациенти с наднормено тегло или затлъстяване (RIO-Северна Америка: рандомизирано контролирано проучване).“ JAMA 295.7 (2006): 761-775.
[15] Scheen, Andre J., Nick Finer и Priscilla Hollander. „Ефикасност и поносимост на римонабант при пациенти с наднормено тегло или затлъстяване с диабет тип 2: рандомизирано контролирано проучване.“ Lancet 368 (2006): 1660-1672.
[16] Деспрес, Жан-Пиер, Ален Голей и Ларс Сьостром. „Ефекти на римонабант върху метаболитните рискови фактори при пациенти с наднормено тегло с дислипидемия.“ NEJM 353 (2005): 2121-34.
[17] Leung, Wilson, G. N. Thomas, Juliana Chan, et al. „Управление на теглото и текущи възможности във фармакотерапията: Орлистат и сибутрамин.“ Клинична терапевтика (2002): 58-80.
[18] Симънс-Мортън, Дениз Г., Ева Обарзанек и Джефри А. Кътлър. „Изследвания на затлъстяването - ограничения на методите, измерванията и медикаментите.“ JAMA 295.7 (2006): 826-828.
[19] Curioni, C. и C. Andre. „Римонабант за наднормено тегло или затлъстяване (преглед).“ База данни на Cochrane за систематични прегледи (2006).
[20] Яновски, Сюзън З. „Фармакотерапия при затлъстяване - обещание и несигурност“. NEJM (2005): 2187-2189.
[21] Curioni, C. и C. Andre. „Римонабант за наднормено тегло или затлъстяване (преглед).“ База данни на Cochrane за систематични прегледи (2006).
[22] Информационен документ за Санофи, страница 15.
[24] Pi-Sunyer, F, Louis J. Aronne и Hassan M. Heshmati. „Ефект на римонабант, блокиращ рецептор за канабиноид-1, върху теглото и кардиометаболитните рискови фактори при пациенти с наднормено тегло или затлъстяване (RIO-Северна Америка: рандомизирано контролирано проучване).“ JAMA 295.7 (2006): 761-775.
[25] Редакционен състав на предписанията. „Римонабант.“ Prescrire International 15 (2006): 123-126.
[26] Цимер, Андреас, Ан М. Цимер и Андреа Г. Хоман. "Повишена смъртност, хипоактивност и хипоалгезия при канабиноидни CB1 рецепторни нокаут мишки." PNAS 96 (1999): 5780-5785.
[28] Варга, Кароли, Кристи Лейк, Били Мартин и Джордж Кунос. „Новият антагонист включва CB1 канабиноидния рецептор в хипотензивното действие на анандамид.“ European Journal of Pharmacology 278 (1995): 297-283.
[29] Лейк, Кристи Д., Дейвид Р. Комптън, Кароли Варга, Били Р. Мартин и Джордж Кунос. „Канобиноид-индуцираната хипотония и брадикардия при плъхове се медиира от CB1-подобни канабиноидни рецептори.“ Journal of Pharmacolocy an Experimental Therapeutics 281 (1997): 1030-1037.
[30] Pertwee, RG. „Обратен агонизъм при канабиноидните рецептори.“ Международен конгрес от серия 1249 (2003): 75-86.
- Публично известие Япония Хокайдо хапчета за отслабване за отслабване съдържат скрити лекарствени съставки FDA
- Капсула за отслабване на публично известие Dream Body Съдържа скрита лекарствена съставка FDA
- Публично известие Li Da Dai Dai Hua капсула за отслабване съдържа скрита лекарствена съставка FDA
- Обществено известие Perfect Slim Fast Track Slim съдържа скрити лекарствени съставки FDA
- Public Notification Natural Max Slimming съдържа скрити лекарствени съставки FDA
