Shahabeddin Rezaei 1, 2, Mona Kavoosi 1, Reza Shervin Badv 3, Mahmoud Mohammadi 3, Gholam Reza Zamani 3, Mahmoud Reza Ashrafi 3, Mir Saeed Yekaninejad 4, Maryam Mahmoudi 1, 5, 6, *
1 Катедра за клетъчно молекулярно хранене, Училище по хранителни науки и диететика, Техерански университет по медицински науки, Техеран, Иран
2 Студентски център за научни изследвания, Техерански университет по медицински науки, Техеран, Иран
3 Педиатричен център за върхови постижения, Катедра по детска неврология, Детски медицински център, Техерански университет по медицински науки, Техеран, Иран
4 Катедра по епидемиология и биостатистика, Училище за обществено здраве, Техерански университет по медицински науки (TUMS), Техеран, Иран
5 Детски център за гастроентерология и хепатология, Детски медицински център, Техерански университет за медицински науки, Техеран, Иран
6 Екип от експерти по диетология и хранене (DiNET), Универсална мрежа за научно образование и изследвания (USERN), Техеран, Иран
Как да цитирам: Rezaei S, Kavoosi M, Shervin Badv R, Mohammadi M, Zamani G R, et al. Влиянието на кетогенната диета върху чернодробната функция при деца и юноши с неразрешима епилепсия, J Compr Ped. 2017; 8 (3): e12609. doi: 10.5812/compreped.12609.
Резюме
Заден план: Високото съдържание на мазнини и ограничаването на въглехидратите в кетогенната диета (KD) увеличава натоварването на някои органи, особено на черния дроб. Нещо повече, повечето от антиепилептичните лекарства (AED) се метаболизират в черния дроб; следователно, функцията на черния дроб може да бъде повлияна по време на лечението с KD. Това проучване е предприето, за да се изследва влиянието на кетогенната диета върху чернодробната функция.
Методи: Проведено е проспективно открито проучване. Общо 28 пациенти с нелечима епилепсия са започнали диетата. Всички пациенти са деца и юноши, които не са отговорили на поне 2 AED. Тестове за чернодробна функция, включително аланин аминотрансфераза (ALT), аспартат аминотрансфераза (AST) и алкална фосфатаза (ALP) са анализирани преди и след 3 месеца на KD.
Резултати: Четиринадесет пациенти със средна възраст 4.12 (2.31 - 9.70) години са завършили проучването. Серумните нива на ALP и AST не се различават значително преди и след 3 месеца на диетата (P стойност> 0,05). Имаше значителна разлика в серумните нива на ALT преди и след 3-месечно лечение (13 vrs 20, P = 0,014).
Заключения: Въпреки че изглежда, че KD не е оказал влияние върху серумните нива на AST и ALP; обаче има значително влияние върху серумното ниво на ALT. За одобряване на гореспоменатите резултати са необходими повече изследвания с по-голям размер на извадката и по-голяма продължителност на проследяване.
1. Предистория
Кетогенната диета (KD) е диета с ниско съдържание на въглехидрати, високо съдържание на мазнини и адекватно протеини. Преди всичко KD е въведен за лечение на неразрешима епилепсия през 1921 г. (1), но през последните години употребата на KD се разширява и към други заболявания, включително присъщи метаболитни заболявания (2), аутизъм (3) и глиобластом (4). Първоначално използваната диета е класическата KD, чиито триглицериди с дълга верига са основният енергиен източник на диетата (90%) (5). Диетата се изчислява въз основа на съотношението мазнини към въглехидрати плюс протеини (кетогенно съотношение). Съотношението при класическата кетогенна диета е 4: 1 или 3: 1, 4 g (или 3 грама) мазнини към 1 g комбиниран протеин и въглехидрати (5).
При лечението с KD тялото имитира метаболитните условия, установени по време на гладуване (6). Мазнините стават преобладаващи енергийни източници по време на лечението с KD вместо глюкоза (6). В черния дроб дълговерижните мастни киселини се превръщат в кетонни тела, включително β-хидроксибутират, ацетоацетат и ацетон по пътя на β-окислението (6).
Обикновено пациентите с нелечима епилепсия се нуждаят от продължително лечение с антиепилептични лекарства (AED) (7). Повечето от AED се метаболизират предимно от черния дроб, включително валпроат (VPA), карбамазепин, ламотрижин, фенобарбитал, окскарбазепин, фенитоин, фелбамат, етосуксимид и бензодиазепини (8). Освен това някои от тях са AED, частично метаболизирани от черния дроб, включително леветирацетам, топирамат и зонисамид (8).
Изглежда, че комбинацията от KD и AED може да повлияе на чернодробната функция. Няколко проучвания съобщават за краткосрочните и дългосрочните неблагоприятни ефекти на KD (9, 10). И все пак влиянието на KD върху чернодробната функция е неясно. Следователно, това проучване е проведено, за да се изследва влиянието на класическия KD върху серумните нива на чернодробните ензими при епилептични деца и юноши.
2. Методи
2.1. Проучване на населението
Беше използван потенциален, отворен дизайн на проучване. Настоящото проучване беше проведено в детския медицински център на Техеранския университет по медицински науки (TUMS) между септември 2015 г. и октомври 2016 г. В това проучване бяха включени пациенти с неразрешима епилепсия, които имаха следните критерии; 1. на възраст между 2 и 18 години и 2. не е реагирал на поне 2 антиепилептични лекарства. Критериите за изключване включват: 1. предишно лечение с KD; 2. анамнеза за метаболитни заболявания, които имат противопоказана употреба на кетогенната диета, включително дефицит на пируват карбоксилаза и ацил-КоА дехидрогеназа със средна верига; 3. предишна история на чернодробни заболявания; 4. анамнеза за дислипидемия; 5. анамнеза за заболявания на щитовидната жлеза; 6. анамнеза за бъбречни заболявания; и 7. затруднено преглъщане.
2.2. Протокол за кетогенна диета
За пациентите е започнато класическо KD. За пациентите се прилага кетогенното съотношение 4: 1, 4 грама мазнини към 1 грам въглехидрати плюс протеин. Не бяха въведени ограничения на гладно, калории или течности. Преди започване на диетата пациентите са изследвани за метаболитни заболявания, които имат противопоказания за KD. Тъй като KD има хранителен дефицит, мултивитамините и минералите, както и допълнителни добавки с калций и витамин D бяха дадени на всички пациенти. Всички пациенти са били проследявани по телефона по време на лечението и амбулаторно посещение след 1 и 3 месеца на диета.
2.3. Антропометрични оценки
Теглото и височината на пациентите са измервани на изходно ниво и 3 месеца след започване на диетата. Преди измерването участниците бяха помолени да събуят обувките и тежките си дрехи. За измерване на теглото (кг) беше използвана стандартизирана скала на балансираща греда. Височината (cm) се измерва със стадиометър. Индексът на телесна маса (ИТМ) се изчислява като измереното телесно тегло в kg, разделено на квадрата на измерената височина в метри (kg/m 2).
2.4. Параметри на чернодробната функция
Кръвна проба се получава сутрин след гладуване през нощта. Параметри на чернодробната функция, а именно аланин аминотрансфераза (ALT), аспартат аминотрансфераза (AST) и алкална фосфатаза (ALP) бяха анализирани преди започване на диетата и през месец-3.
2.5. Разглеждане на етиката
Изследването е започнато след одобрение от етичната комисия на заместник-изследователя на Техеранския университет по медицински науки (етичен кодекс, IR.TUMS.REC.1394.181512.11.94). Информирано съгласие е получено от всички родители на пациенти преди започване на диетата. Пациентите са участвали доброволно в проучването и родителите на пациента са били уверени, че могат да излязат от проучването на всеки етап от проучването. Не са направени допълнителни разходи от семейството на пациентите.
2.6. Статистически анализи
Използван е тест с ранг, подписан от Wilcoxon, за сравняване на средните серумни нива на чернодробните функционални тестове преди и след започване на KD. Резултатите са изобразени като среден и интерквартилен диапазон (25-ти - 75-и процентил). Статистическото ниво на значимост за всички тестове е P
3. Резултати
Общо 28 пациенти с неразрешима епилепсия са започнали диетата, сред тях 14 пациенти са завършили проучването, включително 11 момчета. Четиринадесет пациенти прекратиха диетата поради непоносимост към диетата, нежелание на семейството, лека ацидоза и пневмония. Средната възраст при започване на диетата е била 4,12 години (интерквартилен диапазон: 2,31 - 9,70). Таблица 1 демонстрира общите характеристики на пациентите.
Таблица 1. Общи характеристики на изследваната популация
| Мъжки пол | 11 (78,6%) |
| Женски пол | 3 (21,4%) |
| Медиана (интерквартилен диапазон) | |
| Възраст (y) | 4,12 (2,31 - 9,70) |
| Височина (см) | 102,85 (90,00 - 137,92) |
| Тегло (кг) | 15,00 (11,65 - 31,25) |
| ИТМ (kg/m 2 ) | 14,75 (13,80 - 16,35) |
Съкращение: ИТМ, индекс на телесна маса.
Средните (интерквартилен диапазон) серумни нива на AST, ALT и ALP на изходно ниво са съответно 21 (18 - 26) U/L, 13 (8 - 21) U/L и 448 (288 - 708) U/L, съответно . След 3 месеца серумното ниво на AST е 29 (17 - 38) U/L, серумното ниво на ALT е 20 (14 - 44) U/L, а серумното ниво на ALP е 453 (298 - 569) U/L.
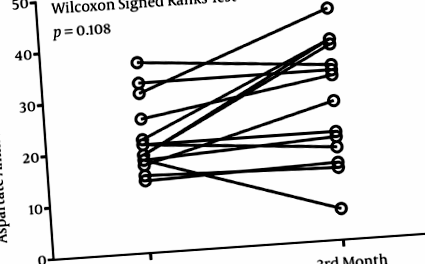
Няма разлика в нивото на ALP на изходно ниво и месец-3 (P = 0,249) (Фигура 1). Стойността на P от 0,108 разкри, че серумните нива на AST не се различават значително преди и след 3-месечно лечение (Фигура 2). Имаше значителна разлика в серумните нива на ALT преди и след 3-месечно лечение (P = 0,014) (Фигура 3).
4. Дискусия
В настоящото проучване ние изследвахме проспективно биомаркерите на чернодробната функция на пациенти с неразрешима епилепсия. Резултатите от настоящото проучване показват, че класическата KD не е оказала пагубно влияние върху серумните нива на AST и ALP; обаче има ефект върху серумното ниво на ALT.
KD има някои краткосрочни и дългосрочни вредни ефекти върху пациентите (9). Хипогликемия, ацидоза, гадене, запек и повръщане са някои примери за краткосрочни странични ефекти (9). Някои от дългосрочните неблагоприятни ефекти са дислипидемия, камъни в бъбреците, остеопения и дефицит на карнитин (11). По-ранни проучвания съобщават за няколко случая, при които след употреба на KD серумните нива на чернодробните ензими се променят (9, 12). В проучването, проведено от Arslan et al., Те ретроспективно оценяват дългосрочния ефект на KD при пациенти (12). След 3 месеца 2 пациенти са имали високи серумни нива на ALT и AST. Един от пациентите е използвал VPA, както и леветирацетам, а другият е приемал фенобарбитал и леветирацетам преди започване на диетата (12). Освен това, в проучване, направено от Kang et al, сред 129-те пациенти, които са били включени в проучването, 10 от тях са имали повишаване на ALT и AST (9).
Предишни проучвания разкриват, че комбинацията от AED и KD, особено VPA, може да повлияе на чернодробната функция. Stevens et al. съобщава за 18-месечно момиче, което е претърпяло чернодробна дисфункция след започване на KD. Пациентът приема VPA едновременно с KD. Нивата на ALT и AST на пациента се увеличиха драстично след 1 ден на KD, от 13 IU/L на 750 IU/L и съответно от 28 IU/L на 785 IU/L. След прекратяване на VPA, серумните нива на ALT и AST стават нормални (13).
Един от нашите пациенти е имал значително повишаване на серумните нива на ALS и AST. Случаят беше на 13 години. Взе нитразепам и VPA. Неговите изходни серумни нива на AST и ALT са съответно 19 U/L и 12 U/L. След 3 месеца лечение серумните нива на AST и ALT се повишиха съответно до 38 U/L и 79 U/L.
В проучването, проведено от Lyczkowski et al, 2 пациенти, които са приемали KD и VPA едновременно, са имали повишаване на серумните чернодробни ензими (14). При 1 пациент след 3 седмици серумните нива на ALT и AST бяха повишени до 201 U/L и 161 U/L, съответно. Вторият пациент изпитва повишаване на чернодробните функционални тестове след 2 седмици на диета (ALT, 229 U/L; AST, 238 U/L). Въпреки че след сравнение на неблагоприятните ефекти на пациентите, получили комбинацията от KD и VPA и пациентите, приемащи изключително KD, те стигнаха до заключението, че едновременното въвеждане на KD и VPA не увеличава шанса за хепатотоксичност (14). Освен това Ballaban-Gil et al. съобщава за 2 случая, които са имали значително повишаване на биомаркерите на чернодробната функция по време на започване на диетата и 13 месеца след започване на KD (15).
Един от механизмите за нарушение на чернодробните ензими може да бъде влиянието на диетата и AED върху съхранението на карнитин. Карнитинът е производно на аминокиселина, което е отговорно за транспорта на дълговерижните мастни киселини до митохондриите (16). Предишни проучвания разкриха, че и двете AED, особено VPA и KD, изчерпват съхранението на карнитин (16). VPA се метаболизира предимно от черния дроб чрез глюкурониране и окисление (8, 16). VPA претърпява 2 пътя на окисляване, а именно бета- и омега-окисляване. Обикновено бета-окисляването доминира над омега-окисляването (17). По пътя на бета-окислението VPA се комбинира с карнитин, за да се транспортира до митохондриите, поради което съдържанието на карнитин намалява постепенно (17). Освен това, големи количества дълговерижни триглицериди намаляват нивото на карнитин. Всъщност добавянето на KD към някои AED, особено VPA, има синергично влияние върху изчерпването на съхранението на карнитин (16).
Намаляването на количеството карнитин води до хепатотоксичност (16). Точният механизъм не е ясен, но по-ранни проучвания предполагат, че намаляването на карнитина води до дисбаланс между гама- и бета-окисляването. По пътя на гама-окислението се получават някои токсични метаболити, включително 4-en-VPA. При липса на карнитин, VPA се подлага на гама-окисление вместо на бета-пътя, поради което натрупването на токсични метаболити води до хепатотоксичност.
Това проучване имаше някои ограничения. Едно от ограниченията на настоящото проучване беше броят на пробата. Отсъствието на контролната група беше друго ограничение на настоящото проучване. В заключение изглежда, че KD не е оказал влияние върху серумните нива на AST и ALP; това обаче е оказало ефект върху серумното ниво на ALT.
Благодарности
Това проучване беше подкрепено от Техеранския университет по медицински науки; грант № 94-03-161-30342.
Препратки
Wilder R. Ефектите на кетонемията върху хода на епилепсията. Mayo Clin Proc. 1921;
Scholl-Burgi S, Holler A, Pichler K, Michel M, Haberlandt E, Karall D. Кетогенни диети при пациенти с наследствени метаболитни нарушения. J Inherit Metab Dis. 2015 г .; 38(4): 765 -73 [DOI] [PubMed]
Кастро. К., Faccioli LS, Baronio D, Gottfried C, Perry IS, dos Santos Riesgo R. Ефект на кетогенна диета върху разстройство от аутистичния спектър: Систематичен преглед. Res Autism Spectr Disord. 2015 г .; 20.: 31 -8
Winter SF, Loebel F, Dietrich J. Роля на кетогенната метаболитна терапия при злокачествен глиом: Систематичен преглед. Crit Rev Oncol Hematol. 2017; 112: 41 -58 [DOI] [PubMed]
Winesett SP, Bessone SK, Kossoff EH. Кетогенната диета при фармакорезистентна детска епилепсия. Експерт Rev Neurother. 2015 г .; 15(6): 621 -8 [DOI] [PubMed]
Masino SA, Rho JM. Механизми на кетогенно диетично действие. Основните механизми на Джаспър на епилепсиите. 2012; [PubMed]
McCorry D, Chadwick D, Marson A. Текущо медикаментозно лечение на епилепсия при възрастни. Lancet Neurol. 2004; 3(12): 729 -35 [DOI] [PubMed]
Ахмед SN, Siddiqi ZA. Антиепилептични лекарства и чернодробни заболявания. Припадък. 2006; 15(3): 156 -64 [DOI] [PubMed]
Kang HC, Chung DE, Kim DW, Kim HD. Ранно и късно настъпили усложнения на кетогенната диета за неразрешима епилепсия. Епилепсия. 2004; 45(9): 1116 -23 [DOI] [PubMed]
Lin A, Turner Z, Doerrer SC, Stanfield A, Kossoff EH. Усложнения по време на започване на кетогенна диета: Разпространение, лечение и влияние върху резултатите от гърчове. Педиатър Неврол. 2017; 68: 35 -9 [DOI] [PubMed]
Cervenka MC, Henry BJ, Kossoff EH, Zahava Turner R. Кетогенните и модифицирани диети на Аткинс: Лечения за епилепсия и други разстройства. 2016 г .;: 376
Arslan N, Guzel O, Kose E, Yilmaz U, Kuyum P, Aksoy B, et al. Кетогенното диетично лечение хепатотоксично ли е за деца с неразрешима епилепсия? Припадък. 2016 г .; 43: 32 -8 [DOI] [PubMed]
Стивънс CE, Turner Z, Kossoff EH. Чернодробна дисфункция като усложнение на комбинирана валпроат и кетогенна диета. Педиатър Неврол. 2016 г .; 54: 82 -4 [DOI] [PubMed]
Lyczkowski DA, Pfeifer HH, Ghosh S, Thiele EA. Безопасност и поносимост на кетогенната диета при детска епилепсия: ефекти на комбинираната терапия с валпроат. Епилепсия. 2005; 46(9): 1533 -8 [DOI] [PubMed]
Ballaban-Gil K, Callahan C, O'Dell C, Pappo M, Moshe S, Shinnar S. Усложнения на кетогенната диета. Епилепсия. 1998; 39(7): 744 -8 [PubMed]
Lheureux PE, Hantson P. Карнитин при лечението на индуцирана от валпроева киселина токсичност. Clin Toxicol (Phila). 2009; 47(2): 101 -11 [DOI] [PubMed]
Сингх Г. Управление на медицинската коморбидност, свързана с епилепсия. Лечението на епилепсия. 2009;: 259 -72
Bjornsson E. Хепатотоксичност, свързана с антиепилептични лекарства. Acta Neurol Scand. 2008; 118(5): 281 -90 [DOI] [PubMed]
- Кетогенната диета за 3- до 6-годишно проследяване на 150 деца, записани в бъдеще - PubMed
- Кетогенната диета и други диетични лечения за рефрактерна епилепсия при деца
- Твоята майка; диетата може да повлияе на черния дроб; s здраве
- Кетогенната диета и епилепсията; Деца; s Здраве
- Оценката „Оптимизирана смесена диета“ на система за ориентиране на храните за деца и юноши -