Татяна С. Калинина
a V.V. Институт по фармакология на Закусов RAMS, Русия
Дмитрий В. Зленко
b М.В. Московски държавен университет „Ломоносов“, Русия
г Н.Н. Федерален изследователски център по химична физика на Семенов, Руска академия на науките, Москва, Русия
Алексей В. Киселев
г Н.Н. Федерален изследователски център по химична физика на Семенов, Руска академия на науките, Москва, Русия
Александър А. Литвин
c Федерален изследователски и клиничен център по физико-химична медицина FMBA, Русия
Сергей В. Стовбун
г Н.Н. Федерален изследователски център по химична физика на Семенов, Руска академия на науките, Москва, Русия
Резюме
Този кратък доклад е посветен на описанието на широката антивирусна и антибактериална активност на имуномодулиращия агент Panavir®. Panavir® е фракция с високо молекулно тегло на полизахаридите, извлечени от издънките на Solanum tuberosum. Той демонстрира активност срещу много видове вируси, включително животински коронавирус, а също и срещу бактериални инфекции. Тези свойства изглеждат много обещаващи, като се има предвид епидемията на COVID-19 и позволяват да се предположи, че Panavir® ще бъде ефективен в терапията на инфекцията с SARS-CoV-2.
1. Въведение
Panavir® е фракция с високо молекулно тегло на полизахаридите, извлечени от издънките на Solanum tuberosum (картофи). Химичният състав на Panavir® е доста променлив: глюкоза (10–67%), галактоза (2–27%), арабиноза (3–15%), рамноза (2–10%), маноза (0,1–5%), и ксилоза (0,1–3%). Също така съдържа някои уронови киселини (2–5%), следи от липиди и пептиди и протеини, на първо място, RuBisCo (общо под 1%). Липсата на йодно оцветяване показва омрежването на хексозните полимери, което предотвратява образуването на клатрати от канален тип, отговорни за характерното синьо оцветяване [1].
При pH 7 и температура от 36 ° C разтворимостта на Panavir® е 13 g на 100 g. Разтворът на Panavir® е монодисперсната колоидна система, съставена от сферични частици. Зета потенциалът на частиците е отрицателен и е равен на около -25 mV. Според ултразвуковия акустичен спектрален анализ средният диаметър на частиците е около 140 nm, докато според резултатите от DLS изследването е около 350 nm. ЕМ изследването на остатък след изсушаване на разтвора даде оценка от около 250 nm. Средното молекулно тегло на тези частици е оценено на 3 · 10 9 Da [1, 2].
2. Методи
2.1. Антивирусна дейност
Ефектът срещу повтарящ се генитален херпес е оценен при възрастни жени, страдащи от характерни херпесни симптоми като болезненост, парене и сърбеж (медицински център ALS-MED, Санкт Петербург). Експерименталната група беше съставена от 33 жени, докато само 20 жени бяха в контрола. Диагнозата е потвърдена чрез PCR. Panavir® се прилага под формата на кожен мехлем (2 mg на 100 g от гела) и интравенозни инжекции (0,004% разтвор, 5 ml веднъж дневно) в продължение на 14 дни [6].
Ефектът срещу енцефалит, пренасян от кърлежи, е изследван при мишки и хора. Белите безпородни мишки от 10–12 g (24 проби във всяка група) са заразени от щама Sofin на вируса на енцефалит (подкожно инжектиране на 10% мозъчна суспензия на заразените мишки) и са третирани с Panavir® за 24 и 72 часа след инфекцията (0,01 mg на 1 g жива маса, интравенозно). Концентрацията на вирусните частици в мозъка на заразените мишки се оценява чрез контагиозността на мозъчната суспензия върху клетъчната линия на свинския бъбрек (SPEV). Първоначалната суспензия се разрежда последователно 10 пъти и се тества в клетъчната култура. Концентрацията на антителата срещу вируса също се оценява чрез способността на серума да неутрализира вируса и да предотврати инфекцията на същите SPEV клетки.
При хората активността на Panavir® срещу кърлежовия енцефалит е изследвана при пациенти (30 души в експериментална група и 113 в контролната група), страдащи от острия (трескав) стадий на синдрома, лекувани със специфичния имуноглобулин, и бяха уволнени. Но с течение на няколко месеца се върна с главоболие, адинамия и хипорефлексия. Групирането на левкоцитите е направено с помощта на моноклонални антитела, получени от Diagno-Tex (Москва). Концентрацията на интерфероните беше измерена с помощта на специфичните тестови комплекти от Vector-Best (Санкт Петербург) [10]. Panavir® се прилага под формата на интравенозни инжекции от 5 ml 0,004% разтвор, разделени на интервали от 18 часа (дървесни времена).
Активността на Panavir® срещу рабдовирусна инфекция е демонстрирана при мишки, морски свинчета и кучета. При мишки инфекцията е предизвикана от щама ERA-CB-20 M на рабдовируса, инжектиран интрамускулно (0,1 ml 3% церебрална суспензия, получена от заразените мишки). В експерименталната и контролната група имаше 20 бели безпородни животни (по 12–13 g всяко). Panavir® (0,04–4 μg на мишка) се прилага интрамускулно (директно в портала на инфекцията) или коремно, пет пъти: 2 часа преди инфекцията и след това четири пъти с интервал от 48 часа. Контролните мишки получават същия обем физиологичен разтвор. Концентрацията на анти-рабдовирусните антитела се измерва имунохистохимично с помощта на комплекта BIO-RAD.
Ефектът срещу грипния вирус А е демонстриран in vitro, в клетъчната култура на MDCK и при млади бели безпородни мишки (9-11 g). Клетъчната култура MDCK е заразена с вирусната суспензия (щам A/WSN/1933, подтип H1N1) в доза от 0,01-10 ID50 на клетка. Panavir® се прилага 12 часа преди инфекцията или 6 часа след инфекцията (10, 100, 500 и 1000 μg на ml). Активността на разпространението на вируса се контролира от концентрацията на вируса в културалната среда 24 часа след инфекцията. Мишките са заразени интраназално с щам Aichi H3N2 2/68 на грип А вирус. Panavir® се прилага интравенозно (0,2 mg на мишка, 24 и 96 часа след инфекцията) [9].
Активността на Forvet® (животински аналог на Panavir®) е оценена спрямо коронавирусна инфекция при котки. Беше проведено разследване на 22 безплодни бездомни котки с коронавирусна инфекция, потвърдена от PCR. Шестнадесет котки бяха лекувани с Forvet® (1 ml 0,005% разтвор подкожно), пет пъти с интервал от един ден и след една седмица курсът беше повторен. Шест котки бяха използвани като контролна група. Ефектът от лечението се контролира от концентрацията на антикоронавирусните антитела в кръвта от един и пет месеца след прилагането на Forvet®. Концентрацията на антителата беше оценена с помощта на имунохистохимичен комплект, предназначен за диагностика на инфекциозен перитонит при котки (VetBioChim, Русия) [12].
2.2. Антибактериална активност
Защитната активност на Panavir® срещу бактериални инфекции беше изследвана при млади мъже (18–20 g) от белите безплодни мишки, заразени от Klebsiella pneumoniae или Shigella flexneri 516; и върху младите (190–230 g) женски от белите безплодни плъхове с индуциран фекален перитонит. Мишките от експерименталната група (20 животни на група) бяха третирани с Panavir® два пъти (0,4 ml 0,004% разтвор в коремната област): през първия и втория ден от експеримента (след инфекцията). Плъховете в експерименталната група (10 животни на група) са били третирани с Panavir® само веднъж (0,4 ml 0,004% разтвор на 100 g от живата маса, коремно), 4 часа преди инфекцията. Както мишките, така и плъховете в контролната група бяха третирани с физиологичен разтвор със същия обем като експерименталните животни. Мишките са заразени 4 часа след втората абдоминална инжекция на Panavir® или физиологичен разтвор. Суспензията на клетките K. pneumoniae се инжектира интравенозно (
10 4 CFU на мишка), докато Sh. клетките на flexneri се инжектират коремно (
5 · 10 8 CFU на мишка). Перитонитът при плъхове се предизвиква чрез абдоминално инжектиране на 20% фекална суспензия (0,4 ml на 100 g от живата маса).
3. Резултати
3.1. Антивирусна дейност
Panavir® демонстрира забележителния ефект срещу рецидивиращ генитален херпес при хора. В експерименталната група от 30 души (113 в контролната група) облекчаването на симптомите се наблюдава след 2,3 ± 0,1 дни, докато епителизацията на ерозивните фокуси се постига след 5,4 ± 0,1 дни от началото на лечението. В контролната група облекчението е регистрирано след 3,8 ± 0,2 дни, а епителизацията - само след 8,9 ± 1,1 дни [6].
Panavir® демонстрира забележителния положителен ефект срещу кърлежовия енцефалит. Мишките в експерименталната група демонстрират 30 ± 5% по-добра преживяемост, отколкото в контролната. Концентрацията на вирусните частици в мозъка на мишките, лекувани с Panavir®, е значително (2,5–3,0 lg) по-ниска, отколкото в контролната група. Това предизвика статистически значимото ускоряване на облекчаването на главоболието и замаяността, а също така принуди увеличаването на количеството на лимфоцитите (CD3 +, CD4 +, CD8 + и CD16 + клетки) и концентрацията на интерфероните 2α и γ [ 10].
Активността на Panavir® срещу рабдовирусна инфекция е демонстрирана при мишки, морски свинчета и кучета. Интрамускулното приложение на Panavir® в портала на инфекцията допринася за значителното намаляване на заболеваемостта (35–45%), увеличаване на преживяемостта (30–40%) и двукратно увеличаване на концентрацията на анти- рабдовирусни антитела в мозъка и кръвта на оцелелите мишки. Прилагането в корема е неефективно [11].
In vitro Panavir® демонстрира ефекта срещу грипния вирус А в доста високи концентрации (0,5–1,0 mg/ml). При тези концентрации и масивна инфекция (10 ID50 на клетка), концентрацията на вирусните частици в хранителната среда е два до четири пъти по-малка, отколкото в контролната култура. Ефектът е по-виден в случай на предварително приложение на лекарството. При мишки Panavir® причинява 25% увеличение на оцеляването (от 55 на 70%), докато средният живот на мъртвите животни се увеличава от 11,0 ± 0,3 на 13,0 ± 0,6 дни [9].
Panavir®/Forvet® демонстрира забележителния ефект срещу коронавирусната инфекция при котки. Три от шест контролни котки умряха в рамките на пет месеца от началото на експеримента, а само една от 16 котки умря в експерименталната група. В експерименталната група концентрацията на антителата срещу коронавируса намалява 4.8 ± 0.8 и 3.3 ± 0.6 пъти след един и пет месеца от лечението, докато в контролната група няма промени в концентрацията на антителата през първия месец на експеримент и само 1,5 ± 0,6 намаление след пет месеца (при оцелели животни) [12].
3.2. Активност срещу бактериални инфекции
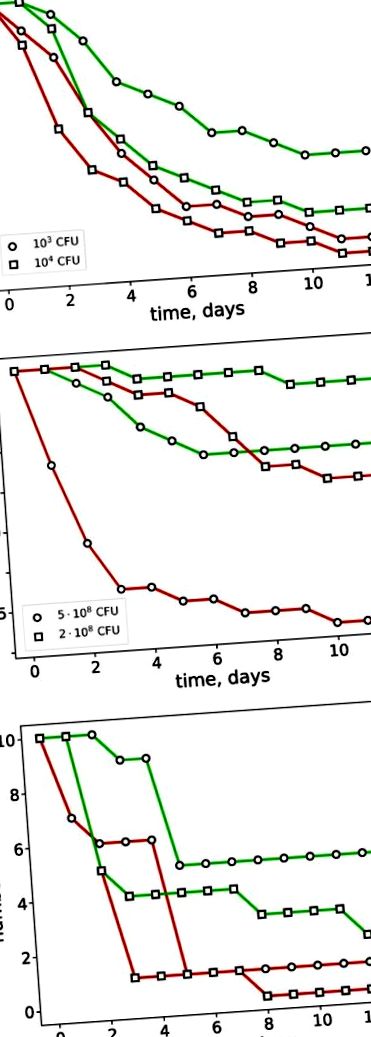
Според нашите резултати, Panavir® значително е увеличил оцеляването на животните, изложени на близка до леталната доза от причинителите на инфекцията. В модела на пневмония Panavir® причинява четирикратно увеличение на 12-дневната жизнеспособност (фиг. 1 А): от 10 до 40% (10 3 CFU на мишка) и от 5 до 20% (10 4 CFU на мишка ). В модела на бактериалния перитонит Panavir® също демонстрира значителен защитен ефект. При масивната инфекция (5 · 10 8 CFU на мишка) смъртността намалява от 85 на 30%, докато при по-леки условия (2 · 10 8 CFU на мишка) смъртността намалява от 40 на 10% (фиг. 1 Б) . Подобен ефект е получен при модела на фекалния перитонит при плъхове (фиг. 1 С). В контролната група 14-дневната смъртност от фекалния перитонит е била толкова висока, колкото 90–100%, докато приложението на Panavir® е намалило тази стойност до 50–80%. Следователно коремното приложение на Panavir® стана ефективно срещу инфекции с висока степен на смъртност, независимо от употребата преди или след инфекцията.
Динамиката на смъртността на мишки, заразени с Klebsiella pneumoniae (A) или Shigella flexneri (B) и плъхове, страдащи от фекален перитонит (C). Експерименталните групи (зелени криви) бяха третирани с Panavir®, докато контролните (червени криви) - не бяха. В С са представени резултатите от два независими експеримента.
4. Заключение
В заключение на нашия кратък доклад бихме искали да опишем нашия първи опит в използването на Panavir® срещу инфекцията с SARS-CoV-2. Към момента имаме само дванадесет субекта (на възраст от 22 до 56 години), страдащи от тежката форма на COVID-19, приели Panavir® и успешно се възстановили. Графикът на лечение включваше: 1. Пет интравенозни инжекции на Panavir® (5 ml от 0,004% разтвор), три с интервал от 24 часа и след това още две с интервал от 48 часа; 2. Азитромицин, 500 mg два пъти дневно, в продължение на три дни след първите три инжекции на Panavir®, след това 500 mg веднъж дневно в продължение на още три дни. Всички пациенти са се възстановили напълно в рамките на десет дни след първата инжекция на Panavir®. Осъзнаваме, че настоящата статистика за анти-COVID-19 активността на Panavir® е недостатъчна, но смятаме, че нашият опит трябва да бъде обявен за всички.
Изявление на авторите
Татяна С. Калинина: Разследване, концептуализация, писане - оригинален проект. Дмитрий В. Зленко: Проверка, писане - оригинален проект, писане - преглед и редактиране, визуализация. Алексей В. Киселев: Разследване. Александър А. Литвин: Разследване. Сергей В. Стовбун: Концептуализация, валидиране, писане - оригинален проект, надзор, администриране на проекти, придобиване на финансиране.
Бележки под линия
☆ Работата е завършена като част от държавното задание (номер на тема AAAA-A20-120013190076-0).
- Bell Peppers засилват метаболизма, активност, Trim Body Fat Journal на растителните лекарства
- Модификация на поведението и активност - Коалиция за действие при затлъстяване
- Цяла активност
- Ползи от физическа активност Физическа активност CDC
- 10-седмична програма за физическа активност за възрастен с хипертония със затлъстяване - Physiopedia