Дефицитът на протеин потиска съдържанието на липаза в тъканите и способността на ацинарните клетки да секретират липаза, като по този начин предполага защитен ефект срещу индуциран от етанол панкреатит.
Свързани термини:
- Липопротеин с висока плътност
- Хронично бъбречно заболяване
- Интелектуални увреждания
- Протеин
- Фенотип
- Мутация
- Недохранване
- Протеин за трансфер на холестеролов естер
- Затлъстяване
Изтеглете като PDF
За тази страница
Дефицит на протеин
Терминът „дефицит на протеини“ представлява състояние на относителен или абсолютен дефицит на телесни протеини или една или повече от незаменимите аминокиселини. „Протеиновият оборот“ отразява баланса на разграждането и ресинтеза на протеини. Повече синтез, отколкото разграждане, показва анаболно състояние, което изгражда чисти тъкани, повече разпадане, отколкото синтез, показва катаболно състояние, което изгаря чистите тъкани. Количествената връзка между концентрациите на циркулиращи аминокиселини и техния процент на катаболизъм не е еднородна нито между индивидите, нито между диетите. Постоянно високият или ниският прием на протеин води до цялостно увеличаване или намаляване на скоростта на катаболизъм на аминокиселини, която е частично независима от циркулиращите концентрации на аминокиселини. Въпреки че основната причина за недостиг на протеини е диета с недостиг на протеини, разстройството често може да се появи в различни патологични състояния. Диетичното лечение на дефицита на протеини зависи от причината за дефицита и трябва да зависи от доброто разбиране на основното заболяване, а основата на лечението включва балансирано добавяне на енергийни протеини и микроелементи.
Липопротеин и липиден метаболизъм
96.7.1.1 Клинични характеристики
Недостигът на CETP води до натрупване в плазмата на богат на СЕ голям HDL, в резултат на което се повишават плазмените концентрации на HDL холестерол и апо A-I и намаляват плазмените LDL холестерол и апо В (17). Няма специфични физически прояви, свързани с дефицит на CETP. Въздействието на генетичния дефицит на CETP върху риска от ССЗ е противоречиво, особено след като клинично изпитване с торцетрапиб, инхибитор на CETP, предизвика неочаквано увеличение на сърдечните смъртни случаи (109). Дефицитът на CETP може да е състояние на нарушена RCT, което може да доведе до атеросклероза въпреки високите плазмени нива на HDL холестерол (110) .
ПРОТЕИНИ | Недостиг
Лечение
Диетичното лечение на дефицита на протеини зависи от причината за дефицита. При пациенти с нефротичен синдром, характеризиращ се с огромни загуби на албумин в урината, приемът на протеин трябва да се увеличи до 90–120 g на ден за възрастни, когато чернодробният синтез на албумин може частично да компенсира загубите на урина. (Вижте KWASHIORKOR; MARASMUS.)
В случаи на остра бъбречна недостатъчност приемът на протеин трябва да бъде само 20 g на ден. Това намалява метаболизма на протеините и производството на урея. При пациенти с чернодробна цироза приемът на протеини също трябва да бъде намален, тъй като диетата с високо съдържание на протеини може да ускори чернодробната енцефалопатия.
Специални методи за хранене
Недостигът на протеини може да бъде лекуван чрез хранене със сонда, интравенозно хранене или допълнително хранене. Храненето със сонда е показано при пациенти с тежко недохранване, които не могат да се хранят. Парентералното хранене е от съществено значение, когато тънките черва не могат да смилат и усвояват хранителни вещества или след тежки наранявания като изгаряния.
При лек дефицит на протеин, увеличеният прием на протеин през устата е достатъчен, за да отговори на хранителните нужди. На пазара се предлагат няколко специални препарата, съдържащи високи нива на протеин.
Усложнения
Тъй като дефицитът на протеин често се придружава от инфекции, дехидратация и лишаване от витамини и електролити, тези състояния се нуждаят от специално внимание. Следователно в повечето случаи на тежък дефицит на протеин, лечението трябва да започне с заместване на течности и, ако е показано, с антибиотична терапия.
Липопротеинови нарушения
Дефицит на протеин за пренос на холестерилов естер (CETP)
Геномика и фармакогеномика на липидопонижаващите терапии
Недостиг на CETP
Дефицитът на CETP се наследява по автозомно-рецесивен начин, при който засегнатите индивиди имат мутации на загуба на функция и в двете копия на гена CETP. Това води до повишени нива на HDL-C и ниски нива на LDL-C поради неуспеха на CETP-задвижвания трансфер на холестеролови естери от HDL към апо В-съдържащи липопротеини като VLDL, IDL и LDL. Установени са няколко мутации и данните сочат, че това генетично заболяване е най-разпространено сред японската популация [41]. Двете най-често срещани мутации са G> A при +1 позиция на интрон 14 и D> G заместване в позиция 442 на екзон 15 (D442G), които съответно присъстват при приблизително 2% и 7% от японската популация. Като се има предвид, че инхибирането на активността на CETP води до по-ниско производство на атерогенни липопротеини, се предполага, че дефицитът на CETP е свързан с по-нисък риск от ССЗ [42]. Към днешна дата доказателствата са противоречиви, като някои проучвания предполагат нисък риск от ССЗ, свързан с дефицит на CETP, а някои показват двусмислени резултати. Този проблем се усложнява допълнително от текущия неуспех на фармакологичното инхибиране на CETP да има някаква полза върху сърдечно-съдовите резултати.
Дефицит на протеини и алкохол: Взаимодействия и органични ефекти
Ефекти на дефицита на протеин върху черния дроб
Дефицитът на протеин е свързан с чернодробни промени, включително чернодробна стеатоза, некроза на чернодробните клетки и повишено отлагане на фиброзна тъкан (Webber and Freiman, 1974). Тези промени са подобни на тези, наблюдавани при алкохолно увреждане на черния дроб. Всъщност дефицитът на етанол и протеин може да си взаимодейства, което води до по-тежко метаболитно разстройство и чернодробни лезии. Етанолът може да потисне синтеза на протеин при определени обстоятелства, ефект, споделен от протеинов глад (Rothschild et al., 1974). Дефицитът на протеин нарушава метаболизма на етанола, намалявайки чернодробния клирънс на етанол и дейностите на чернодробния алкохол дехидрогеназа и микрозомалната система за окисляване на етанол (MEOS), въпреки че намаляването на първата е по-слабо изразено и активността на MEOS дори се увеличава, ако дефицитът на протеин е придружен от консумация на етанол ( Wilson et al., 1986).
Фигура 1 . Връзка между чернодробната глутатион пероксидаза и теглото на плъховете в края на проучване, при което животните са били хранени с етанол и диета с дефицит на протеин в продължение на 5 седмици (González-Reimers et al., Непубликувани резултати).
Маса 1 . Чернодробна и мускулна глутатионпероксидаза (GPX, в mU/mg) и супероксиддисмутаза (SOD, в lU/mg), и концентрации на малондиалдехид (MDH, в nmol/mg тъкан) при плъхове, хранени изокалорично, 18% протеин- и 2 % диети, съдържащи протеини
| Черен дроб GPX | 54,9 ± 5,4 | 26,1 ± 3,8 | p Таблица 2). Възстановяването на чернодробната GPX активност може да възстанови антиоксидантния капацитет и е свързано с по-малко отлагане на фиброзна тъкан. Селенът действа като кофактор на GPX, като активността на този ензим е драматично зависима от концентрацията на селен. Въпреки това, метаболизмът на селен при алкохолно чернодробно заболяване и относителното тегло на дефицит на селен при липидно пероксидация не са известни. |
Таблица 2. Хистоморфометрично определени чернодробни мазнини и фиброза и съдържание на чернодробно желязо (чрез атомно-абсорбционна спектрофотометрия) при плъхове, третирани с етанол и диета с ниско съдържание на протеини, следвайки модела на Либер-ДеКарли
Етанол + 2% протеин (8)
Забележки: Различията между групите са оценени с помощта на теста на Student's-Newmann-Keuls (SNK). Цифрите в скоби показват броя на случаите (González-Reimers et al., Непубликувани данни).
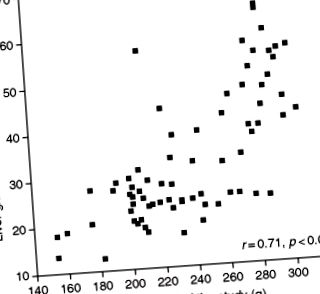
Натрупването на желязо благоприятства липидната пероксидация и е свързано с чернодробната стеатоза. Синергично взаимодействие между етанол и бедна на протеини диета по отношение на натрупването на чернодробно желязо е описано при плъхове, използвайки експерименталния модел на Либер-ДеКарли (Conde-Martel et al., 1992a). Претоварване с желязо се наблюдава в други ситуации на протеиново-калорично недохранване (Jackson, 1986). В проучване, проведено от нашата група върху 76 плъхове, следвайки експерименталния модел на Либер-ДеКарли в продължение на 5 седмици, се наблюдава значителна корелация между чернодробното желязо и загубата на тегло (Фиг. 2). Интересното е, че железните праймери Купферови клетки за активиране на ядрен фактор каппа В, поне при алкохолно увреждане на черния дроб (Tsukamoto et al., 1999) и повишеното насищане на трансферин са свързани с чернодробна фиброза при неалкохолен стеатохепатит (Angulo et al., 1999) - въпреки че тази връзка все още не е очевидна при многовариантния анализ - докато устойчивото желязо в чернодробната биопсия е рисков фактор за фиброза при алкохолно чернодробно заболяване (Raynard et al., 2002). Джордж и др. (1998) в поредица от 51 пациенти с неалкохолен стеатохепатит, при които 31% са хетерозиготни или хомозиготни по отношение на генната мутация на хемохроматозата, откриват връзка между чернодробното желязо и тежестта на чернодробната фиброза.
Фигура 2. Връзка между чернодробното желязо и теглото на плъховете в края на проучване, при което животните са били хранени с етанол и диета с дефицит на протеини в продължение на 6 седмици (González-Reimers et al., Непубликувани резултати).
По този начин, в допълнение към описаните ефекти на етанола върху метаболизма на чернодробния протеин и редуциращите ефекти на дефицита на протеин върху метаболизма на етанол, може да съществува връзка между дефицита на протеин и етанола по отношение на патогенетичния механизъм на увреждане на черния дроб. И в двете ситуации са наблюдавани повишена липидна пероксидация и променени запаси на желязо.
Хематологични прояви на системни заболявания
Протеиново-калорично недохранване
Дефицитът на протеин при наличието на адекватен прием на въглехидрати (kwashiorkor) се свързва с лека нормохромна, нормоцитна анемия, вторична за намаленото производство на червените кръвни клетки, въпреки нормалните или повишени нива на еритропоетин, както и намаленото оцеляване на червените клетки. Недохранването с протеинови калории също е свързано с нарушена функция на левкоцитите.
Скорбут
Леката анемия е често срещана. Има тенденция на кървене поради загуба на съдова цялост, което може да доведе до петехии, субпериостални, орбитални или субдурални кръвоизливи. Може да се появят хематурия и мелена.
Анорексия Нервоза
Той произвежда следните хематологични промени в по-напреднали етапи:
Желатинови промени в костния мозък, които могат да станат силно хипопластични
Лека анемия (макроцитна), неутропения и тромбоцитопения
Предразположение към инфекция, свързана с неутропения
Виждат се нередовно свити червени клетки (както при хипотиреоидизъм) вследствие на нарушение в състава на мембранните липиди.
Хематологични прояви на системни заболявания
Хранителни разстройства
Протеиново-калорично недохранване
Дефицитът на протеин при наличието на адекватен прием на въглехидрати (kwashiorkor) се свързва с лека нормохромна, нормоцитна анемия, вторична за намаленото производство на червените кръвни клетки, въпреки нормалните или повишени нива на еритропоетин, както и намаленото оцеляване на червените клетки. Протеиново-калоричното недохранване също е свързано с нарушена функция на левкоцитите.
Скорбут
Леката анемия е често срещана. Има тенденция на кървене поради загуба на съдова цялост, което може да доведе до петехии, субпериостални, орбитални или субдурални кръвоизливи. Може да се появят хематурия и мелена.
Анорексия Нервоза
Anorexia nervosa е свързана с хематологични промени, които могат да бъдат полезни при диагностицирането:
Морфологията на червените клетки е поразителна за необичайната морфология на акантоцитозата. Това се дължи на придобита хипобеталипопротеинемия, вторична вследствие на хранителна недостатъчност
Лека анемия (макроцитна), неутропения и тромбоцитопения
Леко предразположение към инфекция, свързана с неутропения
Желатинови промени в костния мозък, които могат да станат силно хипопластични.
Х-свързани лимфопролиферативни синдроми
Ким Е. Никълс, Ребека А. Марш, в имунната недостатъчност на Stiehm, 2014
Дефицит на XLP1/SAP
Въпреки че няма известни корелации генотип-фенотип при дефицит на SAP, податливостта към развитие на заболяването може да бъде свързана с нивата на SAP протеин и функционалната способност в общите лимфоцити. Това се доказва от факта, че близнаците с дефицит на SAP, които приютяват мутация на мястото на снаждане в SH2D1A, която позволява някои остатъчни експресии на SAP в лимфоцитите в периферната кръв, са останали здрави и в зряла възраст. 12 Освен това, експресията на дивия тип SAP само в малък процент лимфоцити може да бъде достатъчна за предотвратяване на проявите на заболяването. В подкрепа на това схващане, женските носители на мутации SH2D1A, които нямат експресия на SAP протеин в приблизително половината от Т и NK клетките поради случайно инактивиране на X-хромозома, не проявяват явни симптоми на XLP1. Въпреки че остава теоретичен риск от развитие на заболяване, ако настъпи сериозно изкривяване при лионизация в полза на клетки, които нямат експресия на SAP, доколкото ни е известно, това все още не е описано. И накрая, наскоро беше съобщено, че корекцията на мутацията SH2D1A чрез соматична реверсия в едва 1-2% от Т-клетките на периферната кръв води до повторна експресия на функционален SAP и може да допринесе за удължено оцеляване след EBV инфекция. 16.
- Нефролитиаза - общ преглед на ScienceDirect теми
- Нефросклероза - общ преглед на ScienceDirect теми
- Skinfold - общ преглед на ScienceDirect теми
- Натриев баланс - общ преглед на ScienceDirect теми
- Покой за разход на енергия - общ преглед на ScienceDirect теми