Анкит Бхарат
1 Медицински факултет на Северозападния университет във Файнберг, Чикаго, IL 60611, САЩ
Скот А. Кънингам
2 клиника Майо, Рочестър, MN 55905, САЩ
Г. Р. Скот Бъдингер
2 клиника Майо, Рочестър, MN 55905, САЩ
Даниел Крейсел
3 Вашингтонски университет, Сейнт Луис, МО 63110, САЩ
Charl J. DeWet
3 Вашингтонски университет, Сейнт Луис, МО 63110, САЩ
Андрю Е. Гелман
3 Вашингтонски университет, Сейнт Луис, МО 63110, САЩ
Кен Уейтс
4 Университет на Алабама в Бирмингам, Бирмингам, AL 35233, САЩ
Дона Краб
4 Университет на Алабама в Бирмингам, Бирмингам, AL 35233, САЩ
Ли Сяо
4 Университет на Алабама в Бирмингам, Бирмингам, AL 35233, САЩ
Сангета Бораде
1 Медицински факултет на Северозападния университет във Файнберг, Чикаго, IL 60611, САЩ
Намасиваям Амбалаванан
4 Университет на Алабама в Бирмингам, Бирмингам, AL 35233, САЩ
Даниел Ф. Дилинг
5 Университет Лойола, Чикаго, Медицинско училище „Стрич“, Чикаго, IL 60153, САЩ
6 Hines VA Hospital, Hines, IL, САЩ
7 RML Specialty Hospital, Hinsdale, IL 60521, САЩ
Ерин М. Лоуъри
5 Университет Loyola University Chicago Stritch School of Medicine, Чикаго, IL 60153, САЩ
Тод Астор
8 Обща болница в Масачузетс, Харвардско медицинско училище, Бостън, Масачузетс 02114, САЩ
Рамзи Хахем
3 Вашингтонски университет, Сейнт Луис, МО 63110, САЩ
Александър С. Крупник
3 Вашингтонски университет, Сейнт Луис, МО 63110, САЩ
Малкълм М. ДеКемп
1 Медицински факултет на Северозападния университет във Файнберг, Чикаго, IL 60611, САЩ
Майкъл Г. Исън
1 Медицински факултет на Северозападния университет във Файнберг, Чикаго, IL 60611, САЩ
Робин Пател
2 клиника Майо, Рочестър, MN 55905, САЩ
Свързани данни
Таблица S2. Протокол за лечение на хиперамонемия.
Таблица S3. Резултати от микробиологични анализи върху индексния пациент.
Резюме
ВЪВЕДЕНИЕ
РЕЗУЛТАТИ
Индексен случай
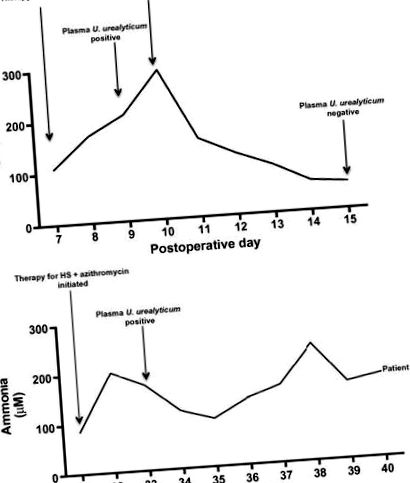
(A) Първоначална поява на хиперамонемия при пациент с индекс. (Б.) Повторение на хиперамонемия при индекса на пациента и отговор на терапията.
Молекулярна диагностика
маса 1
ХОББ, хронична обструктивна белодробна болест; PF, белодробна фиброза; CF, муковисцидоза; IPF, идиопатична белодробна фиброза.
| Индекс на пациента | Плазма (ден 5) | PCR | Отрицателни | 44 години; мъжки пол; саркоидоза; двустранна белодробна трансплантация; оцеляване, 40 дни |
| Плазма (ден 9, преди азитромицин) | PCR | U. urealyticum | ||
| Плазма (ден 15, на азитромицин) | PCR | Отрицателни | ||
| Плазма (ден 33, на азитромицин, рецидив на хиперамонемия) | PCR | U. urealyticum | ||
| Пикочен мехур (прясно, след смъртта) | PCR | U. urealyticum | ||
| Бели дробове (прясно, след смъртта) | PCR | U. urealyticum | ||
| Бели дробове (прясно, след смъртта) | Култура | U. urealyticum * | ||
| Черен дроб (прясно, след смъртта) | PCR | U. urealyticum | ||
| Далак (прясно, след смъртта) | PCR | U. urealyticum | ||
| Изтекъл пациент 1 † | Белият дроб (фиксиран с формалин парафин) | PCR | U. urealyticum | 59 години; мъжки пол; ХОББ; двустранна белодробна трансплантация; оцеляване, 10 дни |
| Изтекъл пациент 2 † | БАЛ | PCR | U. parvum, M. hominis | 64 години; мъжки пол; IPF; двустранна белодробна трансплантация; оцеляване, 16 дни |
| Пълна кръв (EDTA) | PCR | U. parvum, M. hominis | ||
| Изтекъл пациент 3 † | БАЛ | PCR | U. urealyticum | 59 години; мъжки пол; IPF; двустранна белодробна трансплантация; оцеляване, 21 дни |
| Бели дробове (фиксиран с формалин парафин) | PCR | U. urealyticum | ||
| Черен дроб (фиксиран с формалин парафин) | PCR | U. urealyticum | ||
| Потенциален случай 1 | BAL (ден 12 преди лечение с уреаплазма) | PCR и култура | U. parvum | 52 години; женски пол; IPF; двустранна белодробна трансплантация; жив на 6 месеца |
| Кръв (ден 12 преди лечение с уреаплазма) | PCR | U. parvum | ||
| BAL (ден 19, след лечение) | PCR и култура | Отрицателни | ||
| Кръв (ден 19, след лечение) | PCR | Отрицателни | ||
| Потенциален случай 2 | BAL (ден 42 преди лечение с уреаплазма) | PCR и култура | U. parvum | 55 години; женски пол; IPF; двустранна белодробна трансплантация; жив на 4 месеца |
| Кръв (ден 42 преди лечение с уреаплазма) | PCR | U. parvum | ||
| Отрицателни контроли (n = 15) ‡ | BAL (архивирани образци) | PCR | Отрицателни | Пациенти с документирано нормални концентрации на амоняк. Средна възраст, 54,5 ± 5,3 години. Имал ХОББ (50%), PF (35%) или CF (15%). |
| Серум (архивирани проби) | PCR | Отрицателни | ||
| Отрицателни контроли (n = 5) § | БАЛ | PCR и култура | Отрицателни | |
| Пълна кръв | PCR и култура | Отрицателни |
Допълнителни пациенти с хиперамонемия и контролна кохорта
След това тествахме BAL течност и серум, събрани от 20 реципиенти на белодробна трансплантация, които са документирали нормални концентрации на амоняк 1 до 7 дни след трансплантацията; всички са PCR-отрицателни за U. urealyticum, U. parvum и M. hominis. Култури могат да бъдат получени от петима от тези пациенти и също са отрицателни за същите три организма (Таблица 1).
Проспективно валидиране
Въз основа на тези резултати тествахме за уреаплазмени организми в кръв и BAL течност от 52-годишна жена, която претърпя двустранна белодробна трансплантация във Вашингтонския университет (Сейнт Луис, Мисури) за интерстициална белодробна болест, усложнена от рефрактерна хиперамонемия 9 дни по късно. И двата екземпляра са положителни за U. parvum чрез PCR, а BAL течната култура е положителна за U. parvum, но отрицателна за U. urealyticum или M. hominis. Два дни след започване на терапия с левофлоксацин и азитромицин, концентрацията на амоняк се нормализира и психическият й статус се нормализира (фиг. 2). След 7 дни антимикробно лечение, както BAL течността, така и кръвта са отрицателни за U. parvum и не е имало рецидив на хиперамонемия за 6 месеца проследяване.
Проспективно валидиране на връзката на уреаплазма с хиперамонемия след белодробна трансплантация.
ДИСКУСИЯ
HS е често фатално усложнение на системната имуносупресия, включително свързаното с трансплантация на бели дробове и други твърди органи; ниската му честота обаче възпрепятства систематичното изследване на нейната етиология и изключва рандомизирани проучвания на потенциални терапии (1, 6, 9-12). Тук представяме доказателства, които предполагат, че системната инфекция с видове Ureaplasma играе причинно-следствена роля в развитието на хиперамонемия. Намерихме доказателства за системна инфекция или с U. urealyticum, или с U. parvum при всички пациенти с HS след трансплантация на белия дроб и нито един от 20 пациенти с контролна белодробна трансплантация без разстройството. При трима засегнати пациенти лечението с антимикробни средства, насочени към видовете Ureaplasma, е свързано с разрешаване както на биохимичните, така и на неврологичните аномалии. Повтарящата се хиперамонемия при един от тези пациенти е придружена от дисеминирана инфекция с щам Ureaplasma, който вероятно е придобил антибиотична резистентност.
МАТЕРИАЛИ И МЕТОДИ
Култура
Културата на U. urealyticum, U. parvum и M. hominis се извършва в клиниката Mayo и в Quest Diagnostic Nichols Institute. Образците се култивират върху A8 плочи от агар (Hardy Diagnostics) в анаеробна атмосфера при 35 ° С в продължение на 6 седмици. Културните плочи се изследват чрез инвертирана светлинна микроскопия поне веднъж седмично. Подозрителните колонии бяха потвърдени чрез PCR в реално време (21). Възстановените изолати се субкултивират и инкубират в продължение на 48 часа. Субкултурният материал се поставя в транспортна среда M5 (Remel) и се замразява при -20 ° C за транспорт до Университета на Алабама в Бирмингам (UAB) за тестване на чувствителност.
Изпитване за чувствителност към антибиотици
Стойностите на минималната инхибиторна концентрация бяха определени чрез микроразреждане на бульон в 10В бульон (22), в съответствие с насоките на Института за клинични и лабораторни стандарти (http://clsi.org/blog/2011/11/11/clsi-publishes-a-guideline- на методи за тестване за антимикробна чувствителност-за-човешки микоплазми-m43 /) (22).
Профилиране на PCR и молекулярно съпротивление
PCR за U. parvum, U. urealyticum и M. hominis е извършена в клиниката Mayo, както е описано по-горе (21). ДНК на геномна U. urealyticum се пречиства с помощта на QIAamp DNA Mini Kit Kit (Qiagen). Запазените региони на рибозомни протеини L4 и L22 гени и два цели 23S rRNA оперона бяха амплифицирани с помощта на публикувани праймери (23, 24). PCR се извършва с Platinum PCR SuperMix (Invitrogen) върху Veriti 96-гнездов термичен циклер (Applied Biosystems). PCR продуктите бяха почистени чрез USB ExoSAP-IT (Affymetrix) и секвенирани с помощта на технологията Sanger в UAB. Последователностите са сравнени със съответните генни последователности на 14 макролидно-чувствителни щамове от тип американска колекция от култури (ATCC) на U. parvum (serovar 1, ATCC 27813; serovar 3, ATCC 27815; serovar 6, ATCC 27818; и serovar 14, ATCC 33697 ) и U. urealyticum (серовар 2, ATCC 27814; серовар 4, ATCC 27816; серовар 5, ATCC 27817; серовар 7, ATCC 27819; серовар 8, ATCC 27618; серовар 9, ATCC 33175; серовар 10, ATCC 33699; серовар 11, ATCC 33695; serovar 12, ATCC 33696; и serovar 13, ATCC 33698), използвайки CLC DNA Workbench 7.5 (Qiagen).
Допълнителен материал
Допълнителен материал
Таблица S1. Тестове за чернодробна функция и резултати от анализи на серум и урина за вродени грешки в метаболизма.
Таблица S2. Протокол за лечение на хиперамонемия.
Таблица S3. Резултати от микробиологични анализи върху индексния пациент.
Благодарности
Благодарим на изключителния персонал на клиничната лаборатория по клинична микробиология в клиниката Mayo, лабораторията за диагностична микоплазма към UAB и Quest Diagnostics за извършване на анализи, използвани за откриване на видове Ureaplasma, и M. E. Wylam и колеги, които се грижат за пациент с изтекъл срок на годност 2.
- Премахване на хранителните разстройства по основната причина - Хедър Дейн
- Хранителните алергии като причина за нощно напикаване - TheraPee
- Може ли вашата диета да причини инфекции с дрожди; Диетата на кандида
- Хранителните алергии могат да бъдат свързани с инфекция на ушите
- Хранителна алергия при инфекция с човешки имунодефицитен вирус (ХИВ) - PubMed