Лорънс А. Лайтер
1 отдел по ендокринология и метаболизъм, Институт за знания Li Ka Shing на болница „Сейнт Майкъл“, Университет в Торонто, 61 Queen Street East, # 6121Q, Торонто, ON M5C 2T2 Канада
Марина В. Шестакова
2 Институт за захарен диабет, Изследователски център по ендокринология и M.I. Първи Московски държавен медицински университет, Москва, Руска федерация
Илхан Сатман
3 Отдел по ендокринология и метаболизъм, Катедра по вътрешни болести, Медицински факултет в Истанбул, Университет в Истанбул, Истанбул, Турция
Свързани данни
Някои от данните, съобщени в ръкописа, са представени на 11-ия конгрес на Международната федерация по диабет в Западен Тихоокеански регион в Тайпе, Тайван, 27–30 октомври 2016.
Наборите от данни, използвани и/или анализирани по време на настоящото проучване, са достъпни от съответния автор при разумна заявка.
Резюме
Заден план
Въпреки че броят на антихипергликемичните агенти се е увеличил значително, сулфонилурейните продукти (по-специално гликлазид) остават важна опция поради различни фактори за пациентите и здравната система. Голямото, реално наблюдавано и международно проучване EASYDia оценява ефективността на гликлазид с модифицирано освобождаване (MR) 60 mg при лица с диабет тип 2 с широк спектър от анамнеза за диабет, индекс на телесна маса (ИТМ) и фоново антихипергликемично лечение.
Методи
Общо на 7170 участници от осем държави, на възраст ≥ 35 години с HbA1c ≥ 7,5% и не лекувани с инсулин, са предписани 30–120 mg гликлазид MR 60 mg веднъж дневно. Целите на HbA1c са индивидуализирани и дозирането е повишено, според изискванията, в рамките на 6-месечното проучване. В тази post hoc субанализа крайните точки за ефикасност бяха анализирани според стратифицирани изходни нива на HbA1c, режими на тегло и понижаване на глюкозата. Документирани са епизоди на хипогликемия, изискващи помощ.
Резултати
На изходно ниво средната възраст е била 58,9 години, HbA1c 8,8%, ИТМ 30,1 kg/m 2 и продължителност на диабета 5,1 години. В края на проучването са отбелязани клинично значими подобрения на HbA1c (средна промяна - 1,78%) във всички изходни слоеве на HbA1c (> 7,0 до ≤ 8,0%,> 8,0 до ≤ 9,0%,> 9,0 до ≤ 10,0% и> 10,0%), Класификации на ИТМ (18,5 до 2) и независимо от първоначалния режим на лечение на диабет (P 2, който регистрира загуби на тегло съответно от 0,9 и 2,2 kg (P 2 подгрупа спечели средно 0,5 kg (P 2. Хора с най-висок изходен HbA1c и ИТМ преживява най-големите подобрения на HbA1c и теглото.
Пробна регистрация ISRCTN Регистър ISRCTN00943368 на 1 юли 2011 г.
Заден план
Действието при диабет и съдови заболявания: Проучването с контролирано оценяване с модифицирано освобождаване на Preterax и Diamicron (ADVANCE) [1–3] демонстрира, че прогресивното повишаване на състава на гликлазид с модифицирано освобождаване (MR) като част от интензивен режим на лечение осигурява последователен гликемичен контрол, свързан с дългосрочни ползи от комбинираната микроваскуларна и макросъдова крайна точка. Въпреки наличието на по-нови класове антихипергликемични средства, сулфонилурейните продукти (по-специално гликлазид) все още запазват важна позиция в управлението на диабета поради съображения около запознатост, препоръки за насоки, цена и покритие [4–12].
С основната цел за подобряване на придържането, лекарствената форма на гликлазид MR 60 mg веднъж дневно (QD) се предлага като таблетка с делителна черта, за да се осигури удобно титруване. Ефективността и поносимостта на тази таблетка гликлазид са оценени в реалното проучване ObsErvationAl, за да се анализира титруването на Diamicron MR 60 mg в ежедневната клинична практика при голяма популация с неконтролирано проучване на диабет тип 2 (EASYDia). След 6 месеца прогресивно повишаване, хората в кохортата EASYDia са имали значително подобрен гликемичен контрол, лека загуба на тегло и редки събития на хипогликемия [13]. Тук описваме времевата и свързаната с дозата ефикасност на гликлазид MR 60 mg, колко ефикасността варира в зависимост от изходните характеристики на участниците и потенциалните клинични последици от тези наблюдения.
Методи
Проучване и популация
EASYDia беше международно, отворено, нерандомизирано, несравнително наблюдателно проучване (ISRCTN00943368), проведено в съответствие със стандартите и принципите на Декларацията от Хелзинки. Етичното одобрение е специфично за обекта и писмено информирано съгласие, получено при или преди базовото посещение.
Прожекцията се проведе от юли 2011 г. до февруари 2014 г. на 596 обекта в осем държави (Армения, Грузия, Ливан, Малайзия, Русия, Словения, Швейцария и Турция). Потенциалните участници трябваше да изпълнят всички изброени по-долу критерии: ≥ 35 години с диабет тип 2, HbA1c ≥ 7,5% и нелекувани или неинсулинови антихипергликемични терапии. Лица, които са били бременни или кърмят, показват свръхчувствителни реакции към сулфонилурейни продукти, показват тежка чернодробна или бъбречна недостатъчност (креатининов клирънс 7,0 до ≤ 8,0%,> 8,0 до ≤ 9,0%,> 9,0 до ≤ 10,0% и> 10,0%), тяло индекс на масата (ИТМ 18,5 до 2) и предходни режими за понижаване на глюкозата. Що се отнася до хипогликемията, във формулярите за доклад за случая бяха събрани само тежки епизоди. Тежките хипогликемични инциденти бяха класифицирани като тези, свързани с преходна дисфункция на централната нервна система без друга очевидна причина, при която индивидът не можеше да се лекува сам и се нуждаеше от помощ от друга страна.
статистически анализи
Демографските данни и други базови характеристики се отчитат за включения набор. Информацията за FPG и HbA1c е получена от пълния набор за анализ [FAS; участници, които са приели поне една доза от изследваното лечение, която им е била предписана и са имали поне една изходна стойност и една след изходната стойност на FPG (или HbA1c) в досието]. Резултатите от теглото бяха изчислени от комплекта за безопасност. Освен ако не е посочено друго, данните се представят като средни стойности (стандартно отклонение, SD). Промените от съответните изходни стойности се оценяват с тест с ранг на Wilcoxon и двустранен 95% интервал на доверие. Статистическата значимост е определена при некоригирана P стойност 1. Накратко, около две пети от участниците в EASYDia бяха мъже; изходната възраст на кохортата беше 58,9 (10,6) години, BMI 30,1 (5,0) kg/m 2, FPG 10,2 (2,8) mmol/L и HbA1c 8,8 (1,3)%. Над 44% от участниците в EASYDia са имали ИТМ на изходно ниво, който е бил 30 kg/m 2 или по-голям, докато 12 и 42% са документирали стойности на ИТМ съответно на изходно ниво от 18,5 до 24,9 и 25,0 до 2. Приблизително две трети от участниците са имали изходно ниво на HbA1c, което е> 8,0%. Около половината от кохортата е ново диагностицирана, което прави изходната продължителност на диабета на 5.1 (4.4) години. Метформин е най-често използваният орален антихипергликемичен агент при влизане в проучването. Когато се обмислят профили на антихипергликемична терапия преди проучването, повечето от участниците са били или нелекувани с лекарства, или лекувани с монотерапия с метформин; много малко се лекуват с двойна терапия, която включва или сулфонилурейно производно, или DPP-4i в комбинация с метформин.
маса 1
Демографски данни на кохортата EASYDia въз основа на предварително зададен изходен индекс на телесна маса и стратификация на HbA1c
| Демография | |
| Мъже a | 2949 (41,5) |
| Възраст (години) * | 58,9 (10,6) |
| Изходен индекс на телесна маса (kg/m 2) b | |
| 18,5 до c | |
| > 7,0 до ≤ 8,0 | 1765 (17.4) |
| > 8,0 до ≤ 9,0 | 2074 (47.1) |
| > 9,0% до ≤ 10,0 | 809 (18,4) |
| > 10,0 | 758 (17,2) |
Данните са представени като n (%) или * средно (стандартно отклонение)
a Полът на 63 (0,88%) участници не е докладван; b Данни, събрани от комплекта за безопасност; c Данни, събрани от пълния набор за анализ
Ефективност на гликлазид MR
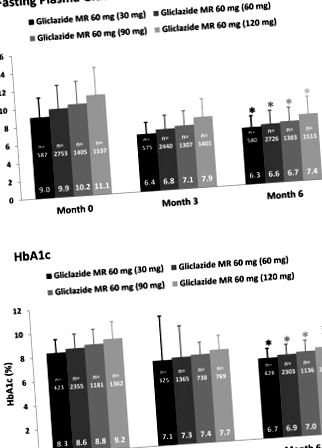
По-рано се съобщава, че постепенното дозиране на гликлазид MR за период от 6 месеца (действителната средна продължителност на лечението при FAS е била 5,6 ± 1,1 месеца) е свързано с временни подобрения в гликемичния контрол в кохортата на EASYDia [13]. Всъщност тези ползи са очевидни в рамките на 3 месеца след започване на проучването. На 3 и 6 месец нивата на FPG за цялата кохорта са средно съответно 7,1 (1,7) и 6,8 (1,7) mmol/L; това представлява подобрение от 3,4 (2,8) mmol/L (P 1 показва временните промени в FPG и HbA1c, когато участниците в EASYDia са били стратифицирани според дозата гликлазид MR, предписана на месец 6. По-специално, подкохортата е определила най-високата доза гликлазид (120 mg QD) на 6-ия месец в началото на проучването е имала най-високите средни FPG и HbA1c съответно от 11,1 mol/L и 9,2% .Средните разлики в изходните стойности на FPG и HbA1c между тези, приемащи гликлазид MR 30 mg и гликлазид MR 120 mg на 6-мия месец са съответно 2,1 mmol/L и 0,9%. На 3-ия месец сравненията между същите групи дават по-малки разлики от 1,5 mmol/L за FPG и 0,6% за HbA1c. Въпреки че разликата между двете групи, на 6-ия месец, за FPG се стеснява допълнително до 1,1 mmol/L, това за HbA1c не показва по-нататъшно подобрение.Същите тенденции на спад се наблюдават, когато средните стойности на FPG и HbA1c се сравняват между 6-ия месец гликлазид MR 60 mg и гликлазид MR 120 mg групи, както и месеца 6 гликлазид MR 90 mg и гликлазид MR 120 mg ръце (фиг. 1). Тези открития предполагат, че стратегията за прогресивно повишаване на състава на гликлазид MR е свързана с подобрения в гликемичния контрол.
Временни и свързани с дозата подобрения в (а) FPG и (б) HbA1c, стратифициран според MR 6 дозата на гликлазид 6 месеца. * P 10,0%) и най-малко в слоя с най-ниските изходни стойности на HbA1c (> 7,0– ≤ 8,0%) (фиг. 2 а). Подобрения в гликемичния контрол бяха очевидни още през месец 3 във всичките четири изходни слоя HbA1c (фиг. 2 b). За отбелязване е, че на 6-и месец почти половината от тези в изходната група HbA1c> 10,0% са постигнали HbA1c ≤ 7,0%. По-нататъшен интерес представлява наблюдението, че на 3-ти месец и четирите изходни подгрупи HbA1c включват индивиди, чийто HbA1c е спаднал до под 6,5% (фиг. 2 б).
HbA1c понижаваща ефикасността на гликлазид MR (а) на месец 6 като стратифициран по изходно ниво HbA1c и (б) както е определено от постигането на HbA1c ≤ 7,0 и ≤ 6,5% на месеци 3 и 6. n = 1765 за групата „> 7,0 до ≤ 8,0%“; n = 2074 за групата „> 8,0 до ≤ 9,0%“; n = 809 за групата „> 9,0 до ≤ 10,0%“ и n = 758 за групата „> 10,0%“. * P 2) на месец 6.
Стратификацията според режимите на лечение на диабет преди проучване, сред които бяха преминавания от друга сулфонилурея или инхибитор на дипептидил пептидаза-4 (DPP-4i), разкри значителни подобрения на HbA1c с гликлазид MR във всички четири изследвани слоя (Фиг. 3 а; P 3 б). Освен това на 6-ти месец над половината от тези, които са преминали от друга сулфонилурейна киселина или от DPP-4i, са постигнали целта HbA1c ≤ 7,0%; по-строгата цел HbA1c ≤ 6,5% е постигната на 6-и месец от повече от две пети от тези, които първоначално са били на DPP-4i (фиг. 3 б).
HbA1c понижаваща ефикасността на гликлазид MR (а) на месец 6 като стратифициран от изходните стратегии за понижаване на глюкозата и (б) както се дефинира от постигането на HbA1c ≤ 7,0 и ≤ 6,5% на месеци 3 и 6. n = 1142 за групата „Ново диагностицирана или нелекувана с лечение“; n = 2550 за групата „Добавка към MET“; n = 819 за групата „Превключване от SU“ и n = 249 за групата „Превключване от DPP-4i“. * P 2) регистрира статистически значими загуби на тегло през месец 6 (и двата P 2 получават средно 0,54 (4,04) kg за същия период от време (Фиг. 4; P 2 ”група; n = 3029 за„ 25,0 до 2 ”) група и n = 3191 за групата „≥ 30 kg/m 2". * P = 0,02 и † P 2 и по-горе. За отбелязване е, че изходните стойности на ИТМ от 25,0 kg/m 2 и по-високи са свързани със значителни загуби на тегло. Както се вижда при много антихипергликемични агенти, участниците с най-високи изходни нива на HbA1c и ИТМ са имали най-големи HbA1c и подобрения в теглото, докато обратното е вярно за тези в най-ниските изходни слоеве на HbA1c и ИТМ.
През последните 5 години се наблюдава постоянен поток от публикации, фокусирани върху сърдечно-съдовата и бъбречната безопасност, както и сигналите за ефикасност на нови лекарства за диабет в големи кохорти от диабет тип 2, повечето от които са познавали сърдечно-съдови заболявания [14–23]. Докато резултатите от тези мегатриали са породили много вълнение, макар и наред с някои опасения относно по-новите класове антихипергликемични средства, сулфонилурейните продукти, по-специално гликлазидът, остават важна възможност за лечение за много лекари и пациенти, когато нивата на глюкозата остават повишени въпреки максимално поносимата доза метформин [4–12].
Освен метформин, единственият друг перорален антихипергликемичен агент, цитиран във версията от 2017 г. на списъка на основните лекарства на Световната здравна организация е гликлазид [9]. По същата вена, няколко национални насоки [6, 10, 11] понастоящем позиционират гликлазид като избор от втора линия, един препоръчва ранно започване на гликлазид MR или глимепирид [12], докато друг [4] предлага добавяне на сулфонилурея, DPP- 4i, пиоглитазон или двойна комбинация от трите, когато максимално поносимата монотерапия с метформин не постига желания гликемичен резултат. Трябва да се отбележи, че гликлазид MR се препоръчва и широко се използва за лечение на диабет по време на Рамадан [24-26], период, през който продължителното гладуване може да направи управлението на гликемията предизвикателно. Препоръките на тези професионални групи ясно подкрепят постоянната роля на гликлазид MR в съвременното управление на диабета.
Рискът от хипогликемия остава важно съображение при лечението и е основна бариера за спазването на лекарствата, като по този начин възпрепятства постигането на гликемичните цели. Тежките хипогликемични епизоди са необичайни, дори сред участниците със само умерено повишаване на гликемията, като само четири инцидента са докладвани от четирима участници в EASYDia (0,06%). При по-нататъшна оценка обаче беше отбелязано, че само трима от тези индивиди са преживели общо четири събития, за които се подозира, че са свързани с гликлазид (0,04%). Нечестите прояви на тежка хипогликемия отразяват ниския риск от хипогликемия (по отношение на други сулфонилурейни продукти), съобщаван при гликлазид MR в последните ретроспективни кохортни проучвания (P 2 и по-високи, също са имали значителна загуба на тегло. лечение, намалява важна загриженост, рутинно заобикаляща сулфонилурейния клас.Като цяло, тези данни подчертават, че описаният режим на гликлазид MR е ефективна опция за голямо разнообразие от лица, не лекувани с инсулин с диабет и неадекватен гликемичен контрол.
Принос на авторите
LAL допринесе за разработването на концепцията и дизайна на изследването, интерпретира резултатите, написа, прегледа и критично преразгледа ръкописа за важно научно и интелектуално съдържание. MVS беше националният координатор за Русия, прегледа и критично преразгледа ръкописа за важно интелектуално съдържание. IS беше национален координатор за Турция, интерпретира резултатите, прегледа и критично преразгледа ръкописа за важно научно и интелектуално съдържание. Всички автори прочетоха и одобриха окончателния ръкопис.
Благодарности
Авторите признателно оценяват приноса на пациентите, клиницистите и изследователските екипи на EASYDia. Д-р Hwee Teoh на HTaq Biomedical Editorial and Education Services Inc. е финансиран от Institut de Recherches Internationales Servier (Франция) и е признат за писане и редакторска подкрепа.
Конкуриращи се интереси
LAL получи подкрепа за безвъзмездна помощ за научни изследвания и/или хонорари за лектори/консултанти от AstraZeneca, Boehringer Ingelheim, Eli Lilly, GlaxoSmithKline, Janssen, Merck, Novo Nordisk, Sanofi и Servier. MVS е получил подкрепа за безвъзмездна финансова помощ и/или хонорари за лектори/консултанти от Astra Zeneca, Eli Lilly, MSD, Novo Nordisk, Novartis, Sanofi и Servier. IS е получила подкрепа за безвъзмездна финансова помощ и е служила като лектор или съветник без пряко финансово обезщетение от договори между нейния работодател и следните компании: AstraZeneca, MSD, Novo Nordisk, Sanofi и Servier.
Наличност на данни и материали
Някои от данните, съобщени в ръкописа, са представени на 11-ия конгрес на Международната федерация по диабет в Западен Тихоокеански регион в Тайпе, Тайван, 27–30 октомври 2016.
Наборите от данни, използвани и/или анализирани по време на настоящото проучване, са достъпни от съответния автор при разумна заявка.
Съгласие за публикуване
Етично одобрение и съгласие за участие
EASYDia беше международно, отворено, нерандомизирано, несравнително наблюдателно проучване (ISRCTN00943368), проведено в съответствие със стандартите и принципите на Декларацията от Хелзинки. Етичното одобрение е специфично за обекта и писмено информирано съгласие, получено при или преди базовото посещение.
Финансиране
Тази работа беше подкрепена от Institut de Recherches Internationales Servier (Франция). Мненията, изразени в този материал, са на авторите и не отразяват непременно възгледите на Institut de Recherches Internationales Servier (Франция).
Бележка на издателя
Springer Nature остава неутрален по отношение на юрисдикционните претенции в публикувани карти и институционални принадлежности.
- Клинична ефективност на лираглутид при лечение на диабет тип 2 в реалния свят А
- Glucerna, Enterex или Ensure - кой от тях е най-подходящ за диабетно хранене - диабет тип мен
- Диета, физическа активност или и двете за профилактика или забавяне на захарен диабет тип 2 и неговите
- GLP-1 аналогов лираглутид като допълнително лечение при диабет тип 2 след неуспешен бариатричен метаболизъм
- Глобален пазар за диети за отслабване и управление на теглото по производители, региони, видове и