Винченцо Рочира
1 Ендокринологичен отдел, Катедра по биомедицински, метаболитни и невронни науки, Университет в Модена и Реджо Емилия, Via P. Giardini 1355, 41126 Модена, Италия
2 Azienda USL di Modena, Nuovo Ospedale Civile Sant'Agostino Estense (NOCSAE), Via P. Giardini 1355, 41126 Modena, Италия
Елда Кара
1 Ендокринологичен отдел, Катедра по биомедицински, метаболитни и невронни науки, Университет в Модена и Реджо Емилия, Via P. Giardini 1355, 41126 Модена, Италия
Чезаре Карани
1 Ендокринологичен отдел, Катедра по биомедицински, метаболитни и невронни науки, Университет в Модена и Реджо Емилия, Via P. Giardini 1355, 41126 Модена, Италия
Резюме
1. Въведение
При мъжките мъже тестостеронът (Т) и естрадиолът (Е2) са основните циркулиращи полови стероиди, действащи върху костната тъкан. Първият се произвежда от клетките на Leydig в тестиса, докато вторият произтича от ароматизацията на андрогените посредством ензимния комплекс на ароматазата [1]. Ароматазата е цитохром Р450 ензим, кодиран от гена CYP19A1, който играе ключова роля в биосинтеза на естроген: катализира превръщането на Δ 4 -андростендион в естрон и този на Т в Е2 [2, 3]. Ароматазата се изразява широко в голям брой тъкани като тестиси (клетки на Сертоли и Лейдиг), яйчници (гранулозни клетки и лутеален корпус), мозък (включително хипоталамус), космени фоликули и фибробласти [2, 3]. Мастната тъкан също изразява ароматаза и представлява важен източник на естрогени, особено при мъжете [1–4]. Всъщност при мъжете Е2 се произвежда главно от тестисите и на второ място от мастната тъкан [2–4]. Биологичните действия на естрогените се медиират от техния рецептор (ER), който принадлежи към семейството на ядрените рецептори и към днешна дата са идентифицирани две различни ER: ER-α и ER-β [5]. Описан е по-нататъшен негеномен път на действие на естрогена, който вероятно включва взаимодействие на плазмената мембрана на ER [6, 7].
Модели на животни [8, 9] и хора [10, 11] на вродения дефицит на естроген при мъжете предлагат нов сценарий, полезен за по-добро разбиране на естрогенните ефекти върху мъжката кост, както и върху няколко органа и тъканите при мъжете [12–14]. Всички тези физиологични действия на естрогените при мъжете остават пренебрегвани дълго време (вж. [13] за преглед). В миналото естрогенът също се считаше погрешно за незаменим за имплантиране на бластоцисти [15] и се предполага, че вродените естрогенни дефекти са несъвместими с живота [10, 11]. Откриването на първите случаи на вродени естрогенни дефекти при хората позволи да се разбере, че дефицитът на ароматаза се дължи на мутации на гена, кодиращ ензимния комплекс на ароматазата, което води до липса на синтез и действие на естроген, докато естрогенната резистентност се дължи на мутации на гените, кодиращи естрогенни рецептори и води до устойчивост на действията на естроген дори при наличие на циркулиращи естрогени [10, 11].
Този преглед ще се фокусира върху ролята на естрогените върху човешката мъжка кост според всички скелетни физиологични събития, които се случват in vivo в различни етапи от живота при мъжете. Повишаването на Т и Е2 при мъжете в пубертета прогресивно излага костите на половите стероиди, като по този начин им позволява да действат върху нарастващия скелет. Половите стероиди модифицират начина, по който незрелите кости се развиват по отношение на размера, структурата, минералната плътност на костите (КМП) и пропорциите до постигане на окончателно зреене на скелета. След постигането на пикова костна маса, естрогените продължават да влияят на ремоделирането на костите в зряла възраст, като намаляването на циркулиращия Е2 е пряко свързано със загубата на кост от възрастен до стареене.
2. Естрогенни ефекти върху костите от ранен до късен пубертет
Много ниски нива на естрогени циркулират в кръвта дори при мъжки деца по време на ранна детска възраст, но реалното им физиологично значение не е известно [16]. При препубертатни момчета с генитален Tanner етап 1, серумният E2, измерен със златна стандартна течна хроматография тандемна масспектрометрия (LC/MS/MS) започва да се увеличава, варирайки от 0,5–1,0 до около 1,9 pg/ml при здрави контроли и затлъстели момчета, съответно [17, 18]. Считането на развиващия се скелет да не е под въздействието на естрогените преди пубертета при мъжки плодове и деца е добро опростяване, въпреки че това е слабо проучена област на изследване (Таблица 1).
маса 1
Роля на естрогените върху мъжката кост през целия живот.
| Фетален живот | Лошо разследван/неизвестен |
| Детство | Лошо разследван/неизвестен |
| Пубертет | |
| Рано пубертет (откриваемо но ниско Е2) | Удължаване на плоча за растеж Бързо развитие на костната възраст Ускорен линеен растеж на костите Увеличение на скоростта на височината (скок на растежа) Осигуряване на адекватно достигане на целевата височина |
| Късен пубертет (високо E2) | Изтъняване и изчезване на плаката с прогресивен растеж преди затваряне на епифизата Костно съзряване Подобряване на скелетното съзряване Прогресия на костната възраст в края на пубертета Епифизарно сливане и спиране на растежа Постигане на крайна височина Надбавка на пропорциите на скелетното тяло Постигане на адекватна пикова костна маса Размер на костта Дължина на костта Периостална костна апозиция (кръстосана връзка с андрогени) |
| Зрелост | Поддържане на костната маса |
| Стареене | Предотвратяване на загуба на костна маса |
Първоначалното активиране на оста хипоталамус-хипофиза-гонада при мъжки деца, което води до прогресивно, бавно нарастване на половите стероиди, включително естрогени, характеризира перипуберталния период [17–19]. Излагането на кости на ниски концентрации на естрогени води до добре известни естроген-зависими костни промени при мъжете [20, 21].
2.1. Ефекти на естрогените върху надлъжния скелетен растеж
Клиничният фенотип, представен от уникалния мъжки пациент, описан до момента [36] с естрогенна резистентност, е много близък до този на мъжете с дефицит на ароматаза [37, 40]. Характеризира се с висок ръст, анамнеза за непрекъснат линеен растеж в зряла възраст, неразляти епифизи, прогресивен genu valgum, евнухоиден дял на скелета, забавена костна възраст и остеопороза. През 1997 г. Carani et al. [38] демонстрира, че трансдермалното заместване на Е2 е ефективно за постигане на пълно затваряне на епифизата, окончателно зреене на скелета, спиране на растежа във височина, увеличаване на КМП и пикова костна маса [10, 38]. Впоследствие този резултат беше възпроизведен от много други автори при всички мъже с дефицит на ароматаза, описани досега [40–46]. От друга страна, шестмесечното лечение с високи дози Т, дадено преди диагностицирането на дефицит на ароматаза в опит да се спре непрекъснат линеен растеж, няма ефект върху костната възраст при този пациент [10, 38]. Освен това лечението с Е2 не беше ефективно при естроген-резистентните хора, както се очакваше [36]. Всички тези открития предполагат, че затварянето на епифизата е естрогензависимо явление дори при мъжете и че андрогените сами по себе си не са ефективни за осигуряване на нормално развитие на скелета по време на късните пубертетни стадии [10, 11, 21-23] (Таблица 1).
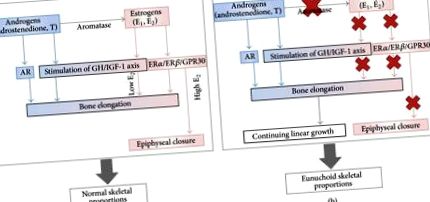
Преки и косвени ефекти от увеличаване на циркулиращите естрогени и тяхното изчерпване върху растежната плоча (а) и ефекти от лишаването от естроген върху удължаването на костите и епифизарния статус (b). AR: андрогенен рецептор; Е1: естрон; Е2: естрадиол; Т: тестостерон; ER-α: естрогенен рецептор алфа; ER-β: естроген рецептор бета; GPR30: мембранозен-G-протеин-свързан естрогенен рецептор.
Предложен диапазон за критичен серумен праг на естрадиол, над който и скелетното узряване, и минерализацията могат да продължат по оптимален начин. Е2: естрадиол; BioE2: Бионаличен естрадиол.
2.2. Ефекти на естрогените върху скелетните пропорции
Таблица 2
Риск от остеопороза и фрактури, както и клинични прояви според естрогенния статус при възрастни мъже.
- Ендокринната система; ХРАНЕНЕТО НА ЧОВЕКА НЕОБХОДИМО
- Бъдещата роля на чревните хормони при лечението на затлъстяването
- Най-великият мъжки гимнастик от всички времена яде само по едно хранене на ден
- Спешна покана за насоки за правата на човека относно диетите и хранителните системи - BMJ
- Какво ям на ден Топ мъжки модел Янис Остоич - списание Eluxe