Малканти Евънс
1 KGK Synergize Inc, Лондон, ON, Канада
John A Rumberger
2 Центърът за дълголетие в Принстън, Принстън, Ню Джърси, САЩ
Исао Азумано
3 Daiichi Fine Chemical Co, Ltd, Toyama, Япония
Джоузеф Дж Наполитано
4 Независим консултант, Allentown, PA, САЩ
Даниел Ситроло
5 Kyowa Hakko САЩ, Ню Йорк, Ню Йорк, САЩ
Тошиказу Камия
5 Kyowa Hakko САЩ, Ню Йорк, Ню Йорк, САЩ
Резюме
Въведение
Експертната група за откриване, оценка и лечение на висок кръвен холестерол при възрастни от Националната образователна програма за холестерол (NCEP) (Възрастна група за лечение III [ATP-III]) предоставя препоръки, основани на доказателства, за управлението на високия холестерол в кръвта и свързаните с тях заболявания. Докладите на ATP-III идентифицират липопротеиновия холестерол с ниска плътност (LDL-C) като основна цел на терапията за понижаване на холестерола. Много проспективни проучвания показват, че високата серумна концентрация на LDL-C е основен рисков фактор за коронарна болест на сърцето (ИБС) .1,2 Въз основа на натрупаните доказателства от епидемиологични проучвания и рандомизирани контролни проучвания, ATP-III предлага алгоритъм за лечение за понижаваща LDL-C терапия. Съгласно алгоритъма ATP-III хората са категоризирани в три рискови категории: 1) установени еквиваленти на CHD и CHD риск; 2) множество (два или повече) рискови фактора; и 3) нулев до един рисков фактор. Еквивалентите на риска от ИБС включват некоронарни форми на клинично атеросклеротично заболяване, диабет и множество (два или повече) рискови фактора за ИБС с 10-годишен риск за ИБС> 20%. Всички лица с ИБС или еквиваленти на ИБС могат да се считат за изложени на висок риск
Диетична намеса и диетично въвеждане
Регистриран диетолог инструктира участниците относно диетата TLC. Незадължителното добавяне на 10 до 25 g/ден вискозни влакна и/или 2 g/ден растителни станоли/стероли и/или соев протеин беше изключено от предписаната диета. Участниците трябваше да следват TLC диетата в продължение на 4 седмици, водеща до проучването (скрининг до изходно ниво), така че ефектът от TLC диетата върху техните липидни нива може да бъде оценен преди началото на добавката. Това елиминира потенциалния принос от разнообразни диети между участниците. Участниците трябваше да останат на диета TLC по време на проучването и трябваше да попълнят 3-дневен запис на храна за всеки 2 делнични дни и 1 уикенд ден преди следващото посещение. За да се насърчи спазването на TLC диетата, хранителните записи бяха попълнени и върнати за преглед и съвет от диетолога при всяко проучвателно посещение. Хранителните записи бяха анализирани за среднодневен енергиен прием на протеини, мазнини, въглехидрати и фибри.
Рандомизация и заслепяване
След завършване на 4-седмичното въвеждане на TLC диета, участниците бяха рандомизирани в съотношение 1: 1, за да получат или пантетин, или плацебо. За рандомизиране е използван блокиращ фактор от две. За да се запази ослепяването, изследваните таблетки и неактивните плацебо таблетки са с идентичен външен вид и са запечатани в идентични блистерни опаковки, идентифицирани само чрез рандомизиран номер.
Изследван продукт
Изследваният продукт е патентован фармацевтичен клас Pantesin HF55. Всяка таблетка съдържа 300 mg активна съставка и е произведена от Eagle Nutritionals (Carlstadt, NJ, САЩ). Блистерните опаковки са произведени от Generic Pharmaceutical Services (Hauppauge, NY, USA) и са етикетирани в съответствие с насоките на Международната конференция по хармонизация на добрите клинични практики, както и приложимите местни разпоредби. Всяка блистерна опаковка съдържа две таблетки с активна съставка и една плацебо таблетка (600 mg/дневна доза, от 1 до 8 седмици), три таблетки с активна съставка (900 mg/дневна доза от 9 до 16 седмици) или три плацебо таблетки. Участниците в двете групи са приемали по една таблетка три пъти на ден за целия период на изследване, от изходното ниво до седмица 16. Съответствието е оценено чрез преглед на върнатите блистерни опаковки.
Клинични оценки
Участниците се завръщат в клиниката на седмици 0, 2, 4, 8, 12 и 16 и при всяко посещение се събира кръв за гладно (12 часа) за анализ (Gamma-Dynacare Medical Laboratories, Лондон, ОН, Канада) на липида панел (TC, HDL-C, LDL-C, TG, VLDL-C, Apo-B и липопротеин) и маркери за безопасност; CBC, електролити и тестове за чернодробна и бъбречна функция. TG се анализира чрез ензимен колориметричен анализ, извършен на Roche P800 Clinical Chemistry Analyzer, VLDL-C се изчислява от стойностите на TG (чрез разделяне на TG на 2,18) и липопротеинът се измерва чрез нефелометричен анализ, извършен на Siemens BN II Nephelometer. hs-CRP, хомоцистеин и CoQ10 бяха измерени на седмици 0, 4, 8, 12 и 16. hsCRP бяха анализирани с помощта на Dade Behring BNII нефелометър и хомоцистеин, анализирани с помощта на FPIA технология (Gamma-Dynacare Medical Laboratories). Анализът на общия CoQ10 беше извършен чрез HPLC с UV детекция от KGK Synergize Laboratory (Лондон, ON, Канада). HPLC методът е адаптиран от Mosca et al.36
Нежеланите събития (AE) се записват от участниците в дневници и се наблюдават от изследователя от момента, в който са получили поне една доза от изследвания продукт до края на периода на лечение. Неблагоприятните признаци и симптоми, включително необичайни лабораторни находки, заболяване или влошаване на каквито и да било съществуващи състояния, които са били временно свързани с употребата на изследвания продукт, се считат за НЕ. Изследователят на изследването е оценил AE и е определил причинно-следствената връзка с изследвания продукт като най-вероятна, вероятна, възможна, малко вероятна или несвързана.
статистически анализи
Бяха извършени междугрупови анализи на демографски и изходни характеристики, като се използва ковариантна корекция за сравнение на крайните точки на проучването, а когато липсваха изходни стойности, бяха използвани стойностите, получени от скрининговото посещение.
Междугруповите анализи на първични и вторични крайни точки и параметрите за безопасност бяха коригирани за изходно ниво, а групите сравнени с помощта на несдвоен t-тест. Тестът на Андерсън-Дарлинг е използван за определяне дали данните не са нормално разпределени. Когато данните не са били нормално разпределени, са направени сравнения между групи, като се използва непараметричен тест. Сравненията в рамките на групата бяха направени с помощта на t-тест на Student или теста на Wilcoxon за подписване, според случая. Техниката „последна стойност, пренесена напред“ също се прилага, когато данните липсват след 2-та седмица, като се използва последното налично наблюдение на пострандомизация за статистически анализи.
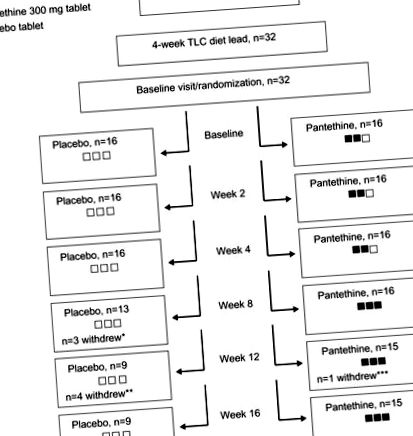
Извършен е междугрупов анализ на дела на участниците, изпитващи нежелани събития, използвайки точния тест на Fisher’s. Всички статистически анализи бяха извършени с помощта на R и стойности на вероятността в таблица 1). Общо 32 участници завършиха 4-седмичното TLC диетично въвеждане и бяха рандомизирани в съотношение 1: 1, за да получат или пантетин, или плацебо. И накрая, 24 участници завършиха 16-седмичното добавяне (Фигура 1).
Бележки: * Двама участници се оттеглиха от проучването поради неблагоприятни събития, а един се изнесе извън града. Съобщените нежелани събития са: симптоми на настинка (n = 1); и наличие на кръв в изпражненията (n = 1). ** Четирима субекти се оттеглиха от проучването поради нежелани събития. Съобщените нежелани събития са: LDL-C се повишава до ATP III високорискова категория (n = 3); и един субект не желае да продължи да учи след заболяване от стрептокок в гърлото (n = 1). *** Един субект се оттегли от проучването поради повишаване на LDL-C до ATP III високорискова категория. Черните кутии представляват таблетките пантетин, който е бил изследваният продукт, а белите кутии представляват плацебо. За да поддържат ослепяването, всички субекти са получили 3 таблетки. На 8 седмица дозата беше увеличена в групата на пантетина, така че те получиха три таблетки пантетин (три черни кутии).
Съкращения: ATP III, Група за лечение на възрастни III (Експертна група за откриване, оценка и лечение на висок кръвен холестерол при възрастни); LDL-C, липопротеинов холестерол с ниска плътност; TLC, Терапевтична промяна в начина на живот.
маса 1
Изходни физически характеристики на участниците в пантетиновите и плацебо групите
| Възраст (години) | 54,4 ± 7,3 | 47,2 ± 12,1 | 0,051 |
| Височина (см) | 164,8 ± 6,9 | 169,3 ± 7,5 | 0,083 |
| Секс (%) | |||
| Женски пол | 87,50 | 56.25 | 0,113 |
| Мъжки пол | 12.50 | 43,75 | |
| Раса (%) | |||
| Бял | 87,50 | 93,75 | > 0,999 |
| Други | 12.50 | 6.25 | > 0,999 |
Бележки:
Промени в серума (A) TC, (Б.) LDL-C, (° С) не-HDL-C и (д) Апо-В нива при скрининг, изходно ниво и седмици 2, 4, 8, 12 и 16 от периода на изследване.
Таблица 2
Биохимия и клинични характеристики на участниците в пантетина и плацебо групите
Бележки: Вероятностни стойности P * P-стойности, които се различават значително между групите. Междугруповата статистическа значимост в стойностите на червените кръвни клетки, MPV и AST остава в рамките на нормалния лабораторен референтен диапазон.
Съкращения: ALT, аланин трансаминаза; AST, аспартаза аминотрансфераза; CoQ10, Коензим Q10; eGFR, изчислена скорост на гломерулна филтрация; hs-CRP, високочувствителен С-реактивен протеин; MCH, среден корпускуларен хемоглобин; MCV, среден корпускуларен обем; MPV, среден обем на тромбоцитите; RDW, ширина на разпределение на червените клетки; SD, стандартно отклонение.
Нежелани събития
В настоящото проучване е регистриран общо един симптом, потенциално приписан на изследваното лекарство, при един участник в групата на плацебо. Общо два симптома (диария и метеоризъм), потенциално приписани на изследваното лекарство, са докладвани от участниците на пантетин. Диарията е с умерена интензивност, изпитва се в продължение на 3 дни по време на периода на дозиране от 600 mg/ден и не се повтаря, когато дозата ескалира. Метеоризмът, докладван от един участник, е преживян през двата периода на дозиране, с лека интензивност и отзвучава преди края на проучването. При участник на плацебо е открит единичен лек епизод на неутропения.
Дискусия
Добре установено е, че повишените нива на плазмените липиди играят основна роля в развитието и прогресирането на атеросклеротичната болест.37–39 Намаляването на нивата на LDL-C при индивида намалява риска от ССЗ и честотата на сърдечно-съдовите резултати. 4,40,41 В момента, лекарства за понижаване на холестерола, като статини, по-нисък LDL-C и разпространението на сърдечно-съдови събития.6–8 Интензивното използване на статини обаче е свързано с появата на диабет, увреждане на мускулите и черния дроб и когнитивно увреждане.10–12, 42
ATP III препоръчва първата линия на лечение за пациент с абнормен LDL-C да бъде диетата TLC. След това хората се категоризират по профил на рисковия фактор и/или FRS и се считат за допустими за терапия със статини, ако нивата на LDL-C са над определена цел.34 Предишно проучване върху пантетин изследва ефикасността на лечението с пантетин при нисък риск ( FRS 10-годишен риск 10%, но 160 mg/dL; или умерен FRS [> 10, но 130 mg/dL). Резултатите от нашето проучване потвърдиха хипотезата, че пантетинът значително ще подобри метаболизма на холестерола, чрез понижаване на TC и LDL-C, без да причинява сериозни AEs при лица с нисък и умерен CVD, които отговарят на условията за терапия със статини. Пантетинът не е оказал ефект върху нивата на TG, вероятно защото включените участници са имали нормални нива на TG на изходно ниво. Основното заключение на това разследване е, че диетата TLC сама по себе си не е довела до значителна промяна в липидния профил, но пантетинът, съчетан с диета TLC, значително намалява TC и LDL-C при участниците по време на 16-седмичното проучване.
Проучването на потомството Framingham предполага секс ефект върху LDL-C.43. Пантетинът има по-високо съотношение между жени и мъже, отколкото при плацебо групата. Анализ на подгрупа на пола показва, че няма значителна разлика в LDL-C при скрининг или след 4-седмично въвеждане на TLC диета, като участниците в двете групи имат сходни LDL-C стойности на изходно ниво. След започването на добавката обаче, пантетиновата група показа по-голямо вътрешногрупово намаление на LDL-C, достигайки 11% до седмица 4. Участничките в жени показаха 13% намаление до седмица 8, което след това се поддържаше на 12 и 16 седмица Тези вътрешногрупови процентни промени са били значителни между групите на 8 и 16 седмица, което предполага, че подобренията в LDL-C при жените са свързани с добавянето на пантетин. Нивата на Апо-В при жените на пантетин също показват значително намаление спрямо изходното ниво на седмици 2, 4, 8, 12 и 16; тези на плацебо показват увеличение на Апо-В по време на проучването. Участниците от мъжки пол на пантетин не показват разлики в липидните параметри, вероятно поради по-малкия брой проби.
Няма значителни промени в нивата на хомоцистеин от изходното ниво до седмица 16 и нивата остават в нормалните граници (≤15 μmol/L) и за двете групи по време на това проучване. Ефектът на хомоцистеин върху риска от ССЗ остава несигурен. Нивото на хомоцистеин е прогностичен маркер за смъртност и ССЗ при пациенти с предварително съществуващи рискови фактори за ССЗ.54 От друга страна, мета-проучванията показват, че намаляването на нивата на хомоцистеин чрез добавяне на витамини не намалява риска от големи сърдечно-съдови събития или обща смъртност в пациенти със съдови заболявания.55,56 Тъй като механизмите на действие на пантетина при понижаване на нивата на холестерола не са напълно изяснени, беше важно да се вземе предвид влиянието на добавките на пантетин, ако има такива, върху хомоцистеина.
Нежеланите събития, приписвани на изследвания продукт, са 6,3% за плацебо и 12,5% за пантетин. В групата на плацебо се наблюдава неразрешен лек AE на кръвта и костния мозък (неутропения). В групата на пантетина се съобщава за метеоризъм и диария, но тези две събития отзвучават по време на проучването. Отчетените в това проучване нежелани реакции са в съответствие с докладваните преди това нежелани реакции на пантетина.32,34 Предишни клинични проучвания показват, че пантетинът се понася добре, с ниска честота на странични ефекти при дози от 600 до 1200 mg/ден.
Някои от рисковете за здравето при продължителна употреба на статини при високи дози включват миалгии и повишен риск от развитие на захарен диабет. Те са свързани със съпътстващо намаляване на in vivo производството на CoQ10. Въпреки че не са значими между групите, нивата на CoQ10 значително се повишават от изходното ниво до седмица 4 и остават повишени на 16-та седмица както при пантетина, така и при плацебо групата. Възможно е диетата TLC да е осигурила храни, съдържащи по-високи нива на CoQ10 в сравнение с храненията, които участниците са консумирали преди началото на проучването. Освен това плазмените нива на CoQ10 не са непременно отражение на нивата на CoQ10 в тъканите.57 За разлика от статините, които са инхибитори на HMG-CoA редуктазата, които блокират биосинтеза на CoQ10, пантетинът не блокира CoQ10.58 Тъй като пантетинът не влияе върху производството на CoQ10, комбинираното употребата на пантетин и ниска доза статини може да действа синергично за понижаване на LDL-C, като същевременно минимизира неблагоприятните ефекти, свързани с високата доза статини. Необходими са допълнителни изследвания, за да се провери тази хипотеза.
Заключение
Това проучване потвърждава, че пантетинът намалява маркерите за риск от ССЗ при участници с нисък до умерен риск от ССЗ, които са кандидати за статини съгласно насоките на NCEP. В сравнение с плацебо, лекуваните с пантетин участници демонстрират значителен спад в нивата на LDL-C, HDL-C и TC след 16 седмици лечение. Освен това, за разлика от статините, които изчерпват CoQ10 до вредни нива, както пантетиновите, така и плацебо групите значително повишават своите нива на CoQ10 над изходното ниво. Това проучване демонстрира, че диетата TLC сама по себе си не повлиява значително липидните профили, но заедно с добавките с пантетин значително намалява нивата на липидите. Следователно добавката с пантетин може да се разглежда като допълнителна допълнителна терапия за пациенти с нисък до умерен риск от ССЗ.
Благодарности
Авторите искат да благодарят на доброволците от това проучване за тяхната готовност и старание при спазване на протокола. Лари Щит, помощник-директор на Биостатистическия отдел, Университет на Западен Онтарио, е благодарен за приноса му относно статистическия дизайн и анализ. Признаваме Соня Бар за провеждането на проучването, Джош Бейсли за осигуряване на качеството и техническата му експертиза, както и Хуей Джун Джу за преглед и редакция на този ръкопис. Това проучване беше подкрепено от Daiichi Fine Chemical Co, Ltd.
Бележки под линия
Разкриване
JJN е получил финансиране за научни изследвания или е действал като консултант на няколко компании за хранителни добавки и хранителни добавки. IA е служител на Daiichi Fine Chemical Co, Ltd. TK и DC са служители на Kyowa Hakko USA, Inc. Авторите съобщават, че няма други конфликти на интереси в тази работа.
- Моля, не „подлагайте се на диета“ - Alchemy Total Wellness
- Трябва ли да приемате статин, дори ако холестеролът ви е нормален Harvard Health
- Ppc инжекция за отслабване True Beauty Чай за отслабване Витаминни добавки за вяра за отслабване
- Премиум CBD масло 1000mg; Витамин B12 с гуарана за отслабване (комбо) Groupon
- Естествени витаминни добавки за косопад Viviscal