Кореспонденция на: Vishalkumar G Shelat, FRCS, FICS, Hesperis Diploma in Organ Transplant (ECOT), Hepatobiliary Consultant Surgeon, Department of General Surgery, Tan Tock Seng Hospital, Level 4, Annex 1, 11, Jalan Tan Tock Seng, Singapore 308433, Сингапур. moc.liamffider@talehsgv
Телефон: + 65-63577807 Факс: + 65-63577809
Резюме
Основен съвет: Класическата триада на внезапна поява на коремна болка, тахикардия и скованост на корема е отличителен белег на перфорираната пептична язва. Ранната диагностика, бързата реанимация и спешната хирургическа интервенция са от съществено значение за подобряване на резултатите. Експлораторната лапаротомия и възстановяването на пластира на омента остава златният стандарт и трябва да се има предвид лапароскопска хирургия, когато е налице експертиза. Гастректомия се препоръчва при пациенти с голяма или злокачествена язва за подобряване на резултатите; обаче резултатите от пациентите, лекувани със стомашни резекции, остават по-ниски.
ВЪВЕДЕНИЕ
Язвената болест (PUD) е резултат от дисбаланс между стомашно-киселинно-пепсиновите и лигавичните защитни бариери. Той засяга 4 милиона души по света годишно [1]. Честотата на PUD се оценява на около 1,5% до 3% [2]. Систематичен преглед на седем проучвания от развити страни изчислява, че годишните нива на заболеваемост от PUD са 0,10% -0,19% за диагностицирани от лекарите PUD и 0,03% -0,17%, когато се основават на данни за хоспитализация [3]. Въпреки че 10% -20% от пациентите с PUD ще получат усложнения, само 2% -14% от язвите ще перфорират, причинявайки остро заболяване [4,5]. Перфорацията е сериозно усложнение на PUD и пациентите с перфорирана пептична язва (PPU) често са с остър корем, който носи висок риск за заболеваемост и смъртност [6]. Доживотното разпространение на перфорацията при пациенти с PUD е около 5% [7]. PPU носи смъртност от 1,3% до 20% [8-10]. Съобщава се за тридесетдневна смъртност, достигаща 20%, и 90-дневна смъртност до 30% [11,12]. В този преглед обобщихме настоящите доказателства за PPU и се надяваме, че нашият преглед ще помогне на хирурзите, актуализирани с доказана практика.
АЕТИОЛОГИЯ
Въпреки че предишни проучвания показват, че сезонните вариации са повлияли на честотата на PPU, други проучвания не са успели да докажат такъв модел [13-16]. В развиващите се страни пациентите обикновено са млади мъже пушачи, докато са в развитите страни; пациентите са склонни да бъдат в напреднала възраст с множество съпътстващи заболявания и свързана употреба на нестероидни противовъзпалителни лекарства (НСПВС) или стероиди [17,18]. НСПВС, Helicobacter pylori (H. pylori), физиологичен стрес, тютюнопушене, кортикостероиди и предишна анамнеза за PUD са рискови фактори за PPU [1,19-27]. При наличие на рискови фактори рецидивът на язва е често срещан въпреки първоначалното успешно лечение. Систематичен преглед на 93 проучвания показва, че средният дългосрочен рецидив на перфорацията е 12,2% (95% ДИ: 2,5-21,9) [5].
НСПВС
НСПВС са широко използвани заради неговите аналгетични, противовъзпалителни и антипиретични ефекти. Известно е, че употребата на НСПВС увеличава риска от PPU [28,29]. Около една четвърт от хроничните потребители на НСПВС ще развият PUD и 2% -4% ще кървят или перфорират [30-33]. Взаимодействието на лекарства със стероиди и селективни инхибитори на обратното поемане на серотонин също увеличава рисковете от PUD. Селективните инхибитори на циклооксигеназа-2 са по-малко свързани с PUD. Проучване в западна Дания показа, че стандартизираните нива на хоспитализация за PPU намаляват от 17 на 100000 население през 1996 г. до 12 на 100000 население през 2004 г. (HR 0.71; 95% CI: 0.57-0.88) след въвеждането на селективна циклооксигеназа-2 инхибитори в клиничната практика [34].
H. pylori
H. pylori остава една от най-честите инфекции в света. Разпространението на H. pylori е намаляло в развитите страни поради подобрена хигиена и намалено предаване в ранна детска възраст. Средното разпространение на H. pylori при пациенти с PPU варира между проучванията поради различни диагностични методи и географски вариации. Последните проучвания, използващи хистопатологични методи за откриване на H. pylori, показват, че разпространението на H. pylori при пациенти с перфорирани язви на дванадесетопръстника варира от 50% -80% [22,35]. Рандомизирано контролирано проучване през 2008 г., включващо 65 пациенти, които са претърпели просто затваряне на перфорирана язва на дванадесетопръстника, показва едногодишна честота на рецидиви от 6,1% при пациенти, лекувани с H. pylori, за разлика от 29,6% в контролната група [36]. Повтарящият се PUD се среща главно при пациенти с инфекция с H. pylori, което предполага, че H. pylori играе важна роля в развитието на PUD и неговите усложнения [22,37]. Рискът от рецидивираща инфекция с H. pylori е значително намален при терапия с инхибитори на протонната помпа, но инхибиторите на протонната помпа имат само умерена ефикасност за намаляване на язви при потребители на НСПВС.
Пушене
Смята се, че тютюнът инхибира секрецията на бикарбонат на панкреаса, което води до повишена киселинност в дванадесетопръстника [38,39]. Той също така инхибира зарастването на язва на дванадесетопръстника. Мета-анализ показва, че 23% от PUD може да бъде свързано с тютюнопушене [40]. В някои проучвания обаче не е имало разлика в употребата на тютюн между пациенти с не-H. pylori, не-НСПВС язви на дванадесетопръстника и тези с язви, свързани с H. pylori, което показва ограничена роля на тютюнопушенето [41]. Това е в съгласие с предишни проучвания, които показват, че тютюнопушенето не увеличава риска от рецидив на язвата след изкореняване на H. pylori [42,43].
Други
КЛИНИЧНИ ХАРАКТЕРИСТИКИ
През 1843 г. Едуард Крисп заявява, че „симптомите са толкова типични, едва ли вярвам, че е възможно някой да не успее да постави диагноза“ [48].
Симптомите на PUD включват коремна болка, дискомфорт в горната част на корема, подуване и чувство за пълнота. Когато PUD се влоши и в крайна сметка перфорира, стомашният сок и газовете навлизат в перитонеалната кухина, което води до химически перитонит. Внезапна поява на коремна болка или остро влошаване на продължаващата коремна болка е типично за PPU. Обикновено болката никога не отшумява напълно въпреки обичайните предмедицински средства и принуждава пациента да потърси медицинска помощ. Химичният перитонит, дължащ се на изтичане на гастродуоденално съдържимо и силна болка, води до тахикардия. Класическата триада на внезапна поява на коремна болка, тахикардия и скованост на корема е отличителен белег на PPU.
Клиничната проява може да бъде разделена на три фази [49]. В началната фаза в рамките на 2 часа от началото са характерни епигастрални болки, тахикардия и хладни крайници. Във втората фаза (в рамките на 2 до 12 часа) болката става генерализирана и се влошава при движение. Типични признаци като коремна скованост и чувствителност на десния долен квадрант (в резултат на проследяване на течности по десния параколичен улей) могат да се видят. В третата фаза (повече от 12 часа) може да са очевидни раздуване на корема, пирексия и хипотония с остър циркулаторен колапс.
Проучване, включващо 84 пациенти с PPU, съобщава, че най-честите проявяващи се симптоми са внезапна поява на силна епигастрална болка (97,6%), раздуване на корема (76,2%) и повръщане (36,9%) [50]. Коремна нежност и класически признаци на перитонит могат да бъдат предизвикани при 88,1% и 66,7% от пациентите с PPU в това проучване. Други симптоми включват също гадене (35,7%), тежка диспепсия (33,3%), запек (29,8%) и треска (21,4%) [50]. Според нашия опит при управление на 332 пациенти с PPU, най-честият проявяващ се симптом е острата поява на коремна болка (61,7%) [51]. Неотдавнашно проучване в Тайван показа, че пациентите с PPU са по-склонни да се явяват в спешното отделение през уикендите и това трябва да бъде потвърдено [52].
Тахикардия и коремна чувствителност с ригидност са често срещани клинични признаци. Силна болка, системна възпалителна реакция от химичен перитонит и дефицит на течности или поради лош прием или повръщане или пирексия води до компенсаторна тахикардия. При пациенти, които забавят търсенето на медицинска помощ, възниква хипотония поради общия дефицит на вода в тялото. Ако е без прекъсване; това прогресира до умствена изостаналост и остра бъбречна травма. Това води до състояние, при което пациентът става физиологично негоден за оперативна намеса, което е абсолютно необходимо. Следователно е важно да се установи бърза потвърждаваща диагноза.
ДИАГНОСТИКА
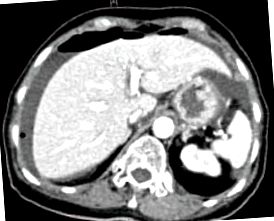
Компютърната томография показва свободен въздух под диафрагмата с перихепатална свободна течност.
Изправете рентгеново изображение на гръден кош на същия пациент с двусмислен свободен въздух под дясната хемидиафрагма.
Лабораторните тестове се извършват в PPU не за установяване на диагноза, а за изключване на диференциална диагноза, както и за разбиране на обидата за различни системи от органи. Те са неспецифични [56]. Серумната амилаза трябва да се прави при представяне на индекса в спешното отделение или след нормален рентгенов анализ на гръдния кош. Повишената серумна амилаза може да бъде свързана с PPU и обикновено се повишава по-малко от четири пъти над нормалното си ниво [57]. Тестове като брой на белите кръвни клетки и С-реактивен протеин могат да бъдат направени като част от разследването в PPU. Левкоцитозата и повишеният С-реактивен протеин могат да бъдат повишени в резултат на възпаление или инфекция [57]. Повишеното ниво на креатинин, урея и метаболитна ацидоза отразява синдрома на системния възпалителен отговор (SIRS) и предбъбречното увреждане [58]. Серумните нива на гастрин са показани при пациенти с анамнеза за повтарящи се язви или непокорни PUD и могат да помогнат за установяване на диагнозата на синдрома на Zollinger Ellison. При пациенти със съмнения за паращитовидни нарушения са показани серумни нива на калций.
УПРАВЛЕНИЕ
PPU е хирургична спешна ситуация, свързана с висока смъртност, ако не се лекува. Като цяло, всички пациенти с PPU се нуждаят от бърза реанимация, интравенозни антибиотици, аналгезия, инхибитори на протонната помпа, назогастрална сонда, пикочен катетър и хирургичен контрол на източника.
Медикаментозно лечение в PPU
Омепразолът и тройната терапия за ерадикация на H. pylori са полезни допълнения при лечението на PPU. Доказателствата показват, че лечението с омепразол и тройната терапия намалява значително честотата на рецидиви. Излекуването на язва, показано при 8-седмично проследяване с ендоскопия, е значително по-високо в групата за ерадикация с тройна терапия [36]. Осемдесет и пет точки три процента от язви са излекувани в групата с тройна терапия, за разлика от 48,4% в групата, приемаща само омепразол. Няколко други проучвания от различни страни също доказаха ликвидирането на тройната терапия след просто затваряне на PPU, намалило честотата на повтарящи се язви [37,59,60]. Нашата практика е да предписваме интравенозен инхибитор на протонната помпа за 72-96 часа и да започнем орална тройна терапия веднага след това. Извършваме дихателен тест за урея, за да установим ерадикация на H. pylori след завършване на медицинското лечение.
Неоперативно управление
Оперативно управление
ВАГОТОМИЯ
Блуждаещият нерв играе важна роля в регулирането на отделянето на гастрин и секрецията на стомашна киселина чрез стимулиране на париеталните клетки чрез холинергични рецептори [70]. Вагусната стимулация също освобождава хистамин и гастрин от ентерохромафиноподобни клетки и G-клетки, което от своя страна ще стимулира париеталните клетки да произвеждат киселинна секреция. Ваготомията е процедура, която трансектира вагусните стволове (тръбна ваготомия) или дисталните нервни влакна (силно селективна ваготомия). Трънкалната ваготомия има за цел да намали секрецията на стомашна киселина, като по този начин намалява рисковете от повтарящи се PUD. Селективната ваготомия, която щади чернодробните и целиакиалните отдели на вагусните стволове, са свързани с по-високи дългосрочни рецидиви [71]. Следователно селективната ваготомия вече не се извършва. Проучванията показват, че честотата на рецидиви на язва е била до 42% при пациенти с перфорирана язва на дванадесетопръстника, които са били подложени на лесен ремонт на пластир на яйцеклетката [72,73]. Малко проспективни рандомизирани проучвания също съобщават за значително по-малко рецидиви на язва при пациенти, които са били подложени на ваготомия в допълнение към възстановяване на пластира на омента [37,74]. Независимо от това, ваготомията рядко се извършва за PPU поради наличието на лекарства като антагонисти на хистаминовите рецептори, инхибитори на протонната помпа и ерадикация на H. pylori.
ГАСТРЕКТОМИЯ
ЛАПАРОСКОПИЧЕН РЕМОНТ
„Разреждането с разтвор е решение на замърсяването“. Към края на операцията някои хирурзи обичат да напояват перитонеалната кухина с 6-10 литра и дори до 30 литра топъл физиологичен разтвор, въпреки че в литературата не са намерени доказателства, че напояването може да намали риска от сепсис [98,99 ]. От друга страна, пневмоперитонуем, предизвикан по време на лапароскопска хирургия, може да увеличи риска от бактериално разпространение [100]. Изглежда също така предпочитанието на хирурга дали да остави дренаж в края на операцията или не [101]. Няма доказателства в подкрепа на това, че оставянето на дренаж може да намали честотата на интраабдоминални колекции [101, 102]. Напротив, това може да доведе до инфекция на мястото на оттичане и повишен риск от чревна непроходимост [102]. Въпросник, извършен от Schein, показва, че осемдесет процента от хирурзите не са оставили дренаж след операция поради причините, обсъдени по-горе [63]. В днешно време рядко се използват тест за гуми (следете за мехурчета след потапяне на пластира под вода) и тест за багрило (за инжектиране на багрило през назогастрална сонда) за търсене на течове след затваряне на PPU (Фигура (Фигура 3 3)).
Показва лапароскопски ремонт на пластир на омента. A: Предна дуоденална перфорация; Б: Лапароскопско зашиване; C: Пластир за оман; D: Поставяне на коремния дренаж.
САМОЕКСПАНДИВНИ МЕТАЛНИ СТЕНТИ
Първичното стентиране и дренаж могат да се използват като нова възможност за лечение на PPU [103]. Осем пациенти с PPU са лекувани със саморазширяващи се метални стентове [103]. Двама пациенти са лекувани със стентиране поради следоперативно изтичане след първоначално хирургично затваряне, а шест пациенти са лекувани с първично стентиране. Седем от 8 пациенти са се възстановили без усложнения и са били изписани 9-36 дни след стентиране. Друго проучване, включващо 10 пациенти с PPU, които са лекувани със стентиране, също показва добри клинични резултати [104]. Това проучване показва лечението със стент като минимално инвазивна алтернатива с по-малко усложнения в сравнение с хирургичното лечение. Тези проучвания показват, че пациентите с PPU могат да бъдат лекувани с първично стентиране и дренаж, където е налице обучение и опит. Необходими са повече данни, за да се докаже ефективността на този метод.
МАРГИНАЛНО ИЗПЪЛНЕНИЕ НА ЯДРАТА
ПОСТОПЕРАТИВНИ УСЛОВИЯ
PPU лечението е свързано със значителна следоперативна заболеваемост и смъртност, независимо дали се извършва лапароскопски или открит ремонт [113]. Следоперативната смъртност за PPU се оценява на 6% -10% [114]. Възраст на възраст над 60 години, забавено лечение над 24 часа, шок при представяне със систолично кръвно налягане по-малко от 100 mmHg и съпътстващи заболявания са основните рискови фактори, влияещи върху резултата [2,115]. Следоперативната смъртност при възрастни хора е 3 до 5 пъти по-висока [116]. Това може да се дължи на наличието на медицински съпътстващи заболявания, забавено представяне, нетипично представяне или забавяне> 24 часа при диагностицирането [116].
В нашето локално проучване, включващо 332 пациенти, претърпели операция за PPU, следоперативните усложнения включват интраабдоминално събиране (8,1%), изтичане (2,1%) и повторна операция (1,2%) [51]. Интраабдоминалният абсцес остава сериозно следоперативно усложнение след операция на PPU. Следователно трябва да се възприеме добра хирургична техника, за да се предотврати това усложнение. Нашите ниски нива на изтичане (2,1%) могат да бъдат обяснени с ранно представяне, бърза диагностика, ранна реанимация и подходяща операция. Нашите данни за 30-дневна смъртност са 7,2%, което е сравнима с скорошно проучване от Южна Корея [120]. По-ниската смъртност в нашето местно проучване може да се дължи на по-млада възраст (54,7), по-малка съпътстваща заболеваемост (16,2%) и по-малко пациенти с предоперативен шок (7,2%).
Неотдавнашно проучване разглежда връзката на смъртността с извънработно приемане при пациенти с PPU [121]. В това проучване са включени общо 726 пациенти, които са били лекувани хирургично за PPU. Това проучване не показва статистическа значимост между 90-дневна смъртност и извънработно приемане при пациенти, лекувани хирургично за PPU.
За да се разпределят по подходящ начин ресурси и да се осигурят оптимални грижи, е важно пациентите да се разслоят на нисък и висок риск от смъртност. Налични са много точкови системи за прогнозиране на смъртността.
БЕЗОПАСНИ СИСТЕМИ ЗА ПРЕДВИДЕНИЕ НА РЕЗУЛТАТИТЕ В PPU
Около 11 различни системи за оценяване, използвани за прогнозиране на резултата в PPU, могат да бъдат идентифицирани чрез литературата: оценка на Boey, оценка на Americal Society of Anesthesiologists (ASA), оценка на Sepsis, индекс на коморбидност на Чарлсън, индекс на Mannheim Peritonitis (MPI), Остра физиология и оценка на хроничното здраве II (APACHE II), Опростената оценка на острата физиология II (SAPS II), Физиологична оценка и оценка на оперативната тежест за изброяване на смъртността и физическата суб-оценка на заболеваемостта (POSSUM-Phys резултат, моделите на вероятността за смъртност II (MPM II), оценка на перфорация на пептична язва (PULP), оценка на Hacettepe и оценка на Jabalpur [121]. Сред тези 11 точки, точките на Boey и ASA резултат са най-често валидираните системи [8,80,122-124] . Други системи за оценяване не се използват широко поради липса на валидиране или тяхната сложност при клинична употреба. Ние потвърдихме ASA резултат, резултат на Boey, MPI и PULP резултат и установихме, че и четирите системи имат умерена точност на пред смъртност от обледяване с площ под кривата на оператора на приемника от 72% -77,2% [51]. В скорошно проучване, включващо 148 пациенти от две свързани с университета болници в Сингапур, Lee et al [125] съобщава, че при избрани пациенти с представяне в рамките на 48 часа и размер на язва 21.
Неотдавнашно проучване разглежда 62 пациенти, претърпели спешна операция за PPU [126]. Това проучване изследва корелацията между количеството перитонеална течност и клиничните параметри при пациенти с PPU. Използвайки методите, описани от Ishiguro et al [126], беше възможно да се предскаже количеството на натрупаната интраперитонеална течност чрез CT сканиране. Това проучване показа, че методът на Ishiguro et al [126] е полезен за прогнозиране на количеството интраперитонеална течност при пациенти с PPU. Смята се, че това ще бъде полезно за прогнозиране на тежестта на следоперативните усложнения и също така за вземане на решение за лечение (Фигура (Фигура 4 4)).
- Пептична язва (стомашна язва) диета и рецепти
- Язва на стомаха Пептична язва Симптоми, причини; Лечение @DocOnline
- Пептична язва при деца
- Язвена болест на стомашно-чревния тракт - Ръководства на Merck Professional Edition
- Мини преглед на пептична язва по отношение на случая - MedCrave онлайн