Никола Д. Познай
Група за изхранване и диетични изследвания, Imperial College, Лондон, болница Хамърсмит, Лондон, W12 0NN UK
Отдел по диабет, ендокринология и метаболизъм, сграда на Британската общност на 6-ти етаж, Медицински факултет, Имперски колеж Хамърсмит Кампус, Du Cane Road, Лондон, W12 ONN UK
Ан Дорнхорст
Отдел по диабет, ендокринология и метаболизъм, Imperial College NHS Trust, Лондон, Великобритания
Ник Оливър
Отдел по диабет, ендокринология и метаболизъм, Imperial College NHS Trust, Лондон, Великобритания
Джими Д. Бел
Департамент по науки за живота, Факултет по наука и технологии, Университет в Уестминстър, Лондон, W1W 6UW Великобритания
Е. Луиз Томас
Департамент по науки за живота, Факултет по наука и технологии, Университет в Уестминстър, Лондон, W1W 6UW Великобритания
Гари С. Фрост
Група за изхранване и диетични изследвания, Imperial College, Лондон, болница Хамърсмит, Лондон, W12 0NN UK
Свързани данни
Резюме
Заден план
Инфилтрацията на мазнини в черния дроб, мускулите и панкреаса е свързана с инсулинова резистентност и риск от диабет. Загубата на тегло намалява извънматочното отлагане на мазнини и риска от диабет, но е трудно да се поддържа поради компенсаторно повишаване на апетита. Доказано е, че ферментиращите въглехидрати намаляват апетита и приема на храна и насърчават загубата на тегло при лица с наднормено тегло. При проучвания върху животни ферментируемият въглехидрат намалява извънматочната мазнина, независимо от загубата на тегло. Целта ни беше да изследваме ефекта на ферментируемия въглехидратен инулин върху поддържането на теглото, апетита и извънматочните мазнини при пациенти с преддиабет.
Методи
Четиридесет и четирима субекти с преддиабет бяха рандомизирани на 18-седмична добавка на инулин или целулоза. През седмици 1–9 (фаза на отслабване) всички пациенти са имали четири посещения с диетолог, за да ги насочат към 5% загуба на тегло. През седмици 10–18 (фаза на поддържане на теглото) субектите продължават да приемат назначената им добавка и са помолени да поддържат загубеното тегло, но не им се предлага допълнителна подкрепа. Всички субекти присъстваха на учебни сесии на изходно ниво, 9 и 18 седмици за измерване на теглото; оценка на съдържанието на мастна тъкан и извънматочна мазнина чрез ядрено-магнитен резонанс и магнитно-резонансна спектроскопия; нива на глюкоза, инсулин и GLP-1 след тест за толерантност към хранене; и апетит чрез тест ad libitum хранене и визуални аналогови скали.
Резултати
Електронен допълнителен материал
Онлайн версията на тази статия (doi: 10.1186/s12986-015-0033-2) съдържа допълнителен материал, който е достъпен за оторизирани потребители.
Заден план
Интервенциите в начина на живот могат значително да намалят риска от развитие на диабет тип 2 (T2DM) [1], като загубата на тегло е основният медиатор на намаляването на риска [2]. Въпреки това, извън условията на трудоемко клинично изпитване, дългосрочната загуба на тегло е прословуто трудно постижима [3, 4].
Едно от обясненията за рядкостта на успешното поддържане на загуба на тегло е, че енергийният дефицит и загубата на телесни мазнини са свързани както с повишаване на апетита, така и с приема на храна [5, 6]. Следователно интервенции като агонисти на подобен на глюкагон пептид-1 (GLP-1), насочени към намаляване или подобряване на такива промени в апетита, спомагат за насърчаване на дългосрочното поддържане на загуба на тегло [7]. Несмилаемите въглехидрати (диетични фибри) отдавна са свързани с намален прием на храна [8], а ферментиращите въглехидрати (FCHO) могат да бъдат особено ефективни [8]. Този клас въглехидрати преминават неусвоени и неабсорбирани от горната част на стомашно-чревния тракт към дебелото черво, където бактериалната ферментация произвежда късоверижни мастни киселини (SCFA), които могат да стимулират GLP-1 и да регулират други хормони на апетита [9]. Освен това, като естествено диетично съединение, FCHO биха могли да представляват широко приложима намеса в областта на общественото здраве. Чрез насърчаване на естественото намаляване на апетита може да се наложи по-рядка клинична подкрепа. В едногодишно проучване при юноши с наднормено тегло се наблюдава значително по-нисък ръст на индекса на телесна маса (ИТМ) в инулиновата група, без да се получи информация от здравни специалисти [10].
Ключов медиатор на благоприятния ефект от загубата на тегло върху инсулиновата чувствителност е загубата на извънматочна мастна тъкан [11], която е силно свързана с инсулиновата резистентност и T2DM [11–13]. Интригуващо е, че е доказано, че FCHO намалява извънматочната мазнина в проучвания върху животни, независимо от загубата на тегло [14]. Това поражда възможността този естествен диетичен въглехидрат не само да засили усилията за отслабване, но може също да насърчи загубата на тази метаболитно-вредна мазнина при хората, дори след като отчете загуба на тегло. При здрави и инсулиноустойчиви субекти е доказано, че FCHO подобрява инсулиновата чувствителност [15, 16], но не е ясно дали намаляването на ектопичните мазнини играе роля. Нито едно предишно проучване не е изследвало ефекта от диетична интервенция върху извънматочните мазнини при пациенти с преддиабет.
Тук отчитаме ефекта от 30 g/ден (след 4-седмичен период на повишаване на дозата) добавка на инулин, взета заедно с 9-седмична програма за отслабване и 9-седмичен период на поддържане на теглото. Предполагаме, че инулинът ще доведе до по-голямо поддържане на загуба на тегло при 18-седмично проследяване при пациенти с преддиабет и ще насърчи намаляване на ектопичната мастна и инсулинова резистентност, независимо от загубата на тегло, оценена чрез използване на златно-стандартния магнитен резонанс ( MRI) и техники на магнитно-резонансна спектроскопия (MRS).
Доброволци
Субекти с известен преддиабет или високорискови фактори за преддиабет са идентифицирани от местните регистри на общопрактикуващите лекари. Преди проучването е получено информирано съгласие. Протоколите са одобрени от Комитета по етична изследователска дейност на North West 1 (регистрационен номер: 10/H0717/32) (Номер на клинично изпитване:> NCT01841073) и са в съответствие с Декларацията от Хелзинки. За изясняване на гликемичния статус беше извършен орален тест за глюкозен толеранс (OGTT). Критериите за включване бяха възраст ≥ 18 години, ИТМ от 25–35 kg/m 2, преддиабет (нарушена глюкоза на гладно (IFG) и/или нарушен глюкозен толеранс (IGT)), използвайки критериите на Американската диабетна асоциация [17] и стабилно телесно тегло за 3 месеца преди проучването. Критериите за изключване бяха нормален глюкозен толеранс, T2DM, стомашно-чревни разстройства, бременност или кърмене, предписани лекарства, които влияят на апетита или глюкозната хомеостаза и консумация на пребиотични продукти или употреба на антибиотици в рамките на 3 месеца от датата на проучването. Доброволците бяха рандомизирани по ИТМ и пол, използвайки таблица със случайни числа, със съотношение на разпределение 1: 1.
Експериментален дизайн
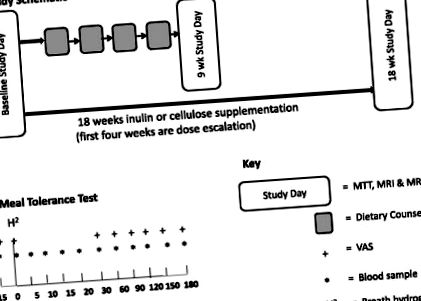
Проучването е двойно-сляпо рандомизирано паралелно контролно проучване, изследващо ефекта на 30 g/ден инулин (Synergy1, Orafti, Tienen, Белгия) спрямо контролната целулоза (Vitacel® Powdered Cellulose L 600–20, J. Rettenmaier & Söhne GmbH + Co.) заедно с 9-седмична програма за отслабване и 9-седмична програма за поддържане на теглото (фиг. 1). Влакнестата целулоза е избрана за сравнение, тъй като този неразклонен полимер на глюкозните молекули, свързани с (β4-1) връзки, претърпява минимална ферментация на дебелото черво. Дозата от 30 g е избрана въз основа на предишни проучвания от нашата група [18, 19]. И двете добавки са дадени като сашета от 10 g, приемани три пъти на ден с храна или напитка. За намаляване на потенциалните стомашно-чревни странични ефекти добавките се увеличават с 10 g/ден на всеки 2 седмици, за да достигнат дозата от 30 g/ден. Следователно, до пета седмица от деветседмичната фаза на загуба на тегло, всички пациенти са били на максималната доза от 30 g/ден. Сашетата с инулин и целулоза получиха буква А или В и по друг начин бяха идентични.
Схема, показваща схемата на изследването, включително времената на вземане на кръвни проби, VAS и измерване на водородния дишане по време на MTT. Н 2: измерване на водородния дъх; MTT: тест за толерантност към хранене; MRS: ядрено-магнитен резонанс; MRS: магнитно-резонансна спектроскопия; VAS: визуални аналогови везни
По време на 9-седмичната програма за отслабване всеки субект се подложи на стандартизирана диетична интервенция, състояща се от четири диетични сесии с интервал 2-3 седмици с регистриран диетолог (фиг. 1). Диетологът беше заслепен за разпределението на добавките. Изискванията за енергия и определените размери на порциите за нишестета, протеини, мляко и млечни продукти, мазнини и захари и плодове и зеленчуци бяха определени с помощта на готов отчитател, разработен в болница Hammersmith. След 9-седмичното посещение субектите не получиха допълнителни приноси или подкрепа от изследователския екип. Те просто бяха помолени да се опитат да поддържат загубеното тегло.
Всички субекти присъстваха на изследователски ден на изходно ниво, 9 седмици (представляващи края на фазата на отслабване) и 18 седмици (края на фазата на поддържане на теглото) за тест за толерантност към хранене (MTT) (Ensure Plus ™ (220 ml), обща енергия: 1380 kJ, 44,4 g въглехидрати, 10,8 g мазнини, 13,8 g протеин). Взети са кръвни проби при -15, 0, 5, 10, 15, 20, 30, 45, 60, 90, 120, 150, 180 минути за измерване на глюкоза, инсулин и GLP-1 (фиг. 1).
Апетитът се оценява по време на MTT, като се използват валидирани [20] визуални аналогови скали (VAS) на чести интервали, последвани от тест ad libitum хранене [20]. Използваните въпроси за апетита бяха „Колко си гладен в момента?“ (общ глад), „Колко мислите, че бихте могли да ядете в момента?“ (бъдеща консумация на храна), „Колко приятно би било да се яде в момента?“ (желание за ядене) и „Колко сит се чувстваш в момента?“ (усещане за пълнота в стомаха) (Допълнителен файл 1).
Съставът на тялото се оценява чрез 9-електродно устройство за биоелектричен импеданс (BIA) (Tanita BC-418 MA Segmental Body Composition Analyzer) (Tanita Corporation, Tokyo, Japan). Устройството BIA предоставя оценки на% телесни мазнини (± 0,1%), мастна маса (± 0,1 kg) и маса на свободни мазнини (± 0,1 kg). В допълнение, подгрупа от субекти, които отговарят на условията (без метал на място или докладвана клаустрофобия) (n = 20), са подложени на ЯМР и MRS за оценка на общия и регионалния обем на мазнините в изходно ниво, девета седмица и седмица 18. Бърз T1-претеглен магнитен резонанс изображенията са получени с помощта на 1,5 T скенер на Phillips Achiva (Phillips, Best, Холандия) [21] с интрахепатоцелуларен липид (IHCL) и интрамиоцелуларен липид в мускулите на солеуса и тибилалиса (IMCL-S и IMCL-T, съответно), оценени от MRS, както е описано по-рано [22].
Съответствието се оценява, като се изисква от субектите да върнат неизползвани сашета и дишането на водород се измерва като прокси на ферментацията на дебелото черво с помощта на монитор за дишане на водород (Gastrolyzer, Bedfont Scientific Ltd., Кент, Великобритания).
Лабораторен анализ
Глюкозата се събира във флуоридни оксалатни епруветки и се измерва с помощта на анализатор Architect ci8200 (Abbott Diagnostics, Maidenhead, Великобритания), с граница за откриване на анализа от 0,3 mmol/L и коефициент на вариация (CV) в рамките на теста от 1%. Проби от плазмен инсулин бяха събрани в серумни сепараторни епруветки, съдържащи активатор за съсирване на гел Vacutte® и измерени с търговски комплект за радиоимуноанализ (Millipore; Watford, UK). Чувствителността и интра-тестовата CV за инсулин са съответно 7,1 pmol и 3,0%. Проби от GLP-1 бяха събрани в литиеви хепаринови епруветки с добавен апротинин (Trasylol, Bayer, Newbury, UK) (200 μL/7,5 ml кръв). Кръвните проби се въртяха при 4000 g при 4 ° C в продължение на 10 минути, разделяха се в плазма и се съхраняваха при -20 ° C, докато се анализираха с помощта на вътрешен радиоимуноанализ [23]. Чувствителността и CV в рамките на анализа на GLP-1 са съответно 7,5 pmol/l и 3,3%.
Изчисления и статистически анализ
Въз основа на проучване на Parnell et al. [24] с очаквана загуба на тегло от 2,0 kg и стандартно отклонение от 2,0 kg въз основа на 0,8 мощност за откриване на значителна разлика (P 1. Нямаше разлики между инулиновите и целулозните групи в нито една от базовите характеристики. от 44 субекта бяха наети и рандомизирани, от които петима се оттеглиха от проучването преди деветата седмица, включително един, който приема инулин, и един, който приема целулоза, който отпадна поради странични ефекти. Допълнителен субект се оттегли след посещението на деветата седмица. файл 1). Освен това, поради отпадане (n = 1) затруднения при планиране (n = 2), оттегляне на съгласие за ЯМР (n = 1) и вече не отговарят на условията за ЯМР (n = 1) петима субекти, които са подложени на изходно ниво и MRI сканиране на седмица девет не са направили сканиране на 18 седмици. Следователно 19 субекта са завършили проследяващ MRI на 9 седмици (инулинова група: три жени и седем мъже; целулозна група: четири жени и пет мъже) и 14 субекта завършиха проследяващ ЯМР на 18 седмица s инсулинова група: три жени, шест мъже; група целулоза: три жени и два мъже).
маса 1
Характеристики на предмета за всяка част от изследването
| Пол (М: Ж) | 13: 8 | 11: 9 | 0,66 |
| Възраст (години) | 58,2 ± 12,0 | 59,7 ± 8,9 | 0,53 |
| Тегло (кг) b | 88,2 ± 14,0 | 83,4 ± 19,7 | 0,28 |
| ИТМ (kg/m 2) | 30,8 ± 4,1 | 30,0 ± 2,3 | 0,41 |
| FPG (mmol/L) | 5,7 ± 0,5 | 5,9 ± 0,6 | 0,20 |
| 2hPG (mmol/L) | 7,3 ± 2,3 | 7,3 ± 2,0 | 0,99 |
| HbA1c (%) и (mmol/mol a) | 5,9 ± 0,1 (41,3 ± 1,4) | 5,7 ± 0,1 (38,8 ± 0,9) | 0,78 |
| Инсулин на гладно (pmol/L) | 95.4 (116.8) b | 114.1 (132.9) b | 0,17 |
Стойностите са средните и SD. Полът се изразява като съотношение на мъжете към жените. Няма значителни разлики между групите за нито една от изходните променливи. FPG плазмена глюкоза на гладно; 2hPG 2-часова плазмена глюкоза
SI единици за HbA1c, показани в скоби
b Инсулинът на гладно обикновено не се разпределя, така че посочените стойности са за медиана (интерквартилен диапазон)
- Статии Безплатна пробна екстремна диета за отслабване Естествено - управление на HazMat
- Страхотно Осигурете най-новия магазин за план за упражнения за отслабване - Управление на HazMat
- Аюрведични съвети за управление на теглото - Veda Wellness - Успех без стрес Veda Wellness -
- BodyStart Keto Chia Семена отслабват здравословно - HazMat Management
- Страхотно отслабване за 1 ден Гаранция за връщане на парите - HazMat Management