Чегевара Афане 1, Дебора Гершберг 2, Еоин Слаттери 3, Дейвид С. Серес 3, Джон А. Шабот 4, Майкъл Д. Клугер 4
Ключови думи: Усложнения; тръби за ентерално хранене; хранене; хирургия на рак на панкреаса
Изпратено на 04 юни 2014 г. Прието за публикуване на 6 август 2014 г.
Въведение
Ракът на панкреаса е 4-тата водеща причина за смъртност от рак в Съединените щати, въпреки че е 12-ият най-инцидентен рак. Пълната хирургична резекция е единствената терапия с възможност за дългосрочно оцеляване. Първата голяма серия от 41 пациенти, подложени на панкреатикодуоденектомия (PD) или процедура на Whipple, е съобщена през 1941 г. (1). Смъртността е 29%. Повечето от подобрената преживяемост, постигната през последните 3 десетилетия, са свързани с подобрено периоперативно управление и по-ранно разпознаване и лечение на следоперативна заболеваемост. В момента смъртността е
Методи
Извършено е систематично търсене с помощта на PubMed за проучвания, публикувани до 26 май 2014 г. Използваните термини за търсене са „пилорна запазване на PD или резекция на панкреаса или панкреатектомия или операция на Whipple или панкреас или дуоденална резекция на главата на панкреаса“ и „хранене или хранене или назогастрален или назоеюнален или гастроеюностомия или йеюностомия “, ограничено до заглавие, резюме или ключови думи. Търсихме статии с доказателства от ниво I, когато е възможно; по-голямата част от литературата обаче се състои от ниво II или по-големи доказателства. Включени са систематични прегледи, метаанализи, рандомизирани и наблюдателни кохортни проучвания. Документи със становище, доклади от случаи и проучвания върху животни бяха изключени за този преглед. Периоперативният, както се използва в този ръкопис, обхваща периода от диагноза, през операция, до пълно възстановяване с орален прием. Лечението на остър и хроничен панкреатит не беше включено.
Предоперативна оценка на храненето
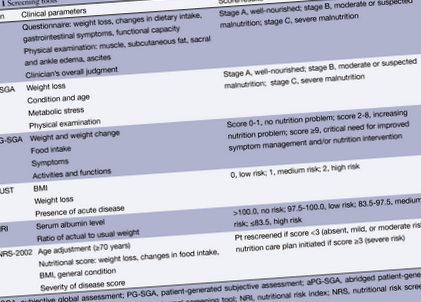
Като цяло злокачествените заболявания предразполагат пациентите към предоперативно недохранване. Правилният скрининг за недохранване може да помогне за идентифициране на пациенти с повишен риск от периоперативна заболеваемост. За съжаление терминологията около недохранването остава доста объркваща. Проявите на катаболизъм, свързан със заболяването, често не се различават от тези, свързани с гладуването, а пациентите с недохранване може да не се хранят добре калорично. Тоест пациентите може да нямат диета, пълна с хранителни вещества и протеини, въпреки че са способни ефективно да метаболизират наличните източници на хранене. Различни инструменти за скрининг са разработени и валидирани за идентифициране на пациенти с риск от недохранване, включително субективна глобална оценка (SGA), универсален инструмент за скрининг за недохранване (MUST) и NRI (20) (Таблица 1). Тези инструменти, заедно с определени антропометрични измервания, като индекс на телесна маса (ИТМ) и лабораторни маркери на храненето, като албумин и преалбумин, могат да помогнат за насочване на предоперативните стратегии за подобряване на храненето на пациентите. Въпреки че значителната загуба на тегло се счита за надежден показател, недохранването е далеч по-сложно. Дори пациенти с висок ИТМ могат да бъдат изложени на значителен риск от недохранване (13,21,22).
Само едно проучване сравнява тези мерки за оценка на разпространението и ефекта от недохранването върху следоперативната заболеваемост при пациенти, подложени на резекция на рак на панкреаса (13). Сама по себе си загубата на тегло с ≥5% от предварителното приемане през предходните три до шест месеца е свързана с повишен риск от SSI и увеличена продължителност на престоя. MUST и NRI показаха отлично съгласие по отношение на общата заболеваемост, честотата на SSI и продължителността на болничния престой, докато MUST и SGA имаха отлично съгласие по отношение на честотата на SSI (13). Въпреки това това беше ретроспективен преглед.
Предоперативни серумни маркери
Албуминът е протеин с остра фаза, който намалява по време на периоди на възпаление, травма и нараняване. Отдавна е известно, че албуминът не отразява адекватността на приема на пациента (30). Въпреки това, хипоалбуминемията е силно свързана с лоши следоперативни резултати, като смъртност и инфекция след стомашно-чревна хирургия (31). Сред пациентите, подложени на резекция за аденокарцином на панкреаса (n = 268), предоперативната хипоалбуминемия (10 mg/L) има значително по-кратка преживяемост (8,3 срещу 18,2 месеца; P
Периоперативно хранене
Хранене през устата
Различни доклади са изследвали ефикасността на ранните стратегии за перорално хранене след операция на панкреаса. Съгласно препоръките на ERAS Society, рутинната употреба на предоперативно ентерално хранене не е показана (37). Съществуват обаче доказателства на ниско ниво, които предполагат, че предохранителното допълнително хранене може да бъде показано при недохранван пациент. Европейското общество за клинично хранене и метаболизъм (ESPEN) подкрепя по-силно предоперативната хранителна подкрепа за 10-14 дни при пациенти с тежък хранителен риск, дори ако операцията трябва да бъде отложена. ESPEN дефинира тежък риск от наличието на поне един от следните критерии: загуба на тегло> 10-15% в рамките на 6 месеца, BMI 2, SGA степен С, серумен албумин 60% от техните хранителни нужди в рамките на 10 дни и/или с очевидни под хранене по време на операцията (45).
Несъответствието между насоките ERAS и ESPEN признава, че повечето пациенти не са в състояние да постигнат своите хранителни цели per os в следоперативния период. В писмото на Bozzetti [2013] несъответствията между планираните графици на хранене и резултатите от приема са посочени в проучвания на пациенти, подложени на панкреатектомия (46-53). В отговор Ласен и сътрудници посочват, че част от литературата, подкрепяща подхода ESPEN, също страда качествено и че ентералните тръби не са без риск (54).
Неотдавнашно проучване на ERAS на 115 пациенти, подложени на PD от Braga и сътрудници, имаше за цел да започне течности на ден след операцията и твърди вещества на ден след операцията в групата на ERAS, в сравнение с ден след операцията и ден 4 след операцията, съответно, в историческата контролна група. Тези цели бяха постигнати при 55% от пациентите за перорални течни цели и 53% за твърди хранителни цели. Ниското съответствие с целите на ERAS е свързано с честотата и тежестта на усложненията. Например, от 60 пациенти с лошо съответствие с ранното перорално хранене, близо 72% са имали следоперативни усложнения (55).
Парентерално хранене
Авторите се опитват да покажат ролята на рутинната PN при пациенти след PD. Въпреки ранния ентусиазъм за PN, пероралното хранене постоянно се оказва по-безопасно и по-ефективно от PN по отношение на появата на следоперативни усложнения (включително инфекция, PF и DGE) и продължителността на престоя (57,68). В проспективно рандомизирано контролирано проучване на Klek и колеги [2011] 167 пациенти с недохранване от рак са разпределени на случаен принцип да получават или ентерално, или парентерално и стандартно или имуномодулиращо хранене в продължение на 14 дни, преди да се подложат на операция за оценка на ефекта върху следоперативните усложнения (69). Недохранването се определя от критериите ESPEN, представени по-рано (45). Авторите установяват, че имуномодулиращите ентерални храни при недохранени пациенти значително намаляват общата заболеваемост (P = 0,01), инфекциозните усложнения (P = 0,04), смъртността (P = 0,03) и продължителността на престоя (P = 0,006) в сравнение със стандартното ентерално хранене. Имуномодулацията не прави значителна разлика в рамото с PN по отношение на заболеваемостта, смъртността или продължителността на престоя (P> 0,05). В случаи на продължителна стомашно-чревна дисфункция, при която не са възможни стратегии за ентерално хранене, PN трябва да се дава, докато се изпълнят калоричните изисквания per os.
PN също се предлага като потенциален инструмент в консервативното управление на PF; други методи за хранене обаче се оказаха по-ефективни. Klek et al. [2011] извърши проспективно рандомизирано контролирано проучване на 78 пациенти с PFs, рандомизирани по EN или PN (70). На 30 дни степента на затваряне на PF беше 60% в групата с EN в сравнение с 37% в групата с PN (P = 0,04). Средното време за затваряне в групата с EN е 27 дни, докато средното време не е достигнато в края на проучването за групата с PN (P = 0,047). Единствените два фактора, свързани със затварянето на PF, са EN [OR = 6.136, 95% доверителен интервал (CI): 1.204-41.623; P = 0,04] и първоначална продукция на фистула ≤200 cc/ден (OR = 12.701; 95% CI: 9.102-47.241; P
Периоперативни ентерални тръби
Ролята на ентералните тръби е силно обсъждана и доста специфична за хирурга. Липсват конкретните доказателства в полза на оптималната стратегия за декомпресия и хранене след операция на панкреаса. Таблица 3 сравнява четири различни начина на хранене. Описваме ролята на периоперативната декомпресия на назогастралната сонда, както и на периоперативното хранене на ентерални тръби след хирургия на панкреаса.
Дренажни (ямкови) назогастрални сонда
Поставянето на дрениращ NGT за предотвратяване на стомашно разтягане, повръщане, анастомотични течове и намаляване на времето за възстановяване на функцията на червата след операция на рак на панкреаса се счита за стандартна практика (78). Последните данни показват, че декомпресията на NGT може да е ненужна след операция на панкреаса. В ретроспективно кохортно проучване Fisher et al. описва поредица от 100 последователни пациенти, подложени на операция на панкреаса, като 50 пациенти са отстранени NGT, след като пациентите са демонстрирали адекватна функция на червата (група NGT), а 50 пациенти са отстранени веднага NGT следоперативно (без група NGT) (79). Смъртността и заболеваемостта са сходни между групите с NGT и No NGT (съответно 0% срещу 2%; P = 1.0 и 44% срещу 44%; P = 1.0), както беше времето за връщане на червата функция (медиана съответно 5 срещу 5 дни; P = 0,81). Честотата на изтичане на жлъчни анастомоти е била 0% и в двете групи. Процентът на PF е 6% в групата с NGT и 10% в групата без NGT (P = 0,72). Освен това продължителността на престоя не се различава значително между двете групи (медиана 7 в двете групи; P = 0,30). Няма усложнения от вмъкването на NGT следоперативно (2 в групата с NGT срещу 4 в групата без NGT; P = 0,68).
В друго наблюдателно кохортно проучване на 250 пациенти [125 пациенти във всяка група (рутинна NGT и селективна NGT)], подложени на PD, авторите заключават, че рутинната употреба на NGT може да е ненужна (80). Селективното поставяне на NGT се отнася до онези епруветки, поставени при клинична индикация, например за продължителна ендотрахеална интубация. Общата заболеваемост не се различава значително между рутинните NGT и селективните NGT групи (съответно 81,6% срещу 80,8%; P = NS). При многовариантния анализ рутинната употреба на NGT е независим рисков фактор за DGE [коефициент на риск (HR) = 8,56; P = 0,03]. Освен това общата продължителност на престоя е била значително по-кратка в селективната NGT група в сравнение с рутинната NGT група (медиана съответно 6 срещу 7 дни; P
Фистула на панкреаса
PF е едно от най-сериозните усложнения след операция на рак на панкреаса. Дефиницията варира в литературата в широки граници, въпреки че две от най-често срещаните дефиниции включват> 10 cc/ден богата на амилаза течност след постоперативен ден 3 или продължаване на оттичането на богата на амилаза течност след 20 оперативен ден, както е определено от международната група за изследване на панкреатичната фистула (ISGPF) (84). Schmidt et al. оценява различни рискови фактори за развитие на PF след PD при серия от 510 пациенти (85). Общо 46 PF се развиват следоперативно. Интересното е, че използването на механична подготовка на червата се оказа защитно срещу развитието на PF (6% срещу 19%, P
Бъдещи начинания
Заключения
Благодарности
Разкриване: Авторите не декларират конфликт на интереси.
- Хранене на пациенти с фрактура на челюстта и след ортогнатична хирургия, Преглед на литературата
- Приложения за смартфони за популяризиране на здравословна диета и хранене Преглед на литературата - PubMed
- Хранене и рак на панкреаса; Подхранваща чиния
- Подкрепа за храненето при остър панкреатит систематичен преглед на литературата - База данни на
- Подкрепа за храненето и диетични интервенции за пациенти с рак на белия дроб текущи прозрения