1 Консултант на терапевтично звено, Отделение по вътрешни болести, Държавен медицински университет в Запорожие, 26, пр. Маяковски, Запорожие, UA-69035, Украйна
2 Катедра по клинична фармакология, Държавен медицински университет, Запорожие, Украйна
3 Частен медицински център „Vita-center”, Запорожие, Украйна
Резюме
Ключови думи
Хронична сърдечна недостатъчност, биомаркери, микровезикули, получени от ендотелни клетки
Съкращения
ACEI: инхибитори на ангиотензин-конвертиращия ензим; ARBs: Ангиотензин рецепторни блокери; AUC: площ под кривата; ИТМ: Индекс на телесна маса; BNP: Мозъчен натриуретичен пептид; CV: Сърдечно-съдови; GDF-15: Диференциален фактор за растеж-15; GFR: Скорост на гломерулна филтрация; HDL-C: Липопротеинов холестерол с висока плътност; СН: Сърдечна недостатъчност; HFmrEF: Хроничен Hf с фракция на изтласкване от среден клас; HFpEF: Хроничен СН с запазена фракция на изтласкване; HFrEF: Хроничен HF с намалена фракция на изтласкване; hs-CRP: високочувствителен C-реактивен протеин; LDL-C: Липопротеинов холестерол с ниска плътност; LVEF: Фракция на изтласкване на лявата камера; MP: Ендотелни клетъчни микровезикули; MVs: Микро везикули
Въведение
Методи
Проучвайте популация
Кохортата на проучването се състоеше от 388 субекта с хронична СН, които бяха ангажирани в бъдеще между април 2010 г. и октомври 2017 г. Всички тези пациенти бяха лекувани в Регионална болница Запорожие, Градска болница № 6 (Запорожие), Градска болница № 10, Запорожки регионален център по сърдечно-съдови заболявания с първична диагноза хронична СН, която е определена съгласно съвременните критерии, предвидени от действителната клинична препоръка [1]. Фенотиповете на хроничната СН са определени съгласно тази препоръка като СН с намалена фракция на изтласкване [HFrEF] (n = 85; LVEF ≤ 40%), СН с фракция на изтласкване от средния диапазон [HFmrEF] (n = 125; LVEF = 41-49 %) и HF със запазена фракция на изтласкване [HFpEF] (n = 178; LVEF ≥ 50%). Критериите за невключване в проучването бяха оценени степен на гломерулна филтрация (GFR) 2; имплантиран пейсмейкър/дефибрилатор/кардиовертер; остри инфекции; активно възпаление; клапно сърдечно заболяване; бременност; исхемичен инсулт; вътречерепен кръвоизлив; хирургия; травма, автоимунно заболяване и злокачествено заболяване преди влизането в проучването.
T2DM е диагностициран с ревизирани критерии, предоставени от Американската диабетна асоциация при преглед на изходните документи [20]. Пациентите с T2DM са лекувани с метформин в индивидуално коригирани дневни дози под непрекъснат контрол на гликемията на гладно, дневния профил на концентрацията на глюкоза и нивото на гликиран хемоглобин (HbAc1). Рядко ситаглиптин се добавя към схемата за лечение. В проучването не са избрани пациенти с T2DM, даващи инсулин.
Демографски данни и антропометрични измервания
Възрастта, полът, височината, теглото, телесната маса, индексът на телесна маса, обиколката на талията и съотношението на талията в миналото в анамнезата и медикаментите са събрани на изходно ниво. Антропометричните данни бяха измерени от професионални здравни специалисти, като участниците стояха без обувки и тежки връхни дрехи със стенен монтиран стадиометър (OMRON, Япония). Индексът на телесната маса (ИТМ) се изчислява от персонала като тегло (Kg), разделено на квадратен ръст (m 2). Обиколката на талията и ханша се измерва в изправено положение по протокол [22,23].
Статус на пушене
Настоящото пушене се определя като консумация на една цигара дневно в продължение на три месеца [24].
Сърдечен ултразвук и доплер
Трансторакална ехокардиография е извършена на ултразвукова система ACUSON (SIEMENS, Германия) в режим на режим В и режим на тъканно доплер изображение (TDI). Фракцията на изтласкване на лявата камера (LVEF) беше измерена по модифициран метод на Симпсън [25].
Измерване на скоростта на гломерулна филтрация
Вземане на кръвни проби
Кръвни проби бяха взети сутрин след гладуване през нощта (в 7-8 сутринта) в баркодирани силиконови епруветки (Thermo Fisher Scientific, Waltham, MA, USA), в които бяха добавени 2 ml 5% разтвор на Trilon B. След това пробите бяха центрофугирани при постоянно охлаждане при 6000 об/мин за 3 минути и след това плазмата беше събрана, за да бъде незабавно охладена. Всяка аликвотна част се съхранява при температура 70ºС.
Нивото на N-терминален про-мозъчен натриуретичен пептид (NT-pro-BNP) беше измерено чрез имуноелектрохемолуминесцентен анализ, използвайки набори от R and D Systems (САЩ) на анализатор Elecsys 1010 (Roche, Mannheim, Германия). Галектин-3 беше измерен с помощта на комплект ELISA (BG Medicine, Германия) и получен с анализатор Elecsys 1010 (Roche, Mannheim, Германия). Разтворимият ST2 беше измерен чрез търговски ELISA комплект „Presage ST2 Assay“ (Critical Diagnostics, Сан Диего, САЩ), в съответствие с препоръките на производителите. Растеж-диференциалният фактор-15 (GDF-15) се определя чрез ELISA комплект (LifeSpan BioSciences, САЩ) на анализатор Elecsys 1010 (Roche, Mannheim, Германия). Високочувствителните нива на С-реактивен протеин (C-RP) бяха измерени чрез нефелометричната техника с търговски комплект (Eagle Biosciences, Nashua, NH, USA) и получени с „AU640 Analyzer“ (Olympus Diagnostic Systems Group, Япония). Извършен е високоефективен метод на течна хроматография за определяне на хемоглобин А1с (HbA1c) в 5% антикоагулирани кръвни проби Trilon B.
Концентрациите на общия холестерол (TC), холестерола на липопротеините с висока плътност (HDL-C), липопротеините с ниска плътност (LDL-C) и триглицеридите (TG) са измерени чрез директен ензимен метод с търговски комплекти (DIALAB, Neudorf, Австрия ) с използване на автоматичен анализатор Roche P800 (F Hoffmann-La Roche AG, Базел, Швейцария).
Приготвяне на кръв, етикетиране и измерване на микровезикули, получени от ендотелни клетки
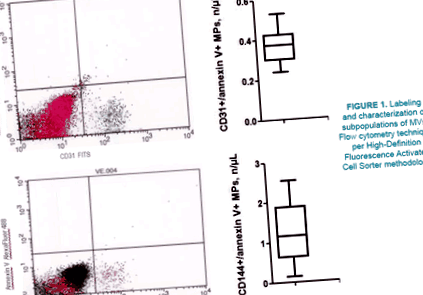
Циркулиращите микровезикули (MVs) са изолирани от 5 ml венозна цитрирана кръв, взета от рака без фистула, съгласно протокол, описан по-рано [27]. Техника на поточна цитометрия съгласно методологията за сортиране на клетъчна сортировка с висока разделителна способност е използвана за етикетиране и характеризиране на субпопулации на MVs веднага след вземане на кръвна проба без замразяване [28].
Фигура 1: Етикетиране и характеризиране на субпопулации на MVs: Техника на поточна цитометрия съгласно методологията за сортиране на клетки с висока дефиниция на флуоресценция.
Статистически анализ
Данните бяха анализирани с помощта на SPSS 20.0 (SPSS, IBM Corporation, NY, USA) и Prism v.6 (GraphPad Software Inc., La Jolla, CA, USA). Данните са изразени като средна стойност (М) и грешка на средната стойност (± m) или 95% доверителен интервал (CI); медианата (Ме) и интерквартилния диапазон (IQR). Категоричните променливи са докладвани като многобройни (n) и проценти (%). Тестът на Шапиро-Уилк и тестът на Колмогоров-Смирнов са използвани за определяне на нормалността на непрекъснатите променливи. За да се сравнят основните параметри на групите пациенти (в зависимост от вида на разпределение на анализираните параметри), беше използван едностранен t-тест на Student или U-тест на Mann-Whitney. Двустранната версия на теста на Wilcoxon беше използвана за сдвоено сравнение на стойностите на параметрите в групата. Категоричните променливи между групите бяха сравнени с тест Chi 2 (χ 2) и точен тест Fisher F.
- Брой на циркулиращите апоптотични ендотелни клетъчни микрочастици като предиктор за
- Оперативни и ранни резултати от байпас на коронарна артерия при пациенти от женски пол в различно тяло
- Затлъстяването е независимо свързано с коронарна ендотелна дисфункция при пациенти с нормално състояние
- Прогностична стойност на нормалната стресова ехокардиография при пациенти със затлъстяване
- Метаболитен синдром при юноши с наднормено тегло и затлъстяване Сравнение на две различни диагностични