Поглъщане на мастен черен дроб и n-3 мастни киселини: нови механизми и перспективи от предклинични животински модели
Аманда Маррейро Барбоса
Мултицентрова магистърска програма по физиологични науки, Център за биологични науки, Федерален университет в Санта Катарина (UFSC), Флорианополис, Бразилия
Тайз Родригес Шагас
2 Завършила програма по хранене, Център по здравни науки, Федерален университет в Санта Катарина (UFSC), Флорианополис, Бразилия
Everson Araújo Nunes
Мултицентрова магистърска програма по физиологични науки, Център за биологични науки, Федерален университет в Санта Катарина (UFSC), Флорианополис, Бразилия
2 Завършила програма по хранене, Център по здравни науки, Федерален университет в Санта Катарина (UFSC), Флорианополис, Бразилия
Резюме
Безалкохолната мастна чернодробна болест (NAFLD) се характеризира с натрупване на липиди, причинено от дисбаланс между синтеза, поглъщането, окисляването и износа на мастни киселини. Животински модели, използващи диети с високи нива на липиди или въглехидрати и прекомерно лечение с глюкокортикоиди са имитирали промените в чернодробната стеатоза. Хранителните интервенции с използване на n-3 полиненаситени мастни киселини (EPA-ейкозапентаенова киселина и DHA-докозахексаенова киселина) показват, че могат да намалят чернодробната стеатоза, особено чрез намаляване на активността на липогенните ензими и увеличаване на потока на окисление. В тази област са изследвани нови механизми като активност на окислителните ензими и промени в тонуса на ендоканабиноидната система, за да се изяснят тези ефекти. В допълнение, изследването на новите специфични за EPA и DHA молекулни цели е обсъдено от нови изследвания.
Ключови думи
чернодробна стеатоза, черен дроб, метаболизъм, n-3 мастни киселини, предклинични модели
Въведение
Безалкохолната мастна чернодробна болест (NAFLD) е една от най-честите форми на хронично чернодробно заболяване в развитите страни, засягаща 20 до 30% от общото население [1-3]. Това заболяване се определя от патологичното натрупване на прекомерна мазнина в черния дроб без консумация на алкохол, като натрупването на чернодробни триглицериди (TG) в резултат на небалансирано усвояване, синтез, износ и окисляване на мастни киселини [4,5]. Такова състояние се характеризира с чернодробна стеатоза, увреждане на чернодробните клетки и лобуларен хепатит [4].
Затлъстяването е важен рисков фактор за развитието на NAFLD, главно натрупване на висцерална мастна тъкан, поради което инсулиновата резистентност може също да бъде отговорна за развитието на NAFLD дори при лица със затлъстяване и слаби лица [6-8]. Патогенезата на NAFLD обаче не е напълно ясна. Счита се, че са включени множество механизми, като отклонен липиден метаболизъм, нерегулирано производство на цитокини, оксидативен стрес и възпаление в хепатоцитите [9-12].
Други фактори, които играят роля в съдържанието на липиди в черния дроб, могат да включват диета, de novo синтез на чернодробни липиди и генетични фактори [13-16]. Следвайки този ред на мисли, за да се възпроизведе етиологията, развитието, прогресията и резултата от чернодробно заболяване, често се използват експериментални модели, базирани на животни, като висококалоричен хранителен прием (прехранване), висок прием на мазнини (особено наситени мастни киселини), висок прием на прости захари и диета за кафене [17-21]. Освен това, някои фармакологични интервенции също могат да причинят NAFLD. Синтетичните глюкокортикоиди (GC) са вещества, имитиращи ендогенни стероидни хормони, секретирани от кората на надбъбречната жлеза при активиране на оста хипоталамус-хипофиза-надбъбречна жлеза (HPA). Те могат да допринесат за развитието на метаболитен синдром. Синтетичните GC обикновено се прилагат като противовъзпалителни лекарства. Въпреки това, употребата за продължително време или във високи дози може да предизвика нежелани реакции, като наддаване на тегло, инсулинова резистентност, хипертриглицеридемия, хиперфагия и централно затлъстяване [22-26].
Въпреки че патогенните механизми, участващи в натрупването на чернодробни липиди, причинени от диета или използване на синтетичен GC, не са напълно разбрани, някои проучвания са проведени, за да се намерят адювантни стратегии за смекчаване на промените, доказани при това метаболитно разстройство, като поглъщането на полиненаситени мастни киселини (PUFA) [27-30].
Мастните киселини могат да повлияят на много клетъчни свойства, което води до променен метаболизъм, генна експресия, модифицирана реакция на хормони и модели на производство на биологично активни вещества. Следователно, мастните киселини могат да модулират физиологичните функции и потенциално полезни за насърчаване на здравето и благосъстоянието [31].
В допълнение, някои данни сочат, че PUFAs омега-3 (n-3), главно ейкозапентаенова киселина (EPA) и докозахексаенова киселина (DHA), могат да допринесат за подобряване на няколко метаболитни дисфункции (напр. Повишаване на глюкозния толеранс, чувствителност към инсулин и намаляване на риска фактори за хронични незаразни заболявания и метаболитен синдром) [32-39].
Освен това, скорошно проучване показа, че пречистените EPA и DHA имат различни ефекти върху развитието на атерогенно високо съдържание на мазнини (AHF) NAFLD на диета, индуцирано заболяване при мишки. EPA и DHA намаляват протеина SREBP-1 и експресията на липогенни гени. Въпреки това, EPA е по-ефективен от DHA за намаляване на иРНК експресията на FAS, (член на семейство ELOVL 6) Elovl6 и глицерол-3-фосфат ацилтрансфераза (GPAT-1). Авторите също така показват, че клетъчната експресия, предизвикваща DFFA като ефектор c (CIDEC), протеин, разположен в липидни капчици, играещ ключова роля в образуването на мастен черен дроб, е значително потиснат в AHF + EPA, но не и в групата AHF + DHA 52]. Ето защо е важно да се има предвид, че тези PUFA (EPA и DHA) имат специфични цели, но могат да допринесат заедно за намаляване на натрупването на мастни киселини в черния дроб.
Изследвани са допълнителни механизми за допълнително изясняване на ефектите на EPA и DHA върху метаболизма на черния дроб в липидите. Мишките, хранени с WD, съдържаща треска (рибен източник на EPA и DHA), показват значително повишаване на концентрациите на EPA и DHA и затихване в натрупването на чернодробна мазнина, придружено от промяна в тонуса на ендоканабиноидната система. Наличието на по-високи концентрации на EPA и DHA, в сравнение с арахидоновата киселина, води до намаляване на синтеза на 2-арахидоноилглицерол (2-AG), N-арахидоноилетаноламин (AEA) и увеличава наличността на субстрат за образуването на ендоканабиноид производни от EPA и DHA (например ейкозапентаеноил етаноламид (EPEA) и докозахексаеноил етаноламид (DHEA), съответно). Този механизъм може отчасти да обясни затихването на нарастването на чернодробните липиди и развитието на затлъстяване при мишки, хранени с WD и треска [54].
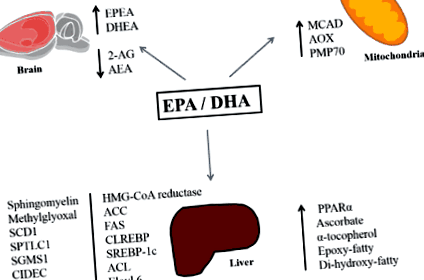
По този начин, най-новата литература показва, че EPA и DHA (n-3 PUFAs, присъстващи в рибеното масло и мазна риба) могат да намалят натрупването на липиди в черния дроб при предклинични модели. Такива ефекти са свързани не само с n-3 мастни киселини, влияещи върху активността на протеините, участващи в липогенезата и а-окислението, но и с метаболитни окислителни ензими и промени в тонуса на ендоканабиноидната система (Фигура 1). По-нататъшни изследвания трябва да изследват тези механизми, особено различните ефекти на EPA и DHA върху специфични молекулярни цели. Това може да ни доведе до следващото поколение ефективни терапевтични подходи.
Фигура 1. Обобщение на молекулярните ефекти на EPA и DHA, свързани с намаляването на чернодробното натрупване на липиди. Съкращения: EPA: ейкозапентаенова киселина, DHA: докозахексаенова киселина, EPEA: ейкозапентаеноил етаноламид, DHEA: докозахексаеноил етаноламид, 2-AG: 2-арахидоноилглицерол, AEA: N-арахидоноилетанолаил, MCAD-АКГА: дезагеноазил, MCAD-ацетил-ацетил-ацетилхлорид, MCAD-ацетаноламин, MCAD-ацетил-ацетил-ацетат, MCAD CoA оксидаза, PMP70: пероксизомален мембранен протеин 70, SCD1: стеароил-CoA десатураза-1, SPTLC1: серин-палмитоил трансфераза, дълга верига, субединица-1, SGMS1: фосфатидилхолин: церамид холин фосфотрансфераза 1, CFAEC: ефект, предизвикващ смърт, DFFA GPAT-1: глицерол-3-фосфат ацилтрансфераза, ACC: ацетил-КоА карбоксилаза, FAS: синтаза на мастни киселини, SREBP-1c: белтък, свързващ елемент на регулацията на стерол 1c, ACL, Elovl 6: член на семейството на ELOVL 6, PPAR ?: пероксисом пролифератор активиран рецептор- ?, ChREBP: протеин, свързващ елемент с въглехидрати
Конфликт на интереси
Авторите потвърждават, че няма конфликт на интереси.
Авторски вноски
Авторите заедно допринесоха за подготовката на дизайна на статията, писането и критичния преглед на интелектуалното съдържание на статията, както и одобрението на окончателната версия.
Препратки
Главен редактор
Тип на статията
История на публикациите
Дата на получаване: 2 ноември 2016 г.
Приета дата: 14 декември 2016 г.
Дата на публикуване: 19 декември 2016 г.
Цитат
Barbosa AM, Chagas TR, Nunes EA (2016) Поглъщане на мастен черен дроб и n-3 мастни киселини: Нови механизми и перспективи от предклинични животински модели. Чернодробна панкреатична наука 1: DOI: 10.15761/LPS.1000104.
Автора за кореспонденция
Еверсън Араухо Нунес
Департамент по физиологични науки, Център за биологични науки, Федерален университет в Санта Катарина (UFSC) 88040-900, Флорианополис, Бразилия
Фигура 1. Обобщение на молекулярните ефекти на EPA и DHA, свързани с намаляването на чернодробното натрупване на липиди. Съкращения: EPA: ейкозапентаенова киселина, DHA: докозахексаенова киселина, EPEA: ейкозапентаеноил етаноламид, DHEA: докозахексаеноил етаноламид, 2-AG: 2-арахидоноилглицерол, AEA: N-арахидоноилетанолаил, MCAD-АКГА: дезагеноазил, MCAD-ацетил-ацетил-ацетилхлорид, MCAD-ацетаноламин, MCAD-ацетил-ацетил-ацетат, MCAD CoA оксидаза, PMP70: пероксизомален мембранен протеин 70, SCD1: стеароил-CoA десатураза-1, SPTLC1: серин-палмитоил трансфераза, дълга верига, субединица-1, SGMS1: фосфатидилхолин: церамид холин фосфотрансфераза 1, CFAEC: ефект, предизвикващ смърт, DFFA GPAT-1: глицерол-3-фосфат ацилтрансфераза, ACC: ацетил-КоА карбоксилаза, FAS: синтаза на мастни киселини, SREBP-1c: белтък, свързващ елемент на регулацията на стерол 1c, ACL, Elovl 6: член на семейството на ELOVL 6, PPAR ?: пероксисом пролифератор активиран рецептор- ?, ChREBP: протеин, свързващ елемент с въглехидрати
- Изключително затлъстело лице с най-висок риск от затлъстяване на черния дроб MedPage днес
- Диета за дебел черен дроб LoveToKnow
- Диетичният капсаицин и антибиотиците действат синергично за намаляване на безалкохолната мастна чернодробна болест
- Диетични мастни киселини Време ли е да се променят препоръките FullText - Annals of Nutrition и
- Диетични мастни киселини Hammer Nutrition