1 Катедра по фармация, Фармацевтичен факултет, Университет в Печ, Печ, Унгария и MedBioFit Lpc. Fácán sor 25. Gödöllö, Унгария
Автора за кореспонденция: Ищван Г. Телеси
Адрес: Катедра по фармация, Фармацевтичен факултет, Университет в Печ, Печ, Унгария и MedBioFit Lpc. Fácán sor 25. Gödöllö, Унгария.
Дата на получаване: 15 февруари 2019; Приета дата: 11 март 2019; Дата на публикуване: 18 март 2019
Цитат: Telessy IG, „Позицията на диета с ниско съдържание на въглехидрати в адювантната терапия на рака: Клинично хранене с диета с ниско съдържание на въглехидрати при пациенти с рак“. Asp Biomed Clin Case Rep, том 2, № s1: 28-33, 2019.
Ключови думи: Диета с ниско съдържание на въглехидрати (LCD); Кетогенна диета (KD); Глюкозен метаболизъм; Туморна терапия; Пациент с рак; Клинично хранене
Въведение
Физиологичен фон
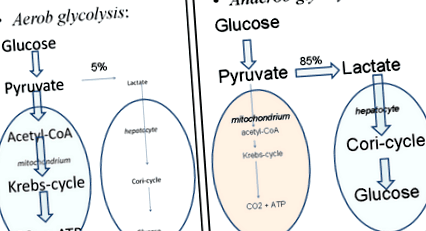
Енергията на здрави (статични, непролифериращи) клетки се произвежда в митохондриите, където по-голямата част от АТФ се генерират окончателно чрез най-ефективната аеробна гликолиза. Противно на това, при липса на кислород анаеробната гликолиза доставя много по-малко АТФ, а също така се ражда млечна киселина, която не може да влезе в митохондрията. Следователно основният път за производство на енергия, цикълът на Кребс отпада от анаеробния процес (Фиг. 1).
Фиг. 1: Схематично сравнение на аеробна и анаеробна гликолиза
Основният източник на енергия за човешкото тяло е въглехидратната група (захари, нишесте и др.). Тези субстрати се метаболизират извънклетъчно до глюкоза, която постъпва в клетките чрез глюкозни транспортери (GLUTs). Тези мембранни протеини присъстват във всяка клетка в различно количество и освен транспортните функции, те играят роля и на рецептор. Някои от GLUT-протеините се концентрират в специални клетки, като GLUT-4 в мускулни клетки и адипоцити, и при специални условия като гладуване, GLUT-4 се съхранява във вътреклетъчните везикули. В случай на хранене - въз основа на инсулиновата сигнализация - молекулите GLUT-4 се преместват в плазмената мембрана и улесняват навлизането на глюкоза в клетката.
Глюкозата - в присъствието на кислород - се трансформира до пируват, който навлиза в митохондриите и се метаболизира по-нататък до ацетил-КоА единици, които произвеждат - чрез цикъла на Кребс - енергия. Целият процес - наречен аеробна гликолиза - произвежда 10 NADH + 2 FADH2 + 2 GTP + 2 ATP всички заедно - преведени в молекули ATP - води до 38 ATPs на молекула глюкоза, за разлика от анаеробната гликолиза, която произвежда 2 NADH + 2 ATP всички заедно 8 ATP само до лактат (Фиг. 2).
Фиг. 2: Схематично производство на енергия при анаеробна и аеробна гликолиза
В митохондрията има и друг (алтернативен) път за производство на енергия, където суровината е мазнина, а не въглехидрати. В случай на гладуване или внезапна нужда от допълнителна енергия, този път доставя АТФ и кетонни тела (Фиг. 3). Последните могат да се използват от неврони (мозък), мускулни клетки (сърдечни клетки също) и адипоцити. Тъй като производството на кетонни тела (главно ацетоацетат, по-късно ацетон и бета-хидроксибутират) се нуждае от специални митохондриални ензими, тези молекули се произвеждат само в митохондриите.
Фиг-3: Схематично представяне на пълното разлагане на мастните киселини и образуването на кетонното тяло
Патофизиологичен фон в туморни клетки
Фиг-4: Сравнение на метаболизма на глюкозата на здрави и ракови клетки
Диета с ниско съдържание на въглехидрати (LCD)
Клинично хранене с диета с ниско съдържание на въглехидрати
Дадохме подробности за ограничаването на въглехидратите, което води до намаляване на източниците на енергия, както и до изграждане на блокове за нови протеини за пролифериращи клетки. Не споменахме, но има някакъв допълнителен ефект на LCD върху имунологичния и хормоналния статус и въздействието на предаването на сигнала на всички жизнени процеси. Всички тези действия подкрепят клиничното използване на LCD в рамките на терапия на рак.
Днес нямаме доказателства, които да твърдят, че диетата с ниско съдържание на въглехидрати е еднакво ефективна от хирургичната, цитостатичната или лъчетерапията, но са публикувани много повече положителни, отколкото отрицателни клинични преживявания. Полезните предполагаеми действия срещу растежа на тумора бяха демонстрирани - в допълнение към гореспоменатите проучвания за безопасност - при група от рак на мозъка [16], рак на главата и шията [17], рак на гърдата [18] и пациенти с рак на щитовидната жлеза [19]. Този тип адювантна терапия към споменатите класически интервенции хранителна терапия се приема все повече и повече. LCD изглежда е ценна част от хранителната терапия в мултидисциплинарните грижи за тумора [20]. Това е направено в заключение от три кохортни проучвания при хора и 17 експеримента върху животни с ограничаване на калориите и/или кетогенни диети като монотерапия или комбинация с други терапевтични интервенции за оцеляване и на пациенти с глиом с висока степен [21].
- Тройно отрицателен рак на гърдата - диета и хранене - CareAcross
- Връзката между диетата, затлъстяването и рака Експертите по храненето изследват доказателствата Диетични и
- Какъв тип диета е най-подходяща за хора с предишна храна за диагностика на рака; Списание за хранене
- Възникващата роля на затлъстяването, диетата и липидния метаболизъм при рак на простатата
- Елементите на здравословния хранителен режим - хранене на майки, кърмачета и малки деца; Недохранване - Хранене