Олга Карлсън
1 Секция за диабет, Лаборатория за клинично изследване, Национален институт за програма за интрамурални изследвания за стареене, Балтимор, д-р
Бронвен Мартин
2 Лаборатория по невронауки, Национален институт за стареене Интрамурална изследователска програма, Балтимор, д-р
Ким С. Стоте
3 Изследователски център за човешко хранене Beltsville, Министерство на земеделието на САЩ, Служба за земеделски изследвания, Beltsville, MD
Ерин Голдън
2 Лаборатория по невронауки, Национален институт по програма за интрамурални изследвания за стареене, Балтимор, д-р
Стюарт Модсли
2 Лаборатория по невронауки, Национален институт по програма за интрамурални изследвания за стареене, Балтимор, д-р
Самер С. Найджар
4 Лаборатория по сърдечно-съдови науки, Национален институт по програма за интрамурални изследвания за стареене, Балтимор, д-р
Луиджи Феручи
5 Клиничен изследователски клон, Национален институт за стареене Интрамурална програма за изследвания, Балтимор, д-р.
Доналд К. Инграм
6 Лаборатория по експериментална геронтология, Национален институт за стареене Интрамурална програма за изследвания, Балтимор, д-р
Дан Л. Лонго
7 Лаборатория по имунология, Национален институт за стареене Интрамурална програма за изследвания, Балтимор, д-р
Уилям В. Румплер
3 Изследователски център за човешко хранене в Белтсвил, Министерство на земеделието на САЩ, Служба за земеделски изследвания, Белтсвил, MD
Дейвид Дж. Баер
3 Изследователски център за човешко хранене в Белтсвил, Министерство на земеделието на САЩ, Служба за земеделски изследвания, Белтсвил, MD
Джоузефин Игън
1 Секция за диабет, Лаборатория за клинично изследване, Национален институт за програма за интрамурални изследвания за стареене, Балтимор, д-р
Марк П. Матсън
2 Лаборатория по невронауки, Национален институт по програма за интрамурални изследвания за стареене, Балтимор, д-р
Резюме
1. Въведение
Глюкозната непоносимост и инсулиновата резистентност са видни характеристики на диабет тип 2 [1], а по-финото увреждане на глюкозния толеранс може да увеличи риска от диабет, сърдечно-съдови заболявания и инсулт [2, 3]. Такива „преддиабетни“ състояния при иначе здрави индивиди се характеризират с умерено повишаване на плазмените нива на глюкоза и инсулин на гладно и променени времеви профили на плазмените нива на глюкоза и инсулин в теста за орален глюкозен толеранс (OGTT) с по-големи и по-трайни повишения на нива на глюкоза и забавен инсулинов отговор [4–6]. Намалената инсулинова чувствителност на скелетните мускулни клетки и намалената реакция на панкреасните бета-клетки допринасят за нарушен глюкозен толеранс [7].
Адипокините са хормони, произвеждани от мастните клетки в отговор на хранене или гладуване, които могат да играят важна роля в развитието на затлъстяване и диабет [1]. Например, нивата на циркулиращия лептин се увеличават при индивиди със затлъстяване и диабет, а резистентността към лептин в хипоталамусните клетки, които обикновено потискат приема на храна, вероятно допринася за преяждането при тези условия [8, 9]. Нивата на циркулиращия адипонектин са ниски, а нивата на резистин повишени при лица със затлъстяване и инсулин резистентни [10]. Ролите на промените в адипокините обаче при нарушен метаболизъм на глюкозата са неясни. В допълнение към инсулина и адипокините, наскоро се предлага невротрофичен фактор, получен от мозъка (BDNF), да играе роля в метаболизма на глюкозата. Изследвания на BDNF хетерозиготни нокаутиращи мишки [11], затлъстели и диабетни животни, прилагани BDNF [12, 13] и хора с диабет тип 2 [14] предполагат, че BDNF сигнализирането повишава инсулиновата чувствителност. Антидиабетно действие на BDNF при хора се предполага от скорошно проучване, което демонстрира обратна връзка между нивата на BDNF на гладно и нивата на глюкозата, но не и нивата на инсулин [14]. Въпреки това, ефектите от вариациите в приема на диетична енергия върху нивата на BDNF при хората са неизвестни.
2. Предмети и методи
Предмети и дизайн на обучение
Подробности за характеристиките на предмета и дизайна на изследването са докладвани по-рано [29]. Накратко, субектите бяха здрави 40-50-годишни мъже и жени с индекси на телесна маса между 18 и 25 kg/m 2 с обичайно хранене от три хранения на ден. Вписването в проучването е одобрено от лекар въз основа на медицинска история, скрининг на резултати от изследвания на кръв и урина и физически преглед. Протоколът е одобрен от Комитета по изследване на човека на Университета Джон Хопкинс и Институционалния съвет за изследване на MedStar. Всички субекти дадоха своето информирано съгласие и получиха компенсация за участието си в изследването. Всеки субект е преминал през два 8-седмични контролирани периода на диета, през които е консумирал всичките си калории за поддържане на теглото или в 3 хранения/ден (закуска, обяд и вечеря), или в 1 хранене/ден (през 4-часов период рано вечер; 16:00 - 20:00 часа) в рандомизиран дизайн на кръстосано изпълнение с 11-седмичен период извън диетата между двата контролирани периода на диета. В експерименталната диета хранителните продукти за закуска и обяд бяха заменени от традиционните артикули за вечеря; съставът на диетите е докладван по-рано (28). По време на проучването енергийният прием се коригира, за да се поддържа постоянно телесно тегло.
Тест за толерантност към глюкоза и измерване на нивата на хормоните
Изчисляване на инсулиновата чувствителност
Ние определихме количествено инсулиновата чувствителност чрез изчисляване на оценката на хомеостатичния модел на инсулинова резистентност (HOMAIR), използвайки нивата на глюкоза и инсулин на гладно [31]. Също така изчислихме индекса на инсулинова чувствителност (ISI), скоростите на метаболитен клирънс (MCR), β-клетъчната функция по време на секреция на първа фаза (β-клетъчна функция, първа фаза) и секреция на втора фаза β-клетъчна функция, втора фаза) (както и като орална чувствителност към глюкоза и инсулин (OGIS: 0, 90 [средна стойност от 80 и 100 минути стойност] и 120) [32–35].
Статистически анализ
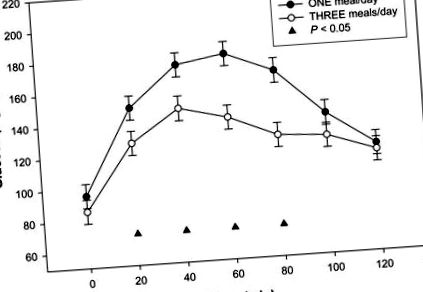
Плазмени концентрации на глюкоза по време на оралните тестове за глюкозен толеранс през всеки период на изследване. Данните са представени като най-малкото квадратче означава ± SEM, n = 15 (10 жени, 5 мъже), от многократно измерване ANOVA. Имаше значителен ефект от лечението между 1 хранене/ден (●) и 3 хранения/ден (○) за OGTT на 20 минути, 40 минути, 60 минути и 80 минути, ▲ P ▲
| Глюкоза mg/dl | 95,9 ± 1,7 | 85,4 ± 1,7 | 0,0002 |
| Инсулин μU/ml | 5,0 ± 0,7 | 5,8 ± 0,7 | 0,4329 |
| Глюкагон pg/ml | 66,5 ± 7,7 | 62,1 ± 7,4 | 0,6878 |
| HOMA-IR | 1,2 ± 0,2 | 1,3 ± 0,2 | 0,8718 |
| OGIS | 403,4 ± 14,0 | 458,8 ± 13,9 | 0,0114 |
| ISI | 0,1 ± 0,004 | 0,1 ± 0,004 | 0,6552 |
| MCR | 8,8 ± 0,3 | 9,2 ± 0,3 | 0,4011 |
| β-клетъчна функция 1-ва фаза | 782,1 ± 66,0 | 1013,85 ± 66,1 | 0,0209 |
| β-клетъчна функция 2-ра фаза | 239,0 ± 19,0 | 253,7 ± 19,0 | 0,5894 |
| Адипонектин pg/ml | 13,5 ± 1,3 | 13,5 ± 1,3 | 0,9919 |
| Резистин ng/ml | 3,1 ± 0,3 | 2,8 ± 0,2 | 0,4147 |
| Лептин ng/ml | 20,2 ± 2,2 | 16,1 ± 2,1 | 0,18 |
| Грелин pg/ml | 163,2 ± 12,8 | 158,4 ± 12,8 | 0,7942 |
| BDNF ng/ml | 141,7 ± 26,7 | 148,1 ± 26,6 | 0,8175 |
Няма значими ефекти от честотата на хранене върху HOMA-IR, ISI или MCR (Таблица 1). Стойностите на OGIS обаче са значително по-ниски при субектите на 1 хранене/ден в сравнение с 3 хранения/ден (Таблица 1). Освен това, при едно хранене/ден стойностите за 1-ва фаза на функцията на β-клетките са значително по-ниски от стойността при 3 хранения/ден (Таблица 1). Стойностите за втората фаза на функцията на β-клетките не се повлияват значително от диетата.
За да се изяснят допълнително ефектите от честотата на хранене без калорични ограничения върху енергийния метаболизъм, ние измерихме нивата на гладно на няколко адипокини, за които е известно, че играят важна роля в регулирането на енергийния баланс. Плазмената концентрация на грелин на гладно е подобна при субектите на 1 хранене/ден или 3 хранения/ден (Таблица 1). Няма значими ефекти от диетата върху плазмените концентрации на грелин по време на OGTT, въпреки че нивата са склонни да бъдат по-ниски при субекти, когато са били на 1 хранене/ден за времеви точки между 40 и 100 минути след поглъщането на глюкоза (Фиг. 3) Диетата няма значителни ефекти върху сутрешните плазмени концентрации на глюкагон, лептин, адипонектин, резистин и BDNF (Таблица 1).
Плазмени концентрации на грелин по време на оралните тестове за толерантност към глюкоза през всеки период на изследване. Данните са представени като най-малкото квадратче означава ± SEM, n = 15 (10 жени, 5 мъже), от многократно измерване ANOVA. Нямаше значим ефект на лечение между 1 хранене/ден (●) и 3 хранения/ден (○) за плазмени концентрации на грелин по време на оралния тест за глюкозен толеранс.
4. Дискусия
Причината за нарушения сутрешен толеранс към глюкоза при субекти, консумиращи 1 хранене/ден в сравнение с 3 хранения/ден, е неясна. Съобщава се, че концентрациите на инсулин, лептин и глюкагон на гладно са повишени при пациенти с нарушен глюкозен толеранс [36, 37]. В настоящото проучване обаче няма значителни ефекти от диетата върху концентрациите на последните хормони. По същия начин няма значителни ефекти от честотата на хранене върху плазмените нива на грелин, адипонектин, резистин или BDNF. По този начин, въпреки че нивата на инсулин на гладно и на адипокин не се различават между двете диетични групи, инсулиновата чувствителност очевидно е намалена при субектите, когато консумират 1 хранене/ден. Всъщност стойностите за OGIS и функцията на бета-клетките от 1-ва фаза са значително по-ниски при субектите, когато те консумират 1 хранене/ден в сравнение с изходните стойности, 3 хранения/ден и стойности извън диетата. Последните резултати предполагат относително увреждане на инсулиновата чувствителност и панкреатичните β-клетъчни инсулинови отговори при пациенти на 1 хранене/ден в сравнение с 3 хранения/ден.
OGTTs се извършват сутрин. Следователно, когато на 1 хранене/дневна диета субектите са консумирали много по-голямо количество храна в близост до OGTT в сравнение с пациенти на 3 хранения/ден, което би могло да повлияе сутрешната чувствителност към инсулин. Освен това са документирани циркадни вариации в глюкозния толеранс, като толерантността е най-добра сутрин [38]. Когато не са свикнали със сутрешно хранене и след това са подложени на сутрешно OGTT, субектите, които ядат 1 хранене/ден, могат да проявят по-лош глюкозен толеранс в сравнение с тези, адаптирани към закуската. Въпреки това, настоящият начин на хранене от западното общество да консумира най-голямото ядене вечер изглежда не е адаптивен начин на живот.
Благодарности
Това изследване беше подкрепено от Програмата за вътрешни изследвания на Националния институт за стареене. Благодарим на К. Спиърс за техническа помощ.
Бележки под линия
Отказ от отговорност на издателя: Това е PDF файл на нередактиран ръкопис, който е приет за публикуване. Като услуга за нашите клиенти ние предоставяме тази ранна версия на ръкописа. Ръкописът ще бъде подложен на редактиране, набиране и преглед на полученото доказателство, преди да бъде публикуван в окончателния си вид. Моля, обърнете внимание, че по време на производствения процес могат да бъдат открити грешки, които биха могли да повлияят на съдържанието, и всички правни откази от отговорност, които се отнасят до списанието, се отнасят до.
- То; Доказано е, че времето ни на хранене оказва влияние върху нашето наддаване на тегло Web24 News
- План за хранене Mesomorph Здравословно хранене SF Gate
- Как влияе кафето на отслабването е кафето здравословен фитнес блендер
- Джой Бауер; s 7-дневен план за хранене за здравословна седмица
- Отслабнете с този здравословен план за хранене от фитнес треньор на жените