1 Отделение по ортопедична хирургия, Служба за гръбначен стълб, Болница за специална хирургия, Ню Йорк, NY 10021, САЩ
Резюме
Болката в кръста в резултат на дегенеративна дискова болест придава голямо социално-икономическо въздействие върху здравната система. Традиционните концепции за лечение на дегенерация на лумбален диск са насочени към симптоматично облекчаване чрез ограничаване на движението в лумбалния отдел на гръбначния стълб, но новите стратегии за лечение, включващи стволови клетки, растежни фактори и генна терапия, имат теоретичния потенциал за предотвратяване, бавна или дори обратна дегенерация на диска. Разбирането на патофизиологичната основа на дегенерацията на диска е от съществено значение за разработването на стратегии за лечение, насочени към основните механизми на дегенерация на диска, а не към симптома на болката надолу по веригата. Такива стратегии в идеалния случай имат за цел да предизвикат регенерация на диска или да заменят дегенерирания диск. Понастоящем обаче възможностите за лечение на дегенеративно дисково заболяване остават неоптимални и развитието и резултатите от новите възможности за лечение понастоящем трябва да се считат за непредсказуеми.
1. Въведение
Болката в кръста (LBP) е единствената най-честа причина за увреждане при лица на възраст 45 години или по-млади и в резултат на това има огромна тежест в социално-икономически съображения. Националните икономически загуби, произтичащи от LBP, се изчисляват на над 100 милиарда щатски долара годишно и са главно косвени поради намалената производителност [1]. Въпреки че рентгенографските признаци на дегенеративно заболяване на диска (DDD) са показани при асимптоматични индивиди [2] и степента на дегенерация по никакъв начин не е маркер за продължителност или тежест на симптомите, свързани с DDD, начини за ограничаване на дегенерацията на диска или дори индуциране на диск регенерацията все още са желани цели при нейното лечение.
Стратегиите за спиране или обръщане на дегенерация на диска в лумбалния отдел на гръбначния стълб варират от възможности за механично лечение, които разчитат на традиционната концепция за премахване на генератора на болка, диска и премахване на болката чрез спиране на движението, до съвсем наскоро възникващи и развиващи се възможности за лечение, включващи генна терапия, растежни фактори и клетъчни трансплантации. Традиционният подход на хирургичната операция за елиминиране на движенията, която в някои случаи може да бъде ефективна за лечение на болка, може също да увеличи скоростта на дегенерация в съседните сегменти на гръбначния стълб. Освен това, тази стратегия не спира развитието на дегенеративната каскада от събития, която води до болка и увреждане. Така че въпреки неоспоримото си значение, операцията за лумбален синтез като лечение на LBP трябва да се счита за неоптимална, тъй като тя е насочена към симптома на болката, а не към нейните причини. Съвременната ера на молекулярната биология донесе революционен напредък в области като геномика, нанотехнологии, биология на стволови клетки, генна терапия и тъканно инженерство, които заедно притежават огромен терапевтичен потенциал за клинични приложения при дегенеративни разстройства като DDD.
2. Патофизиология на дисковата дегенерация
2.1. Анатомия и инервация на междупрешленния диск
Междупрешленният диск (IVD) се състои от ядрото пулпоз (NP) централно, пръстеновидният фиброз (AF) периферно и хрущялните крайни пластини черепно-каудално в кръстовището с телата на гръбначните прешлени. В рамките на NP изобилието от протеогликани позволява абсорбцията на вода. Това свойство на NP е от съществено значение за обработката на аксиалните товари на IVD. В здравия диск най-често срещаният тип колаген в NP е колаген тип II. AF обгражда NP и се състои предимно от тип I колаген.
Описанията на инервацията на IVD са публикувани преди повече от 20 години [3]. Счита се, че клоновете на синувертебралния нерв, гръбначните нерви и сивите rami communicantes [4] са част от неврологичната основа за дискогенна болка в гърба. Съобщава се за увеличаване на нервните влакна и кръвоносните съдове в болезнения диск, достигайки до областите на пръстеновидния фиброз и пулпозното ядро, които обикновено са аневрирани в здравия диск, и се предлага корелация между тези находки и нивата на експресия на невротрофините [5].
2.2. Стареене и дегенерация
Процесът на дегенерация се сравнява с процеса на стареене в много отношения. Дегенерацията на диска обаче често се случва с по-бързи темпове, което прави DDD състояние, което често се среща при пациенти в трудоспособна възраст. Количественият анализ на генната експресия в заешки модел предполага възрастта да допринесе уникално за процеса на дегенерация в сравнение с модела на дегенерация, причинен от нараняване [6]. С увеличаване на възрастта съдържанието на вода в IVD намалява и могат да се появят пукнатини в NP, потенциално простиращи се в AF, и началото на този процес, наречен hondrosis intervertebralis, може да отбележи началото на дегенеративното разрушаване на IVD, крайните плочи, и телата на прешлените [7]. DDD е сложен дегенеративен процес, дължащ се на възрастови промени в молекулярния състав на диска. Тази каскада има биомеханични и често клинични последствия, които могат да доведат до значително увреждане на страдащия индивид.
2.3. Генетичен компонент на дегенерацията
Неоспорим генетичен компонент на дегенеративното заболяване на диска става очевиден, когато се разглеждат резултати от изследвания на близнаци и проучвания, включващи мишки с нокаут за гени, за които се предполага, че играят роля в дегенерацията на диска [8, 9]. Сред гените, за които се предполага, че участват в DDD, са гени, които кодират колагени I, IX и XI, интерлевкин 1 (IL-1), агрекан, рецептор за витамин D, матрична металопротеиназа 3 (MMP-3) и други протеини [10]. Добре известно е, че DDD се регулира от тези и много други гени. Взаимодействията между тези гени, които съвместно допринасят значително за DDD, въпреки предполагаемо малките индивидуални приноси, както и взаимодействията между гените и околната среда, са много вероятни [11].
2.4. Фактори на околната среда
Много специалисти смятат, че факторите на околната среда са второстепенно съображение за генетичния компонент на ДДД. Независимо от това, влиянието на факторите на околната среда върху DDD е далеч от пренебрежимо малко и е дефинирано изчерпателно от Уилямс и Самбрук през 2011 г. [12]. При мета-анализ съотношенията на шансовете за ръчно боравене с материали, често огъване или усукване и вибрации на цялото тяло са изчислени съответно на 1,51, 1,68 и 1,39 по отношение на DDD [13]. Показана е умерена връзка между тютюнопушенето и дегенерацията на диска, което предполага възможни влияния на химическото въздействие [14]. Twin [15], както и проучвания върху животни [16] предполагат, че никотинът участва в дегенерацията на диска, което може да се дължи на нарушен приток на кръв към диска [17]. Освен това се съобщава за асоцииране на атеросклеротични лезии в аортата и LBP, отразяващо възможна връзка между атеросклерозата и DDD [18].
3. Клинично представяне
Пациентите с болест на лумбалния диск често се представят с безброй симптоми, включително болка, радикуларни симптоми и слабост. LBP може да се влоши от положение и движение. Флексията често влошава симптомите, докато удължаването ще ги облекчи. Увеличаването на болката с удължаване може да показва фасетна артропатия.
Когато се изследват пациенти с предполагаем лумбален DDD, е важно да се изключат други потенциални известни етиологии за тяхната болка. Трябва да се изключат коремни патологии, включително аортни аневризми, панкреатични заболявания и бъбречни камъни. Освен това е наложително пациентите да бъдат разпитвани относно други симптоми като треска, студени тръпки, умора и загуба на тегло, което може да е показателно за друга патология.
4. Диагностика
Изправените обикновени рентгенографии в две равнини са първоначално избрано образно изследване. Те помагат при изключването на патологии като деформация, фрактури или метастатичен рак като основни причини за болки в гърба и, често допълнени от други методи за изобразяване, се оценяват за признаци на дегенерация. Констатациите в дегенеративните дискове включват стесняване на дисковото пространство, склероза на крайната плоча, явление „вакуум“ в диска и остеофити. Изгледите за сгъване и разширение могат да бъдат полезни, ако се подозира нестабилност.
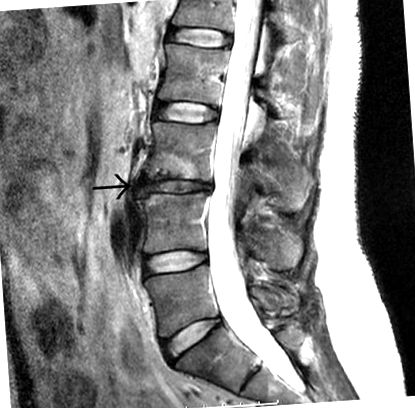
Ядрено-магнитен резонанс (ЯМР) е по-чувствително образно изследване за оценка на дегенеративно заболяване на диска. Констатациите при MRI сканиране включват стесняване на дисковото пространство, загуба на Т2 сигнал в пулпозното ядро, промени в крайната плоча и признаци на вътрешно разстройство на диска или разкъсвания (Фигура 1). Зони с висока интензивност (HIZ) са открити при близо една трета от пациентите, подложени на ЯМР за болки в кръста и са били използвани като маркер за нарушение на вътрешния диск. Точността и надеждността на тези HIZ обаче са поставени под въпрос [19, 20].
Modic и сътр. са едни от първите, които характеризират рентгенологично промени в гръбначните крайни пластини, свързани с дегенеративно заболяване на диска [21, 22]. Системата за класификация на Modic включва три вида промени и класирането е доказано надеждно и възпроизводимо [23]. При тип I има повишен сигнал на Т2-претеглената последователност и намалена интензивност на сигнала на Т1 последователности, което е показателно за мозъчен оток. Тип II се характеризира с мастна инфилтрация в костния мозък, както се демонстрира от хиперинтензивни изображения на Т1 и Т2. И накрая, тип III демонстрира хипоинтензивни сигнали на последователности Т1 и Т2, което съответства на склерозата на крайната плоча. Типовете Modic са обобщени в таблица 1.
Pfirrmann et al. допълнително изследва и охарактеризира патологията на междупрешленните дискове с помощта на ЯМР [24]. Степента на дегенерация на дисковете се степенува от I до V. Дисковете от степен I са бели и хомогенни за Т2 последователности. Дисковете от степен II са бели, но донякъде нехомогенни с ленти. Дисковете от степен III са сиви с неясно разграничение между ядрото и пръстена. Дисковете от степен IV са нехомогенни и тъмни, без разлика между ядрото и пръстена. И накрая, дисковете от степен V демонстрират свито пространство на диска. Системата за оценяване на Pfirrmann е представена в таблица 2.
Докато обикновените рентгенови снимки и ЯМР предоставят информация относно здравето на междупрешленния сегмент, те не предоставят никаква информация относно въздействието на сегментите върху клиничните симптоми. Използването на дискография се опита да идентифицира специфични дегенерирани дискове като генератори на болка [25]. Провокативната дискография включва инжектиране на контрастно багрило в ядрото. Компютърната томография се използва за оценка на екстравазацията на багрилото, показващо пръстеновидни разкъсвания. Симптомите на пациента и вътредисковото налягане по време на инжектирането също се записват. Ако болката при инжектиране е подобна на болката в гърба, тогава дискограмата се счита за съгласувана. Също така, ако болката се произвежда при ниско налягане, се смята, че има симптоматично пръстеновидно нарушение или вътрешно разстройство. Въпреки това, ако болката е различна или се получава при високо налягане на инжектиране, тестът често се счита за несъответстващ. И все пак е установено, че дискографията с ниско налягане има фалшиво положителни нива до 25% при асимптоматични индивиди и може да ускори дегенерацията на диска [26, 27].
5. Стратегии за лечение на лумбална дегенеративна дискова болест
5.1. Механични концепции за регенерация на лумбалния диск
Операцията на гръбначен синтез е призната възможност за лечение на LBP, но нейната ефикасност и успех остават противоречиви. Това може да бъде постигнато чрез различни подходи и техники, включително постеролатерално сливане, сливане на предната лумбална част на тялото и задно сливане на лумбалната част на тялото. Минимално инвазивните подходи към лумбалната част на гръбначния стълб за сливане между тела, като странично лумбално сливане между тялото, придобиват популярност през последните 5 години [28].
Друга потенциална операция за запазване на движението включва задна динамична стабилизация. Тези системи включват поставяне на винтове на педикулите през сегмент на движение, свързан с гъвкав присадка. Тези устройства са проектирани да ограничават движението през междупространството, за да ограничат дискогенната болка [35]. Ранното проследяване на тази техника демонстрира някои обещаващи резултати при лечението на дискогенна болка в гърба по отношение на подобрените резултати за VAS и ODI [36, 37]. По-дългосрочните проучвания обаче демонстрират съседно заболяване на сегмент при 29–47% от пациентите [38–40].
5.2. Клетъчни терапии и фактори на растежа при дегенерация на лумбалния диск
Въпреки че има разнообразие от инвазивни хирургически възможности за лечение на лумбална дегенеративна дискова болест, напоследък акцентът е насочен към обръщането на дегенерацията на диска или замяната на засегнатия диск. Изследвани са различни терапии, включително биологични растежни фактори, стволови клетки и генна трансплантация. Докато тези нови терапевтични модалности са показали някои ранни обещаващи резултати по отношение на обръщането на дегенеративната каскада, техните клинични ефекти и дългосрочни резултати са несигурни [41]. Също така не е ясно дали диференциацията на стволови клетки в зрели тъкани може да ги накара да експресират имуногенни маркери, което в крайна сметка може да доведе до отхвърляне на стволови клетки.
Трансплантацията на стволови клетки се очерта като друга обещаваща стратегия за лечение на DDD [40, 50-52]. Неотдавнашни проучвания върху животни показват повишена извънклетъчна матрица, когато автоложни дискови хондроцити са въведени в модел на дегенерация на кучешки диск. Освен това, скорошно проучване при хора, включващо въвеждането на автоложни хондроцити при пациенти с постдискектомия, е довело до намаляване на болката след 2 години в сравнение с контролите. Също така, имаше повишена хидратация на диска на третираните нива и съседните нива, както се вижда от MRI оценка [53].
Алтернативна техника на трансплантацията на хрондроцити е използването на адипоцитни прогениторни клетки. Предимството на тази техника е относителното изобилие на стволови клетки, получени от мастна тъкан, в сравнение с хондроцитни стволови клетки. В модел на дегенеративна дискова болест на плъхове трансплантираните стволови клетки, получени от мастна тъкан, водят до увеличено производство на извънклетъчен матрикс, минимално намалена височина на диска и подобрена дискална хидратация в сравнение с контролите [54].
И накрая, друг обещаващ тип стволови клетки за бъдещо изследване са стволовите клетки, получени от костен мозък. Инвитро проучвания показват, че тези клетки имат сходен хондрогенен капацитет в сравнение с клетките, получени от ядро-пулпоз [55]. въпреки това, in vivo необходими са проучвания, за да се потвърди тяхната потенциална ефикасност и всяка стратегия, включваща въвеждането на нови клетки в човешкия междупрешленни дискове за индуциране на регенерация, би трябвало да отчете повишеното търсене на хранителни запаси от нарастващия брой клетки или повишената активност на наличните преди клетки [56].
5.3. Генна терапия при дегенерация на лумбалния диск
Трансдукцията на гени, които имат потенциал да възпрепятстват дегенерацията на диска или дори да индуцират регенерация на дискове, е концепция, приложена наскоро към DDD от изследователите. Тази стратегия изисква идентифициране на съответните гени, които играят роля в каскадата на дискова дегенерация, както и начини за доставяне на тези потенциално терапевтични гени в дисковите клетки. Това може да бъде получено чрез така наречените системи с генни вектори, които включват разнообразни вирусни и напоследък невирусни вектори [57]. Проблемите с безопасността са неизбежни за използването на вектори и липсата на неблагоприятни ефекти е наложителна за всяка векторна система.
Ранните проучвания използват вирусни вектори за доставяне на маркери гени в дисковете инвитро и in vivo [51, 58]. Първият ген с потенциално благоприятни ефекти върху дегенерацията на диска, който е експериментално доставен на IVD в животински модел, е TGF-β1 [59]. Подобен подход при първоначалната трансдукция на маркерния ген е предприет от Moon et al. за доставяне на гени в човешки IVD клетки [60].
Освен това, други растежни фактори [61], инхибитори на металопротеинази [62], както и транскрипционен фактор, Sox-9 [63], са разгледани като възможни цели за генна терапия за DDD. След идентифициране на ADAMTS5 като допринасящ за разграждането на хрущяла в модел на мишка [64], ADAMTS5 малка интерференционна РНК беше успешно използвана в заешки модел за потискане на разграждането на NP тъкан [65]. Подобен подход беше използван за насочване на каспаза 3, основен изпълнител на апоптоза, в заешки модел [66]. Бъдеще in vivo желателни са проучвания, свързващи теоретичните ползи от който и да е от тези подходи за генна терапия с ситуации, които евентуално се срещат в клиничната практика [67] и включват дългосрочната перспектива на прилагане на генната терапия като стратегия за лечение на основния механизъм на дегенерация на диска.
5.4. Обобщение
Дегенеративното заболяване на лумбалния диск и произтичащите от това болки в кръста придават голямо социално-икономическо въздействие върху здравната система. Дегенерацията на диска е многофакторно събитие със силен генетичен компонент. Възрастта и факторите на околната среда допринасят за дегенеративния процес. Докато настоящите стратегии имат за цел да премахнат генератора на болка чрез операция, бъдещите, възникващи модалности имат за цел да обърнат дегенеративната каскада чрез използване на биологични препарати и генна модификация. Напредъкът в области като геномика, нанотехнологии, биология на стволови клетки, генна терапия и тъканно инженерство има огромен терапевтичен потенциал за клинични приложения при дегенеративни разстройства като DDD, но новите стратегии за лечение на дегенерация на лумбалния диск изискват допълнителна оценка в предклинични и клинични изпитвания.
Препратки
- Подобряване на основните умения за диагностика на болест, подобна на целиакия, доклад за случая BMC Гастроентерология Пълен текст
- Диети с високо съдържание на фибри и анална жлеза при кучета - симптоми, причини, диагностика, лечение, възстановяване
- Бъбречна (бъбречна) дисплазия и симптоми на кистозна болест, диагностика и лечение - Урологични грижи
- Управление на пациенти с целиакия - Канадска асоциация по целиакия
- JVP и консултиране - Обобщено въведение в сърдечно-съдовата система за управление на заболявания; Мускулно-скелетен;