Марио Крац
1 Фред Хътчинсън Център за изследване на рака, Отдел за науките за общественото здраве, Програма за превенция на рака, Сиатъл, Вашингтон
2 Университет във Вашингтон, Катедра по медицина, Отдел по метаболизъм, ендокринология и хранене, Сиатъл, Вашингтон
Дейвид С. Уайгъл
2 Университет във Вашингтон, Катедра по медицина, Катедра по метаболизъм, ендокринология и хранене, Сиатъл, Вашингтон
Патриша А. Брийн
2 Университет във Вашингтон, Катедра по медицина, Катедра по метаболизъм, ендокринология и хранене, Сиатъл, Вашингтон
Kaatje E. Meeuws
3 Университет за здраве и наука в Орегон, Център за изследване на регулирането на теглото, Отдел по ендокринология, диабет и клинично хранене, Портланд, OR
Верна Р. Тежест
3 Университет за здраве и наука в Орегон, Център за изследване на регулирането на теглото, Отдел по ендокринология, диабет и клинично хранене, Портланд, OR
Холи С. Калахан
4 Университетски център за клинични изследвания във Вашингтон, Сиатъл, Вашингтон
Колийн С. Матис
4 Център за клинични изследвания на Университета във Вашингтон, Сиатъл, Вашингтон
Джонатан К. Пърнел
3 Университет за здраве и наука в Орегон, Център за изследване на регулирането на теглото, Отдел по ендокринология, диабет и клинично хранене, Портланд, OR
Резюме
Въздействието на диетите с ниско съдържание на мазнини върху плазмения профил на липопротеините не е напълно изяснено. Проведохме две 16-седмични диетични проучвания, за да сравним ефектите на диета с умерено съдържание на мазнини (mod-FAT) с изокалорични и диети с ниско съдържание на мазнини, богати или на въглехидрати (високо съдържание на CHO, n = 16) или на протеини (високо съдържание на PRO, n = 19) върху плазмени липиди, активност след хепарин липаза, протеин за пренос на холестерилов естер (CETP) и фосфолипиден протеин за пренос (PLTP). Преминаването от mod-FAT към изокалоричната диета с високо съдържание на CHO понижава плазмените концентрации на HDL-холестерол (p Ключови думи: Мазнини, въглехидрати, протеини, липопротеини, липиди, сърдечно-съдови заболявания
Въведение
Повишените плазмени концентрации на LDL-холестерол и триглицериди и ниските плазмени концентрации на HDL-холестерол, самостоятелно или в комбинация, са установени рискови фактори за коронарна болест на сърцето (ИБС) (1-3). Повишените плазмени триглицериди и ниските концентрации на HDL-холестерол често са свързани с преобладаване на по-малките, по-плътни LDL частици, за които напоследък е доказано, че също влияят на риска от ИБС (4). Сред HDL-частиците има данни, които предполагат, че ниските концентрации на HDL2 и повишените концентрации на HDL3 допринасят за риска от ИБС (5). Повишените плазмени активности на протеини, които променят състава на LDL и HDL, включително протеин за пренос на холестерилов естер (CETP) и протеин за пренос на фосфолипиди (PLTP), също са свързани с атеросклерозата (6, 7).
Много от тези свързани с липидите рискови фактори за ИБС могат да бъдат модифицирани чрез промени в телесното тегло и състава на диетата. Повишеното телесно тегло и особено коремното затлъстяване са свързани с повишени плазмени концентрации на триглицериди, нисък HDL-холестерол и по-малки, по-плътни LDL частици (8). Ниските концентрации на HDL-холестерол може да се дължат отчасти на повишената плазмена активност на CETP, която е описана при затлъстели пациенти (8). След загуба на тегло, плазмените активности както на CETP, така и на PLTP намаляват, придружени от намалени концентрации на триглицериди и увеличаване на HDL-холестерола и LDL размера на частиците (8-10). При стабилно телесно тегло заместването на хранителните мазнини с въглехидрати увеличава плазмените концентрации на триглицериди, понижава плазмените концентрации на HDL-холестерол и намалява размера на LDL частиците (11-13). Изокалоричното хранене обаче не отразява условията на свободен живот, при които заместването на въглехидратите с мазнини води до спонтанно намаляване на приема на храна и умерена загуба на тегло (14). В резултат на тази спонтанна загуба на тегло, някои от неблагоприятните последици от богата на въглехидрати диета върху липидните концентрации могат да бъдат смекчени.
Малко проучвания са изследвали ефектите от заместването на хранителните мазнини с протеини върху плазмените концентрации на липиди (11) и дейностите на протеините, участващи в обработката на липопротеини. Много изследвания не успяват да контролират източника на хранителни протеини (11) или разликите в състава на мазнините и въглехидратите (15, 16). В допълнение, предишни проучвания, заместващи диетичните мазнини с протеини, често не успяват да контролират засилената ситост и загуба на тегло, което се случва по време на хранене ad libitum.
Наскоро завършихме две диетични проучвания, сравняващи ефектите от диетичното ограничаване на мазнините и увеличаването на диетичните въглехидрати или протеини върху хормоните, участващи в регулирането на теглото и спонтанната загуба на тегло по време на хранене ad libitum (17, 18). Като част от тези проучвания, ние също измерихме свързаните с липидите рискови фактори за ИБС, с акцент върху липопротеиновите субфракции и плазмените активности на протеините, участващи в разпределението на липопротеиновите частици. Тези проучвания ни позволиха да определим количествено ефектите от промените в хранителните макронутриенти върху резултатите от липидите при изокалорични условия, когато промяната на теглото не е объркващо, както и потенциалните комбинирани ефекти от промените в диетата и загубата на тегло при условия ad libitum.
Материали и методи
Проучвайте популация
Две диетични проучвания бяха проведени съвместно в Университета на Вашингтон (UW) в Сиатъл, Вашингтон, и Орегонския университет за здраве и наука (OHSU) в Портланд, Орегон. За проучване А (пълно описание по-долу) бяха наети 18 здрави възрастни (2 мъже, 16 жени) със средна (обхват) възраст 45 (28-63) години и индекс на телесна маса 27,1 (24,5-30,2) kg/m 2 чрез реклама във вестници в техния местен район. От тях двама субекти бяха изключени от анализи поради неспазване на диетичния режим ad libitum (17, 18). За проучване Б (вж. Също по-долу), отделна група от 19 здрави възрастни (3 мъже, 16 жени) със средна (обхват) възраст 41 (27-62) години и индекс на телесна маса 26,2 (22,5-30,1) kg/m 2 също бяха наети чрез реклама във вестници (17, 18). Преди да бъдат записани, субектите са предоставили информирано писмено съгласие. Всички процедури бяха одобрени от институционалните съвети за преглед на UW и OHSU.
Проучване на дизайн и диети
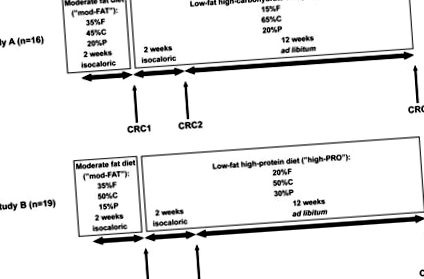
Дизайн на двете проучвания. И в двете проучвания субектите са консумирали умерена мастна диета ("mod-FAT") през първите две седмици. През това време приемът на калории се коригира, за да се поддържа телесното тегло в рамките на 1 kg от изходното ниво. На 14-ия ден от този период участниците са дошли в Центъра за клинични изследвания (CRC) за вземане на кръв. След освобождаване от CRC1, субектите преминаха към диета, богата на въглехидрати („високо-СНО”) в проучване А, и към диета, богата на протеини („висока-ПРО”) в проучване Б. През първите две седмици на тези диети, приемът на калории се поддържа на нивото, което е довело до стабилност на теглото в предишната фаза. Тази изокалорична фаза отново беше последвана от посещение на CRC на 28-ия ден от изследването. През последните 12 седмици от проучванията субектите продължиха да консумират тези диети; сега обаче те получиха повече храна и избраха прием на калории свободно (ad libitum). Субектите завършиха проучването с третото си посещение в CRC на ден 112. F = мазнини, C = въглехидрати, P = протеин.
Диетичният състав, изразен като% от енергийния прием, за първите две седмици от двете проучвания е 30-35% мазнини, 45-50% въглехидрати и 15-20% протеин с обща калория, коригирана, за да поддържа теглото на пациентите стабилно (mod- FAT диета). В проучване А субектите консумират 20% по-малко мазнини и 20% повече въглехидрати (диета с високо съдържание на СНО) по време на втората изокалорична фаза и фазата ad libitum в сравнение с базовия период. Тази диета с високо съдържание на СНО съдържа повече фибри (3,3 срещу 2,2 g/MJ) и по-малко холестерол (17 срещу 27 mg/MJ) от диетата на изходното ниво. В проучване Б субектите консумират 15% по-малко мазнини и 15% повече протеини (диета с високо PRO) по време на втората изокалорична фаза и фазата ad libitum в сравнение с базовия период. Тази диета с високо съдържание на PRO съдържа малко по-малко фибри (2,4 срещу 2,8 g/MJ) и малко повече холестерол (22 срещу 18 mg/MJ) от диетата на изходното ниво.
Всички ястия бяха приготвени в Nutrition Research Kitchens на CRC на UW и OHSU. Всички диети са количествено определени с помощта на софтуера ProNutra и ProNessy (версия 3.0, Viocare Technologies Inc., Princeton, NJ). След приключване на всяка диетична фаза [базовата диета (CRC1), изокалоричната диета с ниско съдържание на мазнини (CRC2) и диетата ad libitum (CRC3)], субектите бяха приети в CRC в съответните си институции, за да преминат тестване, както е описано По-долу.
Лабораторни методи
Липиди и липопротеини
След 12-16-часово бързо гладуване през нощта и след период на почивка от поне 15 минути след интравенозно поставяне, изходната кръв се събира в 0,1% EDTA за липидни изследвания. След това се дава хепаринов болус от 60 U/kg и кръвта се събира след десет минути в литиево-хепаринови епруветки за измерване на липазната активност. Кръвта веднага се центрофугира при 4 ° С при 3000 об/мин за 15 минути. След това аликвотни части от плазмата се замразяват бързо и се съхраняват при -70 ° С. Общият холестерол, триглицеридите, HDL-холестерола, съдържанието на холестерол във фракциите на липопротеините и пиковата плаваемост на LDL частиците, HDL2-холестеролът, HDL3-холестеролът и аполипопротеин В са измерени в Северозападната липидна изследователска лаборатория, както е описано по-рано (22, 23).
Дейности след хепарин липаза
Общата липолитична активност е измерена в плазмата след хепаринов болус, както е описано по-рано (24). Активността на липопротеин липазата (LPL) се изчислява като липолитичната активност, отстранена от плазмата чрез инкубация със специфично моноклонално антитяло срещу LPL, а активността на чернодробната липаза (HL) се определя като активност, останала след инкубация с LPL антитяло. Ензимната активност се изразява като наномоли свободна мастна киселина, отделяни за минута на милилитър плазма при 37 ° C. Коефициентите на вариация в интра- и между теста са съответно 6% и 14% за HL и съответно 7% и 8% за LPL.
CETP плазмена концентрация
Концентрациите на CETP в плазмата бяха измерени чрез търговски комплект за имуноанализ ELISA (Wako Chemicals USA, Richmond, VA), използвайки 2 моноклонални антитела. Вътрешно-пробното и междуопитно CV са съответно 3,1% и 10,5%. Както беше съобщено по-рано, CETP масата, измерена чрез този ELISA анализ, корелира силно (r = 0.83, n = 42) с CETP активността (25).
PLTP анализ на активността
PLTP активността се определя чрез измерване на трансфера на белязан фосфатидилхолин от везикули към HDL3 (26, 27), без използването на плазма като носител, както е описано по-рано (26). Този метод отразява фосфолипидната трансферна активност на PLTP, но не и тази на CETP. Три човешки контролни плазми бяха включени в три екземпляра във всеки анализ и използвани за коригиране на вариацията между теста. Интра- и междупробната CV са съответно 8% и 2%.
Концентрации на холестерол във липопротеинови фракции
Разпределението на плътността на липопротеините и съдържанието на холестерол се определят чрез ултрацентрифугиране с градиент на неравновесна плътност, като се използва модификация на предварително описана техника и вертикален ротор Sorvall TV-865B (DuPont, Wilmington, DE) (28). HDL се намира във фракции 0-6, LDL във фракции 7 до 18, IDL във фракции 19-30 и VLDL във фракции 30-38. Относителната флотация на LDL (LDL Rf), мярка за пикова плаваемост на LDL, се определя чрез разделяне на броя на фракциите между 7 и 19, съдържащ пиковата концентрация на LDL холестерол, на общия брой събрани фракции (равен на 38). Тази техника е оптимизирана за отделяне на субфракции на частици, съдържащи аполипопротеин В, а не по-плътните видове HDL. LDL фракциите също се събират, за да се определи съдържанието на холестерол и аполипопротеин В.
- Ефект на съотношението на протеините, липидите и въглехидратите с храната върху растежа, ефективността на храненето и тялото
- Пълна статия Асоциация на ИТМ и инсулин на гладно с рискови фактори за сърдечно-съдови заболявания в
- Ефект от консумацията на прясна диня върху рисковите фактори за сърдечно-съдови заболявания при наднормено тегло и
- Сравнение на 3 диети ad libitum за поддържане на загуба на тегло, риск от сърдечно-съдови заболявания и
- Качество на диетата и каротидна атеросклероза при лица с междинен сърдечно-съдов риск Хранене