Резюме
Заден план
Ефектите на алфа-линоленова киселина (ALA) върху сърдечно-съдовите рискови фактори варират значително в публикуваните доклади. Следователно, ние изследвахме ефектите от 12-седмично добавяне с ленено масло (FO), което е богат източник на ALA, върху сърдечно-съдови рискови фактори като серумни малки плътни концентрации на липопротеини с ниска плътност (sd-LDL).
Методи
В рандомизирано, двойно сляпо, кръстосано проучване, 15 субекта са приели 10 g FO или царевично масло (CO), съдържащи съответно 5,49 g и 0,09 g ALA, веднъж дневно по време на вечеря. Кръвни проби бяха събрани на 0, 4 и 12 седмици и бяха използвани за анализ на серумни липиди, свързани с липидите протеини, серумни мастни киселини и серумен sd-LDL холестерол. Различията по време на тестовия период бяха идентифицирани с помощта на дисперсионен анализ с повтарящи се мерки (ANOVA) за вътрешногрупови ефекти. Груповите разлики бяха идентифицирани с помощта на сдвоен t-тест във всеки момент от вземане на кръв.
Резултати
Концентрациите на ALA и ейкозапентаенова киселина са значително по-високи през периода на FO на 4 и 12 седмици, отколкото в периода на CO. Не са наблюдавани значителни разлики в концентрациите на докозахексаенова киселина между два периода и концентрациите на протеин за пренос на холестерилов естер и концентрациите на аполипопротеин В са значително по-ниски в периода на FO, отколкото в периода на CO след 12 седмици. Добавянето на FO е свързано със значително намаляване на концентрациите на sd-LDL на 4 и 12 седмици и добавянето на CO няма ефект. Освен това, концентрациите на sd-LDL са били значително по-ниски през периода на FO, отколкото в периода на CO след 4 седмици. Сред субектите с концентрации на триглицериди (TG)> 100 mg/dl, добавянето на FO значително намалява концентрациите на sd-LDL на 4 и 12 седмици в сравнение с изходното ниво. Концентрациите на Sd-LDL значително се различават между периодите както на 4, така и на 12 седмици.
Заключение
Това проучване показва, че FO, който е богат източник на ALA, води до по-ниски концентрации на sd-LDL холестерол.
Заден план
Метаболитният синдром е група от взаимосвързани аномалии на плазмените липиди и липопротеини, включително намален холестерол на липопротеини с висока плътност (HDL), преобладаване на малки плътни частици липопротеини с ниска плътност (sd-LDL) и повишена концентрация на триглицериди (TG) [ 1]. Тези дислипидемични характеристики са свързани с повишен риск от сърдечно-съдови заболявания (ССЗ) [2].
Подкласовете LDL се характеризират с вариации в плътността, размера и химичния състав и са от клинично значение [3]. Sd-LDL е рисков фактор за развитието на коронарна артериална болест при западняците [4,5] и японците с относително ниски концентрации на LDL холестерол [6,7]. В скорошно проучване sd-LDL холестеролът е значително свързан с развитието на ССЗ в японска популация [8], което показва значението на sd-LDL холестерола като биомаркер за предсказване на ССЗ.
Следователно целта на това проучване е да изясни ефектите на 12-седмичното добавяне с ленено масло (FO), което е богат източник на ALA, върху сърдечно-съдовите рискови фактори, включително sd-LDL холестерол.
Методи
Субекти
Бяха проверени 26 възрастни мъже със здравословен и социален начин на живот. Потенциалните участници бяха проверени чрез медицинска история, физически преглед, лабораторен анализ и дневен прием на риба. Субекти с данни за инфекции, захарен диабет, бъбречно, чернодробно или възпалително заболяване бяха изключени. Субектите, които редовно консумираха FO или масло от перила, също бяха изключени. Сред двадесет и един записани мъже, 1 се оттегли преди завършване на проучването поради лекарства и 5 субекта бяха изключени поради несъответствие по време на 12-седмичната интервенция. От тези участници 15 пациенти със средна ± стандартна грешка (SE) индекс на телесна маса (ИТМ, kg/m 2) от 25,1 ± 0,5 и средна ± SE възраст от 44,5 ± 3,1 години завършиха проучването. Четирима субекти са били пушачи, а петима са получавали антихипертензивни лекарства. Характеристиките на субекта и лабораторните данни са представени в таблица 1. Според концентрациите на TG, 15 субекта са разделени на две групи: групата на TG 100 mg/dl (n = 10).
Информирано съгласие беше получено от всички участници преди началото на проучването, което беше одобрено от етичния комитет на университетската болница в Токушима, Токушима, Япония. Изследването е проведено в съответствие с Хелзинкската декларация.
Уча дизайн
В рандомизирано, двойно сляпо, кръстосано проучване, субектите са получавали или FO, или царевично масло (CO) по време на два последователни 12-седмични периода на добавки. Периодите на добавяне бяха разделени от 8-седмичен период на измиване. Субектите са инструктирани да приемат 10 g FO или CO с помощта на предоставената лъжица веднъж дневно с вечеря. Добавките от 10 g FO и CO съдържат съответно 5,49 и 0,09 g ALA. Съставите на мастните киселини на двете масла са представени в Таблица 2. Съставът на мастните киселини на двете масла е измерен чрез газово-течна хроматография. За да се избегне окисляването, те са били инструктирани да поставят бутилки с масло в кутия за блокиране на светлината и да ги съхраняват в хладилника.
Субектите са инструктирани да поддържат обичайната си диета през цялото проучване, за да се изключат влиянията на хранителните хранителни вещества и са били помолени да продължат с нормалните си ежедневни дейности. Субектите също бяха инструктирани да избягват приема на противовъзпалителни лекарства, витамини или други хранителни добавки през целия интервенционен период.
Субектите записвали ежедневните си дейности и приема на храна в дневник и тези записи в начина на живот се потвърждавали по време на интервюта на всеки 2 седмици. Субектите върнаха бутилки с отработено масло и бяха снабдени с хранителни добавки за следващите 2 седмици. Останалите обеми във върнатите бутилки бяха измерени, за да се оцени съответствието. Всички субекти консумират повече от 97% от определеното количество масло.
Субектите са били посещавани в 0 (период на въвеждане), 4 и 12 седмици, за да се вземат кръвни проби на гладно, телесно тегло и измерване на кръвното налягане и да се предадат предишните им 3-дневни диетични записи. Субектите са инструктирани да ядат и пият същите предписани храни в 20.00 часа преди планираните посещения. Кръвни проби на гладно се събират в 08.00 часа след гладуване през нощта и се използват за анализ на серумни липиди, свързани с липидите протеини, серумни мастни киселини и серумен sd-LDL холестерол. Диетолог изчислява средния енергиен прием от диетичните записи на всеки субект за 3-те дни, предхождащи планираните посещения. Тези диетични записи са анализирани с помощта на компютъризиран софтуер (Excel Eiyou-kun версия 4.0, Kenpaku-sha, Токио, Япония), за да се определи приема на калории и съдържанието на макроелементи.
Аналитични методи
Статистически анализ
Данните са представени като средната стойност ± SE. Изходни физически характеристики и лабораторни данни между групата на TG> 100 mg/dl и TG
Резултати
Прием на храна и хранителни вещества
Диетичният прием в периоди на CO и FO е показан в Таблица 3. На 0 седмица не са наблюдавани значителни разлики в общата енергия, протеини, въглехидрати, мазнини, диетични фибри или алкохол между периодите.
В периода на FO общият прием на ALA е значително по-висок на 4 и 12 седмици, отколкото на 0 седмица. Общият прием на ALA на 4 и 12 седмици е значително по-висок в периода на FO, отколкото в периода на CO. В периода на CO общият прием на линолова киселина (LA) е значително по-висок на 4 и 12 седмици, отколкото на 0 седмица. Общият прием на LA през 12 седмици е значително по-нисък в периода на FO, отколкото в периода на CO.
В периода на FO съотношенията n-6/n-3 бяха значително по-ниски на 4 и 12 седмици, отколкото на 0 седмица. В периода на CO съотношенията n-6/n-3 са били значително по-високи на 4 и 12 седмици, отколкото на 0 седмица. Съотношенията на n-6/n-3 на 4 и 12 седмици са значително по-ниски в периода на FO, отколкото в периода на CO.
Приемът на алфа-токоферол на 12 седмици е значително по-нисък в периода на FO, отколкото в периода на CO.
Антропометрични и лабораторни данни
Антропометрични и лабораторни параметри от субекти на периоди на CO и FO са показани в Таблица 4. Не са наблюдавани значителни разлики в телесното тегло на 0 седмица и не са наблюдавани значителни разлики в концентрациите на алфа-токоферол между двата периода в края на проучването.
Промени в серумните липиди и свързаните с липидите протеини в периодите на CO и FO са показани в Таблица 5. Не са наблюдавани значителни разлики в липидите и свързаните с липидите протеини на 0 седмица. В периода на FO концентрациите на CETP са били значително по-ниски на 12 седмици, отколкото на 0 седмица и са били значително по-ниски, отколкото в периода на CO на 12 седмици. Концентрациите на общия холестерол, LDL-, HDL-, не-HDL-холестерол, аполипопротеин (Apo) A-1 и Apo B са значително по-ниски в периода на FO, отколкото в периода на CO след 12 седмици. Концентрациите на TG, RLP-холестерол, апо С-3, апо Е и апо В48 не се променят значително по време на CO и FO периодите.
Нежелани събития като главоболие, умора, диария и пълнота на стомаха са наблюдавани и през двата периода, но не са свързани с тестовата диета. Освен това по време на запитвания за симптоми или по време на прегледи не са забелязани симптоми или странични ефекти от тестовите диети.
Промени в серумните концентрации на мастни киселини
Промени в концентрациите на серумни мастни киселини в периодите на CO и FO са показани в таблица 6. С изключение на докозатетраеновата киселина, не са установени значителни разлики в състава на серумните мастни киселини между двата периода на 0 седмица. На 4 седмици концентрациите на LA са значително увеличени през периода на CO в сравнение с 0 седмица. Докато през периода на FO концентрациите на LA на 4 и 12 седмици са били значително по-ниски, отколкото в периода на CO. Концентрациите на арахидонова киселина са значително намалени на 12 седмици и през двата периода и са значително по-ниски в периода на FO, отколкото в периода на CO на 4 седмици.
Концентрациите на ALA значително намаляват на 12 седмици в периода на CO, но се увеличават на 4 и 12 седмици в периода на FO в сравнение с 0 седмици и са значително по-високи в сравнение с периода на CO в тези часови точки.
На 4 и 12 седмици концентрациите на EPA са значително по-високи в периода на FO, отколкото в периода на CO. Не са установени обаче значителни разлики в концентрациите на докозапентаенова киселина или DHA между периодите и концентрациите на DHA значително намаляват между 0 седмица и 12 седмици и през двата периода. Съотношенията на n-6/n-3 значително се увеличават в периода на CO на 12 седмици, но значително намаляват в периода на FO на 4 и 12 седмици в сравнение с 0 седмица. Освен това съотношенията n-6/n-3 значително се различават между периодите на 4 и 12 седмици.
Серумни концентрации на sd-LDL
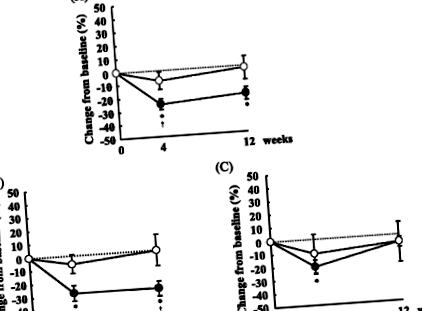
На 0 седмица, серумните концентрации на sd-LDL не се различават значително между двата периода (данните не са показани). Промени в серумните концентрации на sd-LDL от 0 седмица са показани на фигура 1. Добавянето на FO е свързано с 25,8% и 21,2% намаление на концентрациите на sd-LDL на 4 и 12 седмици, съответно, въпреки че добавянето на CO не влияе на концентрациите на sd-LDL (Фигура 1А). На 4 седмици концентрациите на sd-LDL бяха значително по-ниски в периода на FO, отколкото в периода на CO.
Предишен доклад показа, че размерът на LDL частиците се влияе от концентрациите на TG [4]. За да изясним ефекта на изходните концентрации на TG, ние разделихме пациентите на две групи според концентрациите на TG. С изключение на концентрациите на TG, няма значителни разлики между групата на TG> 100 mg/dl и TG 100 mg/dl, добавянето на FO води до 28,2% и 28,9% намаления в концентрациите на sd-LDL на 4 и 12 седмици в сравнение с 0 седмица, съответно, и концентрациите на sd-LDL значително се различават между периодите както на 4, така и на 12 седмици (Фигура 1В). Въпреки това, сред субектите с концентрация на TG от
Дискусия
В настоящото проучване показахме, че добавките с FO значително намаляват серумните концентрации на sd-LDL, особено при пациенти с концентрация на TG> 100 mg/dl. Също така демонстрирахме, че общия серумен холестерол, LDL-холестерол, HDL-холестерол, CETP, Apo A-1 и Apo B концентрациите са значително по-ниски в периода на FO, отколкото в периода на CO след 12 седмици.
FO, използван в това проучване, е богат източник на ALA и предишни мета-анализи показват, че консумацията на ALA може да предостави сърдечно-съдови ползи, с 10% намаляване на риска от смъртност от ИБС за всеки 1 g/d увеличение на ALA [14]. Освен това наскоро публикуван преглед показа настоящите доказателства за връзка между ALA и диабет тип 2 и риск от фрактури, в допълнение към резултатите от ССЗ [15].
Предишно проучване показа, че не HDL-холестеролът (LDL + IDL + VLDL холестерол) е по-мощен предиктор за ССЗ [24]. В това проучване, не HDL-холестеролът е значително по-нисък в периода на FO, отколкото в периода на CO след 12 седмици. Следователно, това показва, че добавката с FO може да допринесе за подобряване на липидния профил. От друга страна, концентрациите на HDL-холестерол също са значително по-ниски в периода на FO, отколкото в периода на CO в това проучване. Други проучвания също показват, че концентрациите на HDL-холестерол са по-ниски в групата ALA, отколкото в групата LA [25,26]. В друго проучване не са установени значителни разлики в концентрациите на HDL-холестерол в сравнение с групата ALA и групата LA [27]. Следователно ефектът на ALA върху концентрациите на HDL-холестерол не е последователен.
Това проучване показа, че добавките с FO значително намаляват серумните концентрации на sd-LDL, особено при лица с концентрация на TG> 100 mg/dl. В заключение, това проучване показва, че FO, който е богат източник на ALA, води до по-ниски концентрации на sd-LDL холестерол.
- КЛИНИЧНИ РЪКОВОДСТВА, ЧАСТ 1 Насоки за използване на серумен холестерол, липопротеин с висока плътност
- Оценка на приема на кофеин при възрастни японци, използващи 16 d претеглени диетични записи, базирани на храна
- Ефекти на диетите с ограничени въглехидрати върху нивата на липопротеините с ниска плътност в
- Всичко, което трябва да знаете, ако имате малък мускул на пениса; Фитнес
- Ранното следоперативно ниво на серумен албумин предсказва оцеляване след лечебна нефректомия за бъбреците