P. R. Shewry
1 Rothamsted Research, Хартфордшир, Великобритания
2 University of Reading, Berkshire, UK
S. J. Хей
1 Rothamsted Research, Хартфордшир, Великобритания
Резюме
Заден план
През последните няколко години се забелязват нарастващи опасения, особено в медиите и непрофесионалната преса, относно въздействието на храните, базирани на пшеница, върху здравето, с нарастващото приемане на диети без пшеница или без глутен. Тези опасения се разпространяват до голяма степен чрез медиите, особено популярната преса, Интернет и социалните медии, а не чрез конвенционалните медицински и обществени канали, а доказателствената база често е неясна. Независимо от това, въздействието е драматично и предизвиква загриженост не само за производителите на пшеница и хранителната промишленост, но и за общественото здраве поради въздействието върху приема на компоненти, които обикновено се консумират в продуктите от пшеница, като диетични фибри, витамини от група В и минерали (Steer et al. 2008).
Притесненията могат да бъдат разделени най-общо на два вида: че продуктите от пшеница са непропорционално отговорни за увеличаване на затлъстяването и диабет тип 2 и че протеините от пшеничен глутен причиняват редица нежелани реакции, включително алергии, цьолиакия и редица по-слабо дефинирани състояния . Ролята на продуктите от пшеница за нарастващите нива на затлъстяване и свързаните с тях състояния бе популяризирана от най-продаваната книга „Пшеничен корем: загуби пшеницата, отслабни и намери пътя си обратно към здравето“ (Davis 2011), което доведе до разпространение на публикации за диети и рецепти без пшеница. Научните недостатъци в аргументите са били обсъждани в научната литература (Jones 2012; Brouns et al. 2013), но тези научни публикации са имали малък или никакъв ефект върху общественото схващане, че пшеницата е вредна за вас!
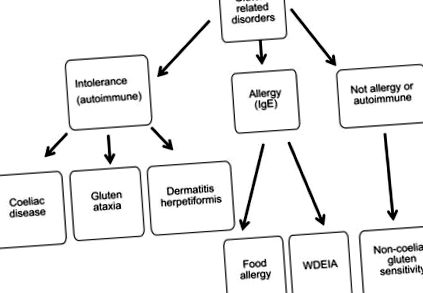
Следователно ние се фокусираме тук върху втората тема, като разглеждаме доказателствата за увеличаване на нежеланите реакции към консумацията на пшеничен глутен (и евентуално и други пшенични компоненти). Спектърът от условия е обобщен на Фигура 1, която се основава на резултатите от международна експертна група, която се срещна през 2011 г. (Sapone et al. 2012). Трябва обаче да се има предвид, че това е опростяване и някои състояния могат да възникнат заедно при едни и същи пациенти. И накрая, важно е да се отбележи, че методите за диагностика са се подобрили значително през последните няколко десетилетия, заедно с повишената осведоменост относно състоянията, свързани с храните, сред клиницистите и потребителите. Следователно е важно да се прецени дали тези промени са повлияли на нашите оценки на разпространението.
Предлага се номенклатура и класификация на нарушенията, свързани с глутена в храната. Променено от Sapone et al. (2012). Зависима от пшеница анафилаксия, предизвикана от упражнения (WDEIA).
Алергия към пшеница
Алергиите са свръхчувствителни реакции към чужди компоненти, най-често протеини, и обикновено са свързани с производството на специфичен клас антитела, наречени IgE (за разлика от IgG антителата, които се произвеждат в отговор на най-нахлуващите патогени). Симптомите на алергия към погълнатите пшенични продукти включват атопичен дерматит, уртикария (наричана още копривна треска или обрив от коприва) и дихателни и стомашно-чревни симптоми. Включени са редица протеини, по-специално инхибитори на а-амилаза и глутенови (глиадин и глутенин) протеини (прегледани от Tatham & Shewry 2008; Matsuo et al. 2015).
Зависима от пшеница анафилаксия, предизвикана от упражнения (WDEIA)
Най-добре характеризираната форма на пшенична алергия е зависимата от пшеница анафилаксия, предизвикана от упражнения (WDEIA). Това е вид алергичен отговор, който се предизвиква от поглъщането на храна, последвано от физически упражнения, като пшеница и ракообразни са най-честите причини (Beaudouin et al. 2006). WDEIA е проучен най-подробно от японски работници, които разпознават две форми (Yokooji et al. 2015). Конвенционалната (CO) WDEIA е доминиращата форма и се счита за сенсибилизирана чрез стомашно-чревния тракт, като основният алерген е ω ‐ 5 глиадин (Palosuo et al. 2001; Morita et al. 2003). В Япония обаче е дефинирана и втора форма, която изглежда е сенсибилизирана чрез кожата и/или лигавицата от хидролизиран пшеничен протеин (HWP), присъстващ в сапуна. Основният сенсибилизиращ агент в HWP-WDEIA изглежда е γ-глиадин и реакции могат да възникнат след излагане на сапун или консумация на пшеница (Yokooji et al. 2013).
Преобладаването на зависимата от храната анафилаксия, предизвикана от физическо натоварване (включително WDEIA), е съобщено като 0,017% при японски деца (Aihara et al. 2001), докато при скрининг на 935 възрастни японци за алергия към пшеница (включително и WDEIA) с помощта на въпросници, убождане на кожата тестове и определяне на ω ‐ 5 специфичен за глиадин IgE идентифицира само двама алергични субекти (0,21%) (Morita et al. 2012).
Целиакия
Целиакия (CD) е автоимунно състояние, което засяга тънките черва, което води до малабсорбция, загуба на тегло, умора, коремна болка, повръщане и диария. Следователно, пациентите с CD страдат от недостиг на хранителни вещества, включително желязна анемия и дефицит на фолиева киселина. Въпреки това, индивидите могат да бъдат асимптоматични или да проявяват само леки симптоми.
Ролята на протеините от пшеничен глутен в задействането на CD е добре установена, като глиадинът и глутениновите протеини са основната причина (прегледано от Gilissen et al. 2014). В момента 31 кратки пептидни последователности в протеините от пшеничен глутен и свързаните с тях протеини в ечемика и ръжта са определени като токсични за целиакия: те често се наричат „епитопи“ на целиакия. Картографирането обаче е непълно и броят на отделните епитопи е въпрос на текуща дискусия (Sollid et al. 2012).
Въпреки че в миналото CD се счита за педиатрично заболяване, сега се признава, че може да се появи на всяка възраст, а мащабният скрининг разкри значително ниво на недиагностициран CD при възрастни. Например, проучване на 7550 участници, проведено в Кеймбридж (Великобритания), показва, че 1,2% от възрастните на възраст 45–76 години са серологично положителни (West et al. 2003). Аналогично, анализ на 16 847 възрастни на възраст 50 години или повече в Минесота показва 0,8% недиагностициран CD (Godfrey et al. 2010). Следователно разпространението на CD в Европа и страните с висок дял на популациите от европейски произход (напр. САЩ, Австралия) сега се оценява широко на около 1% от населението, въпреки че се наблюдават значителни различия между страните от едва 0,2% до над 5%. В рамките на Европа Финландия има особено висока честота, отчетена като 1–2,4% (Maki et al. 2003; Godfrey et al. 2010; Mustalahti et al. 2010; Walker et al. 2010; Rubio ‐ Tapia et al. 2012).
Съществува схващането, че разпространението на CD се увеличава, въпреки че това може да е резултат, поне отчасти, на повишената информираност и подобрена диагноза (с скрининг за наличие на антитела към ензимната тъканна трансглутаминаза в серума, който се използва за първоначално диагноза) (Ludvigsson et al. 2015). Повишеното разпространение в Швеция се дължи на промените в храненето на бебета (Olsson et al. 2008; Myléus et al. 2009), докато Lohi et al. (2007) съобщават за двукратно увеличение на CD при финландски възрастни между 1978–1980 и 2000–2001 (от 1,05% на 1,99%), след коригиране на данните за подобрена диагноза за същия период.
Green and Cellier (2007) отбелязват, че CD за възрастни е около два пъти по-разпространен при жените, отколкото при мъжете, общо с по-високата честота на други автоимунни заболявания. Те също така отбелязват, че жените са по-склонни да страдат от желязодефицитна анемия и остеопороза, симптоми, които могат да доведат до разследвания от здравни специалисти. Съобщава се също така, че разпространението при жените намалява след около 65-годишна възраст (Green et al. 2001).
Дори когато първоначалният серологичен скрининг е потвърден чрез биопсия на тънките черва, пациентите може да не получат промени в телесното тегло или други симптоми. Независимо от това, асоциирането на CD с повишен риск от редица други заболявания (Corrao et al. 2001; Green et al. 2003; West et al. 2004; Green & Cellier 2007; Solaymani-Dodaran et al. 2007; Godfrey et al 2010) означава, че лечението е необходимо дори при липса на симптоми.
Условия, свързани с цьолиакия
Целиакията може да бъде свързана с неврологични състояния, като периферната невропатия и глутеновата атаксия (GA), при които малкият мозък е увреден, са най-честите. Разпространението им не е установено, но Hadjivassiliou et al. (2002) са изчислили, че неврологична дисфункция може да се появи при около 6–10% от пациентите с гастроинтестинални симптоми. Тези автори прегледаха 35 публикации, в които атаксия и периферна невропатия са налице при 29 от 83 пациенти. Подобни симптоми обаче се наблюдават и при пациенти, определени като страдащи от „чувствителност към глутен“, при липса на диагностициран CD (Hadjivassiliou et al. 2010). Съвсем наскоро Hadjivassiliou et al. (2015) съобщават, че GA има разпространение от 15% сред всички атаксии.
Dermatitis herpetiformis (DH) е форма на CD, която се представя като хронично кожно заболяване. Разпространението му е много по-ниско от типичното CD, изчислено на 0,001– 0,04%, и общо с CD, то е по-високо в популациите от европейски произход и ниско в азиатските и афро-американските популации (Gawkrodger et al. 1984; Mobacken et al. 1984; Smith et al. 1992; Bolotin & Petronic-Rosic 2011). За разлика от CD, разпространението на DH е от 1,5–2 пъти по-високо при мъжете, отколкото при жените (Smith et al. 1992)
Шизофрения и разстройство от аутистичния спектър
Връзките между консумацията на пшеница и мляко и шизофренията и разстройството от аутистичния спектър са проучени с подробности, като и двете състояния са подобрени при някои пациенти чрез интервенции с диети без глутен, без казеин или глутен и без казеин (Singh & Roy 1975; Christison & Ivany 2006; Kalaydiian et al. 2006; Whiteley et al. 2010, 2013).
Предполага се, че невроактивните пептиди, освободени при смилане на пшеничен глутен, са отговорни за неврологичните ефекти (Dohan 1979; Dohan et al. 1984), което е породило концепцията за глутеоморфините. Предлага се това да бъдат опиоидни пептиди, които се освобождават чрез смилане на глутен в стомашно-чревния тракт и се поглъщат в кръвния поток, което води до неврологични ефекти и „пристрастяващи“ свойства. По същия начин се предполага, че казоморфините са отговорни за подобни симптоми, свързани с консумацията на мляко. За тази хипотеза обаче има малко експериментални доказателства.
Чувствителност към глутен без целиакия (NCGS)
През последните години все по-голям брой пациенти съобщават за симптоми, свързани с консумацията на пшеница, които не са класически алергичен или автоимунен отговор. Това доведе до дефиницията на ново състояние, наречено „нецелиакална чувствителност към глутен“ (NCGS) (Sapone et al. 2012). Обхватът на симптомите варира в широки граници, включително стомашно-чревни симптоми, умора, главоболие, дерматит, болки в мускулите и ставите, депресия, тревожност и анемия и не е ясно дали NCGS представлява единичен синдром или редица състояния (Sapone et al. 2012). Следователно той е най-добре дефиниран в отрицателни изрази: като реакция на глутен (или пшеница), когато са изключени както CD, така и алергията (Aziz et al. 2012; Sapone et al. 2012). Освен това ролята на глутена не е ясно установена и симптомите могат да се отнасят до други зърнени компоненти. Следователно терминът „чувствителност към нецелиакична пшеница“ (NCWS) може да е по-подходящ (Carroccio et al. 2014; Catassi et al. 2015).
Патогенезата на NCGS/NCWS не е разбрана, но е вероятно да включва комбинация от фактори, включително стимулиране на вродената имунна система. Тази липса на разбиране представлява предизвикателство за диагнозата, но скорошният доклад на експертна група препоръчва безглутенова диета, последвана от двойно-сляпо, плацебо-контролирано глутеново предизвикателство, с вариация от 30% или повече при един до три основни симптома положителен резултат и в двете фази (Catassi et al. 2015).
Истинското разпространение на NCGS/NCWS няма да бъде ясно, докато тези критерии не бъдат стриктно приложени. Следователно разпространението, съобщено в публикувани по-рано проучвания, вероятно ще бъде по-високо от истинските стойности. Например NCGS е диагностициран при 6% от 5896 пациенти, наблюдавани в Центъра за изследване на целиакия в Мериленд, САЩ (Sapone et al. 2012), докато Volta et al. (2014) идентифицира 3% от 12 000 пациенти със съмнения за NCGS в многосайтово проучване на амбулаторни пациенти в италианските здравни центрове. Проучване сред 1002 възрастни в района на Шефилд в Обединеното кралство идентифицира 13% със самоотчетена чувствителност към глутен (GS), докато по-нататъшно проучване на 200 пациенти с GS показва, че 7% имат CD и 93% NCGS (Aziz et al. 2014). Съотношението на жените към мъжете в последните две проучвания е около 4: 1 (Aziz et al. 2014; Volta et al. 2014).
FODMAP и стомашно-чревни разстройства
По-широко въздействие на безглутеновите диети върху храненето и здравето
Заключения
Докато неблагоприятните реакции към пшеницата биха могли да се считат за добре разбрани само преди десетилетие, пейзажът оттогава е изключително усложнен. Пшеничната алергия остава най-добре разбраното състояние и най-лесно диагностицираното. Разпространението изглежда под 1%, като WDEIA (което може да доведе до анафилаксия) е много по-рядко. Няма доказателства, че разпространението се увеличава непропорционално в сравнение с други хранителни алергии или че разпространението е свързано с видовете пшеница или продукти от пшеница, които се консумират. Настоящото разпространение на CD в Обединеното кралство също вероятно е около 1%, но не е ясно дали увеличенията, наблюдавани в много страни, отразяват истински увеличения на разпространението или са резултат от по-голяма осведоменост и подобрена диагноза.
Други състояния, свързани с пшеничния глутен или други компоненти на пшеничното зърно, са по-слабо разбрани и диагностиката е проблематична. Няма съмнение обаче, че разпространението е много по-ниско от дела на потребителите в Северна Америка и Западна Европа, които предпочитат безглутенови диети, или числата, които се самоотчитат за NCGS, може би от същия ред като алергии и CD. Следователно съгласуването на диагностичните критерии за NCGS е важна стъпка за определяне на истинското разпространение, докато са необходими и контролирани интервенции, за да се определи дали пшеничният глутен, FODMAP или други зърнени компоненти са отговорни.
Следователно е свръхреакция да се предположи, че здравето на повече от малка част от населението ще бъде подобрено чрез елиминиране на пшеница или глутен от диетата. Всъщност може да се случи обратното, тъй като пшеницата е важен източник на протеини, витамини от група В, минерали и биоактивни компоненти.
И накрая, важно е да се отбележи, че пшеницата е основната основна храна в по-голямата част от умерения свят, включително развиващите се страни в Северна Африка и Западна и Централна Азия, където може да допринесе между 50–70% от общия прием на храна и части от Китай и Индия. Той също допринася все повече за диетата в Африка на юг от Сахара. Въпреки че данните са ограничени, има малко доказателства, че тези страни изпитват нарастване на неблагоприятните реакции към консумацията на пшеница, а намаленото производство на пшеница поради опасения, произтичащи от проспериращите западни държави, би имало пагубно въздействие върху продоволствената сигурност.
Конфликт на интереси
Авторите нямат конфликт на интереси за разкриване.
Благодарности
Благодарни сме на CGIAR и програмата CGIAR WHEAT за финансова подкрепа за изготвяне на преглед (Proiect No. A403 1.09.47), на който се основава тази статия. Rothamsted Research получава стратегическо финансиране от Съвета за биотехнологични и биологични науки (BBSRC) на Великобритания.
- Трябва ли да се притеснявам да ям „пълноценни“ протеини; Здравни основи от клиника в Кливланд
- Трябва ли да промените хранителните си навици след липосукция
- Наистина ли децата трябва да пият мляко, като ядат лесно
- Рецепта за чисто ядене на пълнозърнест хляб
- Всичко, което трябва да знаете за овеса и чистото хранене! Clean Food Crush