Асоциацията на затлъстяването с диабет тип 2 се признава от десетилетия и основната основа за тази връзка е способността на затлъстяването да породи инсулинова резистентност. Инсулиновата резистентност е основен аспект на етиологията на диабет тип 2 и също така е свързана с широк спектър от други патофизиологични последствия, включително хипертония, хиперлипидемия, атеросклероза (т.е. метаболитния синдром или синдром X) и поликистоза на яйчниците (1) . Въпреки че много подробности за механизмите, чрез които увеличената маса на мастната тъкан, която определя затлъстяването, причинява системна инсулинова резистентност, остават неизвестни, през последните няколко години станахме свидетели на експлозивно нарастване на нашето разбиране за това, което сега може да се нарича адипо-инсулинова ос. Има също така основания за разглеждане на свързаната с това възможност инсулиновата резистентност и хиперинсулинемията, освен че са причинени от затлъстяване, да допринесат за развитието на затлъстяване. В тази перспектива ще направим преглед на скорошния напредък, ще подчертаем области на спорове или несигурност и ще предложим подходи за изясняване на нерешените въпроси.
Инсулиново действие в адипоцита.
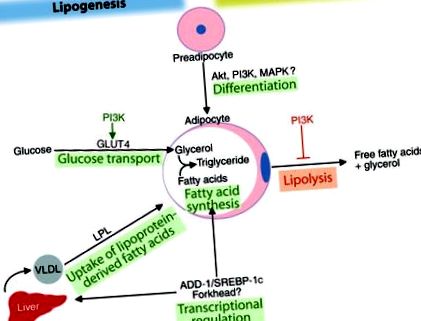
Инсулинът е критичен регулатор на почти всички аспекти на биологията на адипоцитите, а адипоцитите са един от най-силно реагиращите на инсулин клетъчни типове. Инсулинът насърчава запасите на адипоцитни триглицериди чрез редица механизми, включително насърчаване на диференциацията на преадипоцитите до адипоцити и, в зрелите адипоцити, стимулиране на транспорта на глюкоза и синтеза на триглицериди (липогенеза), както и инхибиране на липолизата (Фигура 1). Инсулинът също така увеличава усвояването на мастни киселини, получени от циркулиращите липопротеини, като стимулира липопротеиновата липазна активност в мастната тъкан. Метаболитните ефекти на инсулина се медиират от широк спектър от специфични за тъканите действия, които включват бързи промени в протеиновото фосфорилиране и функция, както и промени в генната експресия. Основното биологично значение на тези действия на инсулина се доказва от факта, че инсулиновата сигнална каскада, която инициира тези събития, се запазва до голяма степен при еволюцията от C. elegans към хората (2).
Плейотропни ефекти на инсулина за насърчаване на съхранението на мазнини. Инсулинът стимулира диференциацията на преадипоцитите до адипоцитите. В адипоцитите инсулинът насърчава липогенезата чрез стимулиране на усвояването на глюкоза и мастни киселини, получени от липопротеини и чрез индуциране на ADD-1/SREBP-1c, който регулира гените, стимулиращи синтеза на мастни киселини и липогенезата, не само в адипоцитите, но и в хепатоцитите. Инсулинът може също да регулира транскрипцията чрез транскрипционни фактори на Forkhead. Инсулинът намалява разграждането на триглицеридите чрез инхибиране на липолизата. Много от тези метаболитни пътища се регулират от сигналния път PI3K.
Инсулинова резистентност при затлъстяване и диабет тип 2.
Терминът "инсулинова резистентност" обикновено означава резистентност към ефектите на инсулина върху усвояването, метаболизма или съхранението на глюкоза. Инсулиновата резистентност при затлъстяване и диабет тип 2 се проявява чрез намаляване на стимулирания от инсулин транспорт на глюкоза и метаболизма в адипоцитите и скелетните мускули и от нарушено потискане на изхода на чернодробна глюкоза (1) Тези функционални дефекти могат отчасти да са резултат от нарушена инсулинова сигнализация във всичките три прицелни тъкани и, в адипоцитите, също и от понижаване на регулацията на главния глюкозен транспортер, реагиращ на инсулин, GLUT4. Както в мускулите, така и в адипоцитите, инсулинът се свързва с неговия рецептор, рецепторното фосфорилиране и активността на тирозин киназата и фосфорилирането на IRSs намаляват. Съществуват и специфични за тъканите промени: При адипоцитите от затлъстели хора с диабет тип 2, експресията на IRS-1 е намалена, което води до намалена активност на PI3K, свързана с IRS-1, и IRS-2 става основният докинг протеин за PI3K (14) . За разлика от това, в скелетните мускули на затлъстели пациенти с диабет тип 2, нивата на протеини IRS-1 и IRS-2 са нормални, но активността на PI3K, свързана с двете IRS, е нарушена (15).
Един механизъм за сигналните дефекти при затлъстяването може да бъде повишената експресия и активност на няколко протеинови тирозин фосфатази (PTPs), които дефосфорилират и по този начин прекратяват сигнализирането, разпространено чрез събития на тирозил фосфорилиране. Някои данни показват, че поне три PTPs, включително PTP1B, свързана с левкоцитния антиген фосфатаза (LAR) и src-хомология-фосфатаза 2, са повишени в експресията и/или активността в мускулите и мастната тъкан на затлъстели хора и гризачи (16) . Показано е, че PTP1B и LAR дефосфорилират инсулиновия рецептор и IRS-1 in vitro (16, 17). Всъщност мишките, при които PTP1B е нокаутиран, са повишили чувствителността към инсулин и устойчивостта към индуцирано затлъстяване (18, 19), поне отчасти, поради увеличения разход на енергия (19). Това предполага регулаторна роля за PTP1B не само в действието на инсулина, но и в енергийната хомеостаза. Интересното е, че инсулиновата чувствителност присъства в мускулите и черния дроб, но не и в адипоцитите (18, 19). Дали има причинно-следствена връзка между инсулиновата чувствителност и слабостта/разхода на енергия или те се регулират от независими сигнални пътища е ключов въпрос.
Други механизми също допринасят за инсулиновата резистентност при затлъстяване. При болестно затлъстяване, експресията на различни инсулинови сигнални молекули е намалена в скелетните мускули (20). При всички форми на затлъстяване и диабет, основен фактор, допринасящ за нарушения инсулин-стимулиран транспорт на глюкоза в адипоцитите, е понижаването на регулацията на GLUT4. Въпреки това, в скелетните мускули на затлъстели хора и хора с диабет експресията на GLUT4 е нормална (прегледана в справка 21) и изглежда, че дефектният транспорт на глюкоза се дължи на нарушена транслокация, докинг или сливане на GLUT4-съдържащи везикули с плазмената мембрана.
Въпреки че инсулиновата резистентност е характерна за затлъстяването и диабет тип 2, не е установено, че всички действия на инсулина са нарушени при индивиди и с двете състояния. Възможно е чернодробната липогенеза и съхранението на липиди да бъдат доведени до излишък в мастната тъкан, докато други инсулинови ефекти, свързани с глюкозната хомеостаза, са нарушени. Ще бъде важно да се идентифицират сигналните пътища и транскрипционните фактори, които биха могли да позволят такива противоречиви действия на инсулина.
Намалено изхвърляне на глюкоза в мастна тъкан при затлъстяване
Допълнителна подкрепа за потенциалната пряка роля на адипоцитите в регулирането на системната глюкозна хомеостаза идва от проучвания, при които гризачи или хора се лекуват с β3 адренергичен агонист CL316,243 (25, 26). Тъй като β3 адренергичните рецептори се експресират почти изключително в мазнини, очаква се ефектът от тези агенти да бъде иницииран от промени в мазнините. Лечението с CL316,243 води до повишена чувствителност както на усвояването на глюкоза в цялото тяло, така и на потискане на производството на чернодробна глюкоза (25). Тези ефекти са придружени от повишено усвояване на глюкоза в мастната тъкан без ефект при множество изследвани мускулни групи. По този начин, увеличаването на селективното усвояване на глюкозата в мазнините с агонисти на β3 адренергичните рецептори може да подобри усвояването на глюкозата в цялото тяло, като неблагоприятно ефектите върху мазнините водят до повишена чувствителност към инсулин в черния дроб. Алтернативно, β3 агонистите могат да действат, като променят освобождаването на някои адипоцитни продукти, които влияят върху системната инсулинова чувствителност.
Значението на местоположението на телесните мазнини за инсулиновата резистентност.
Връзката между затлъстяването и инсулиновата резистентност се наблюдава при всички етнически групи и е очевидна в целия диапазон на телесното тегло. Големи епидемиологични проучвания разкриват, че рискът от диабет и предполагаемо инсулинова резистентност се повишава, тъй като съдържанието на телесни мазнини (измерено чрез индекса на телесна маса [ИТМ]) се увеличава от много постно до много затлъстяло, което предполага, че ефект върху инсулиновата чувствителност в широк диапазон (27). Въпреки че тази връзка се наблюдава с мерки за затлъстяване като ИТМ, които отразяват общото затлъстяване, е от решаващо значение да се осъзнае, че всички места на затлъстяване не са равни в това отношение. Централните (интраабдоминални) складове за мазнини са много по-силно свързани с инсулиновата резистентност, диабет тип 2 и сърдечно-съдовите заболявания, отколкото периферните (глутеални/подкожни) мастни депа (28). Този факт относно чувствителността към мазнини и инсулин не е обяснен адекватно. Възможно е неизвестен общ фактор, генетичен или околна среда, да произвежда както инсулинова резистентност, така и централния модел на регионално затлъстяване и че централното затлъстяване всъщност не причинява инсулинова резистентност. Алтернативно, някои биохимични характеристики на интраабдоминалните адипоцити могат пряко да повлияят на системната инсулинова чувствителност.
Водеща хипотеза в това отношение е, че интраабдоминалните адипоцити са по-липолитично активни, отчасти поради комплемента им от адренергични рецептори. Това би увеличило интрапорталните нива на FFA и потока, което може да инхибира инсулиновия клирънс и да стимулира инсулиновата резистентност чрез механизми, които все още са несигурни. Хиперинсулинемията сама по себе си може да причини инсулинова резистентност чрез понижаване на регулирането на инсулиновите рецептори и десенсибилизиране на пострецепторните пътища, както беше потвърдено от свръхекспресията на инсулин в черния дроб на иначе нормалните трансгенни мишки. Този трансген води до намаляване на експресията на инсулиновия рецептор, непоносимост към глюкоза и хиперлипидемия, свързано с възрастта, без какъвто и да е първичен генетичен дефект в действието или секрецията на инсулина (прегледано в справка 29). Алтернативна хипотеза е, че тъй като сега е известно, че адипоцитите секретират много фактори, които могат да упражняват системни ефекти (виж по-долу), масивът от фактори, секретирани от интраабдоминални адипоцити, може да бъде особено вреден за системната чувствителност към инсулин. Засега тази хипотеза остава недоказана.
Адипоцити като ендокринни клетки.
Адипоцитите са добре известни със своята съществена роля като складове за съхранение на енергия за триглицериди, от които енергията се извиква по време на нужда под формата на FFAs и глицерол. Данните, появяващи се през последните няколко години обаче, установиха допълнителна роля за адипоцита, тази на секреторната клетка (Фигура (Фигура 2). 2). Адипоцитите експресират и секретират множество пептидни хормони и цитокини, включително TNF-α; плазминоген-активатор инхибитор-1, който помага за поддържане на хемостазата; ангиотензиноген, чийто протеолитичен продукт регулира съдовия тонус; и лептин, който играе централна роля в регулирането на енергийния баланс. Мастната тъкан също може да произвежда активни стероидни хормони, включително естроген и кортизол (30, 31). Чрез такива секретирани продукти адипоцитите имат способността да влияят на местната биология на адипоцитите, както и на системния метаболизъм на места, различни от мозъка, черния дроб, мускулите, β клетките, половите жлези, лимфоидните органи и системната васкулатура. Тази реализация поражда много възможности за допълнителни връзки между мастната функция или масата и инсулиновата резистентност, независимо от ролята на адипоцитите в съхранението и освобождаването на енергия (Фигура (Фигура 1 1).
Развиващ се поглед върху биологичните функции на адипоцита. Преди това адипоцитите се считаха за инертни складове, които освобождават гориво като мастни киселини и глицерол по време на гладуване или гладуване. Съвсем наскоро стана ясно, че адипоцитите са жлези с вътрешна секреция, които секретират важни хормони, цитокини, вазоактивни вещества и други пептиди. АНС, вегетативна нервна система.
Голям интерес проявява след откритието, че адипоцитите експресират и секретират цитокина TNF-α и че увеличените адипоцити от затлъстели животни и хора свръхекспресират този фактор (32). Въпреки че не всички проучвания са установили, че TNF-α е повишен при затлъстяване, нормалните циркулиращи нива на този фактор са на границата на откриване, което прави количествения анализ несигурен. Този нисък израз може да означава, че TNF-α действа по паракрин, а не по ендокринен начин. Следователно са необходими алтернативни подходи за оценка на ролята на TNF-α в системната инсулинова резистентност и в някои, но не във всички проучвания, използващи неутрализиращи антитела или други агенти за блокиране на TNF-α функция при животински модели, изглежда, че такава блокада повишава инсулиновата чувствителност ( 33).
TNF-α има много ефекти върху функцията на адипоцитите и те включват действия за инхибиране на липогенезата и за увеличаване на липолизата. Някои действия са разглеждани от някои като обратна връзка срещу прекомерното съхранение на енергия. Може ли прекомерният TNF-α да причини инсулинова резистентност? TNF-α сигнализирането уврежда инсулиновата сигнализация, отчасти чрез сериново фосфорилиране на IRS-1 (32, 33), и може да намали експресията на гена GLUT4, така че е създадена правдоподобна клетъчна основа за TNF-α като медиатор на инсулинова резистентност. Допълнителна подкрепа произтича от благоприятния ефект на нокаутирането на гени на TNFα или TNFα рецептори върху инсулиновата резистентност при няколко животински модели на свързана със затлъстяването инсулинова резистентност (32, 33). Въпреки това, подобряването на инсулиновата резистентност в отговор на загубата на TNF сигнализация е в най-добрия случай и ефектът от неутрализирането на TNF не е наблюдаван във всички експериментални модели. По този начин TNF-α може да допринесе частично за инсулиновата резистентност, но трябва да съществуват и други фактори.
Лептинът, продуктът на гена ob, може да бъде един такъв фактор. Този хормон, получен от адипоцити, упражнява плейотропни ефекти, включително дълбоки ефекти върху ситостта, енергийните разходи и невроендокринната функция (34). Най-убедителната роля на лептина от еволюционна гледна точка е способността му да служи като двупосочен сигнал, който превключва метаболитната физиология и невроендокринния статус между програми, подходящи за състоянията на хранене и глад. Предложената роля за повишаване на лептина като силен (адипостатичен) сигнал за предотвратяване на затлъстяването лесно се подкопава от устойчивостта към лептин. Тъй като увеличените запаси от енергия биха благоприятствали оцеляването в периоди на глад, адипостатичният аспект на действието на лептина може да е бил подбран по време на еволюцията (35). Този възглед за лептина като основно включен в превключвателя за глад/хранене не отрича факта, че липсата на лептин както при гризачи, така и при хора води до тежко затлъстяване, за което лептинът очевидно е лекарството. Нито намалява значението на определянето на молекулната основа за лептинова резистентност, което ограничава способността на повишаващия се лептин да предотврати затлъстяването в повечето ситуации.
Лептинът упражнява множество действия за регулиране на глюкозната хомеостаза чрез автокринни, паракринни, ендокринни и невронни вериги. Докато много от ефектите на лептина се медиират от ЦНС, някои ефекти могат да се проявят директно на нивото на инсулиновите целеви тъкани или панкреатичните островни клетки.
За разлика от гризачите, малкото хора с лептина или лептинови рецепторни мутации и затлъстяване не изглежда да имат извънредни степени на инсулинова резистентност, както се оценява от хиперинсулинемия, и никой досега не е описан с диабет (46, 47). Тази разлика може да бъде свързана с факта, че при хората, за разлика от мишките, лептинът има малък ефект върху оста на HPA. Ако се окаже, че лептинът има важно действие върху инсулиновата чувствителност при хората, както при мишките, тогава ще бъде важно да се определи степента, до която намаленото лептиново действие или лептинова резистентност допринася за инсулиновата резистентност при затлъстяване при хората.
Липотоксичност и липоатрофия: две страни на една и съща монета?
Има два допълнителни начина, по които промените във функцията на мастната тъкан могат да повлияят на глюкозната хомеостаза. В една, увеличеното съхранение на мастна енергия при затлъстяване води до увеличен поток на FFA към други тъкани и увеличено съхранение на триглицериди в тези тъкани, които насърчават инсулиновата резистентност и други неблагоприятни ефекти, наричани от някои като „липотоксичност“. В другата, парадоксално, липсата на мастна тъкан поражда много от същите резултати. Как да си обясним този парадокс?
Когато мастното депо се разшири, както при затлъстяването, плазмените FFA стават повишени, което се дължи най-вероятно на увеличеното освобождаване от разширената мастна маса и вероятно на нарушен чернодробен метаболизъм. Повишените FFAs увреждат способността на инсулина да потиска продукцията на чернодробна глюкоза и да стимулира усвояването на глюкоза в скелетните мускули, както и да инхибира секрецията на инсулин от β клетки на панкреаса. Дефектът в мускулите може да включва нарушено активиране на PI3K, вероятно поради повишаване на PKCθ (48). Придобитата загуба на активиране на PI3K в мускулите също се разглежда в резултат на диета с високо съдържание на мазнини (49). При хората съдържанието на триглицериди в мускулите корелира директно с инсулиновата резистентност, а мастнокиселинният състав на мускулните фосфолипиди влияе върху чувствителността към инсулцин (50). Трябва да научим много повече за механизмите, които стимулират натрупването на липиди в неадипозни тъкани, и механизмите, чрез които възниква такова липотоксично увреждане на функцията. Последните проучвания в β клетки предполагат, че дълговерижните мастни киселини могат да упражняват неблагоприятни ефекти чрез индуциране на свръхпроизводство на керамид (51). Ще бъде важно да се определи дали мастните киселини променят генната експресия чрез свързване като лиганди към транскрипционни фактори от семейството на активирания от пероксизома пролифератор (PPAR).
Прозрения от тиазоладиндиони и PPARγ.
Основен терапевтичен напредък при диабета е наличието на тиазоладиндиони (TZD), клас лекарства, които подобряват хипергликемията, поне отчасти чрез подобряване на инсулиновата чувствителност (прегледано от Olefsky, тази серия Perspective, реф. 56). Пробив в разбирането на техния механизъм на действие идва от осъзнаването, че рецепторът за тези лекарства е ядреният транскрипционен фактор PPARγ, предварително идентифициран като ключов транскрипционен фактор за адипогенезата. PPARy се активира от TZD, които се свързват с лиганд-свързващия домен и увеличават трансактивацията на целевите гени. Най-голямата експресия на PPARy е в адипоцитите, въпреки че съществена експресия се наблюдава в някои други тъкани, като имунни клетки и съдови клетки, и по-ниско ниво на експресия с неизвестно значение се наблюдава в тъкани като мускули и черен дроб. Фактът, че TZD действат чрез PPARy и че PPARγ се изразява предимно в мазнини, е нова мощна връзка между адипоцитите и инсулиновата резистентност. Каква точно е връзката?
Заключения и последици
Най-вероятно сложната оркестрация на връзката между мастната тъкан, действието на инсулина и хомеостазата на глюкозата се е развила поради необходимостта от оцеляване за поддържане на запасите от гориво, когато храната е оскъдна. Сега по време на изобилие в западното общество затлъстяването с придружаващите го заболявания достига епидемични размери и необходимостта от научен напредък за идентифициране на нови терапевтични подходи не може да бъде по-остра. Предизвикателството да се използва нарастващият репертоар на функциите на адипоцитите, за да се измести уравнението за приемане и използване на енергия към намалено съхранение на мазнини, има големи възможности да промени хода на човешкото заболяване.
Благодарности
Тази работа беше подкрепена от безвъзмездни средства от NIH (RO1 DK-43051, RO1 DK-28082 и PO1 DK-56116) и безвъзмездна помощ от Eli Lilly and Co. Авторите признават много допълнителни приноси в областта, които не са успели да цитират поради ограничение в броя на препратките. Авторите благодарят на Young-Bum Kim за експертна помощ.
- Затлъстяване; Инсулинова резистентност - как са свързани OMAMain
- Инсулиновата резистентност на майката променя развитието на панкреаса, увеличава риска от метаболитни нарушения в
- Ниацинът подобрява микробиома и инсулиновата резистентност; GT Health, ендокринология
- Механизъм на ER стрес и възпаление за чернодробна инсулинова резистентност при затлъстяване - FullText -
- Остеопонтинът е необходим за ранното начало на инсулинова резистентност, индуцирана от високо съдържание на мазнини при мишки